της Δήμητρας Σπανού Χημικού, Καθηγήτριας Δευτεροβάθμιας Εκπαίδευσης 1ου Γυμνασίου Δάφνης
Ένζυμα είναι πρωτείνες που έχουν καταλυτικές ιδιότητες. Ο ρόλος τους στον οργανισμό είναι σαφής . "Κοντρολάρουν" τις βιοχήμικές αντιδράσεις ώστε να γίνονται με τέτοιον τρόπο, που να μην βλάπτεται ο οργανισμός. Γιατί, ο οργανισμός θα είχε πολύ δυσάρεστες συνέπειες, εάν οι βιοχημικές αντιδράσεις γίνονταν ανεξέλεγκτα. Το PH ,οι διάφορες συγκεντρώσεις ουσιών, αλλά κυρίως οι μεταβολές στην θερμοκρασία θα έφερναν μοιραία αποτελέσματα για τον οργανισμό. Όπως έχουμε καταλάβει, οι περισσότεροι οργανισμοί ζουν μέσα σε στενά όρια εσωτερικών συνθηκών. Θερμοκρασίας συγκεντρώσεων ουσιών στα υγρά, πίεσης , οξύτητας.
Μέσα στο κύτταρο γίνονται συνεχώς πολυάριθμες χημικές αντιδράσεις που πρέπει να ολοκληρωθούν σε περιορισμένο χρονικό διάστημα χωρίς η θερμοκρασία να ξεπεράσει τους 37 βαθμούς Κελσίου. Αυτό γίνεται με την βοήθεια των ενζύμων που χαμηλώνουν την ενέργεια ενεργοποιήσεως και επεμβαίνουν στην ταχύτητα της αντίδρασης.
Όμως ουδέποτε μετακινούν το σημείο ισορροπίας της αντίδρασης αυτής το οποίο παραμένει ως έχει
Κάθε ένζυμο είναι εξειδικευμένο για μια αντίδραση που καταλύει στον οργανισμό. Κάποιες φορές παράγονται στην ανενεργή τπυς μορφή και ενεργοποιούνται σε διάφορα σημεία και από διάφορους παράγοντες αναλόγως. Φθείρονται ,αλλά αργά και διασπώνται σε αμινοξέα . Η αναστολή της δράσης τους αλλά και η φθορά τους εξαρτάται επίσης από άλλους παράγοντες όπως συγκεκριμένες ουσίες (π.χ. υδρολάσες ενζύμων) ή συνθήκες στον οργανισμό (π.χ. μεταβολή στις τιμές του PH.)
Η πραγωγή των ενζύμων οφείλεται σε νευρικά σήματα από το Κεντρικό Νευρικό Σύστημα, τα οποία μεταφέρουν αντίστοιχες εντολές σε συγκεκριμένα κύτταρα του οργανισμού. Αφού βέβαια πριν το ΚΝΣ έχει ειδοποιηθεί από αισθητικά κύτταρα για να ενεργήσει για την παραγωγή τους.
Αν ομαδοποιήσουμε τις βιοχημικές αντιδράσεις στον οργανισμό μπορούμε να έχουμε και μια κατηγοριοποίηση ομάδων ενζύμων ανάλογα με την δράση τους και με το ποιες αντιδράσεις καταλύουν . Έτσι μπορούμε να πούμε ότι έχουμε,
1.Οξειδάσες
 που καταλύουν τις οξειδώσεις ουσιών που ανάγονται (ελλάτωση του αριθμού οξείδωσης ) με πρόσληψη ηλεκτρονίων ή αφαίρεση πρωτονίων
που καταλύουν τις οξειδώσεις ουσιών που ανάγονται (ελλάτωση του αριθμού οξείδωσης ) με πρόσληψη ηλεκτρονίων ή αφαίρεση πρωτονίων
οι οποίες συνήθως έχουν την έννοια
α. της ενεργοποίησης-πρόσληψης οξυγόνου από την οξειδούμενη ουσία και τις καταλύουν οι οξειδάσες
β. της ενεργοποίησης- απομάκρυνσης υδρογόνου από την οξειδούμενη ουσία, καταλύουν οι δευδρογενάσες . Επί πλέον στις οξειδώσεις συναντάμε και άλλα ένζυμα όπως καταλάσες και υπεροξειδάσες, οξυγενάσες.
Τι θα συμβεί εάν καταστραφεί οξειδάση ή εάν εμποδιστεί η δράση της:
Σαν παράδειγμα οξειδάσης αναφέρουμε την οξειδάση του κυττοσώματος. Η πρωταρχική σημασία της φαίνεται όταν αυτή δεσμευτεί και εμποδιστεί έτσι η καταλυτική της δράση:
Οι κυανυούχες ουσίες που η δηλητηριώδης δράση οφείλεται στην είσοδο των CN- μέσα στα κύτταρα (ανταγωνιστικά) και την επίδρασή τους σε ένα ένζυμο που καταλύει αντιδράσεις απαραίτητες για την αναπνοή του κυττάρου και συγκεκριμένα την οξειδάση του κυτοχρώματος που είναι μια 
Ο οργανισμός δεν μπορεί να χρησιμοποιήσει το οξυγόνο σαν δέκτη Η+ και έτσι το οξυγόνο του αρτηριακού αίματος δεν χρησιμοποιείται αλλά επιστρέφει με το φλεβικό αίμα. Το φλεβικό αίμα εξακολουθεί να έχει το ζωηρό κόκκινο χρώμα του αρτηριακού και γι αυτό ένα χαρακτηριστικό ατόμων που έχουν δηλητηριαστεί από κυανυούχα είναι το ζωηρό κόκκινο χρώμα του δέρματος (και άλλα της ασφυξίας όπως, ιλλιγγος, διανοητική σύγχιση, υπερπνοια, δύσπνοια,αύξηση πίεσης).
2.Υδρολάσες
 που καταλύουν τις Υδρολύσεις οργανικών ουσιών δηλαδή την διάσπασή τους με την ταυτόχρονη πρόσληψη μορίων νερού. Οι Υδρολάσες, που καταλύουν υδρολύσεις οργανικών ουσιών ,όπως εστέρες (εστεράσες), πεπτιδικούς δεσμούς (πρωτεάσες πεπτιδάσες), σάκχαρα (γλυκοζυλάσες), ανυδρίτες οξέων (υδρολάσες ανυδρίτων οξέων). Οι υδρολάσες μπορούν επίσης να καταλύουν δεσμούς όπως άνθρακα-αζώτου, άνθρακα-άνθρακα, φωσφόρου- αζώτου, θείου- αζώτου, άνθρακα-φωσφόρου, θείου -θείου, άνθρακα- θείου.
που καταλύουν τις Υδρολύσεις οργανικών ουσιών δηλαδή την διάσπασή τους με την ταυτόχρονη πρόσληψη μορίων νερού. Οι Υδρολάσες, που καταλύουν υδρολύσεις οργανικών ουσιών ,όπως εστέρες (εστεράσες), πεπτιδικούς δεσμούς (πρωτεάσες πεπτιδάσες), σάκχαρα (γλυκοζυλάσες), ανυδρίτες οξέων (υδρολάσες ανυδρίτων οξέων). Οι υδρολάσες μπορούν επίσης να καταλύουν δεσμούς όπως άνθρακα-αζώτου, άνθρακα-άνθρακα, φωσφόρου- αζώτου, θείου- αζώτου, άνθρακα-φωσφόρου, θείου -θείου, άνθρακα- θείου.
Τι θα συμβεί εάν καταστραφεί η υδρολάση ή εάν εμποδιστεί η δράση της
Σαν παράδειγμα υδρολάσης μπορούμε να πάρουμε την εστεράση της χολινεστεράσης που προκαλέι υδρόλυση της ακετυλοχολίνης
όταν η τελευταία έχει εκπλήρώσει την διαβίβαση του μυνήματος και πρέπει να αποσυρυρθεί από τις συνάψεις . Το πόσο σημαντικός είναι ο ρόλος της εστεράσης αυτής το διαπιστώνουμε, εάν επιρρεαστεί ή καταστραφεί από τοξικές ουσίες . Όπως από ,
Εστέρες οργανοφωσφορικών ή και καρβαμιδικών, εάν βρεθούν στην περιοχή,(της νευροδιαβίβασης) λόγω εκλεκτικότητας, δηλαδή μεγαλύτερης χημικής συγγένειας,, δεσμεύουν την ακετυλοχολινεστερόσης (που υδρολύει την ακετυλοχολίνη)
Κατά συνέπεια ο νευροδιαβιβαστής ακετυλοχολίνη, παραμένει στις συνάψεις διαρκώς , γιατί λείπει το ένζυμο που θα τον υδρολύσει και αυτό κάνει τις νευρικές ίνες να είναι διαρκώς φορτισμένες.
Η συσσώρευση της ακετυλοχολίνης που παραμένει αδιάσπαστη είναι αγγειοδιαστολή, βραδυκαρδία, βροχοσπασμός, υπερίδρωση κ.α.)
2.
3. Λυάσες
που καταλύουν το σπάσιμο δεσμών μέσα στα μόρια, χωρίς όμως να γίνεται υδρόλυση
που καταλύουν οι Λυάσες . Οι Λυάσες αφαιρούν ομάδες από τα υποστρώματα δημιουργώντας διπλούς δεσμούς. Ένα τέτοι ένζυμο μπορεί να θεωρηθεί η ηλεκτρική αυδρογονάση που καταλύει την μετατροπή του ηλεκτρικού οξέος  σε φουμαρικό
σε φουμαρικό  στον κύκλο του Κρεμπς, Είναι ένα πολύπλοκο ένζυμο με συμπαράγοντες φλαβοπρωτείνες και αίμη
στον κύκλο του Κρεμπς, Είναι ένα πολύπλοκο ένζυμο με συμπαράγοντες φλαβοπρωτείνες και αίμη
Η μετατροπή γίνεται σε δυο στάδια
4. Τρανφεράσες
που καταλύουν
Την μεταφορά ομάδων από έναν δότη σε έναν αποδέκτη καταλύουν οι Τρανφεράσες, όπως οι φωσφορυλάσες, οι αποκαρβοξυλάσες, οι τρανσκετολάσες οι τρανζαμινάσες
Τι θα συμβεί εάν καταστραφούν ή επιρρεαστούν οι τρανφεράσες ή εμποδιστεί η δράση τους
Σαν παράδειγμα τρανφεράσης αναφέρω την κινάση κρεατίνης (φωσφοτρανφεράση) που καταλύει την μετατροπή της κρεατίνης σε φωσφοκρεατίνη χρησιμοποιόντας φωσφωρικές ρίζες από την τριφοσφωρική αδενοσίνη ATP η οποία μετατρέπεται σε ADP.

Η κινάση αυτή όπως και η ανάλογη που μετατρέπει το ADP σε ATP και συναντάται στους κύκλους της γλυκόλυσης και του κιτρικού οξέος επηρρεάζεται από τοξικές ουσίες όπως είναι οι δινιτροφαινόλες (εντομοκτόνα). Αυτό έχει συνέπεια την επιτάχυνση του ρυθμού της γλυκόλυσης και της κυτταρικής αναπνοής του συστήματος, (ώστε να εξασφαλιστεί το ATP). Όμως αντί αυτού η οξειδώσεις δεν καταλήγουν στον σχηματισμό δεσμών υψηλής ενέργειας του ATP αλλά την μεταβολή της απελευθερούμενης ενέργειας σε θερμότητα. (δηλητηρίαση από εντομοκτόνα)
5. Ισομεράσες
Την δημιουργία ισομερών των χημικών ουσιών καταλύουν αλλαγές μέσα στο μόριο. Μετατρέπουν το ένα ισομερές στο άλλο. που έχουν ίδιο μοριακό αλλά διαφορετική φυσική δομή που μπορεί να είναι διαφορετική δομική ή στερεοχημική δομή. Η ισομερίωση έχει ιδιαίτερη σημασία στην φύση γιατί συνήθως επικρατεί το ένα από τα δυο ισομερή πράγμα που συνήθως εξαρτάται από την διαφορά ενέργειας μεταξύ των ισομερών. Σε περίπτωση αμινοξέων στα οποία έχουμε μόρια με ασύμμετρο άτομο άνθρακα, βρίσκουμε τα δυο ισομερή D και L. Συνήθως σε ζωικούς οργανισμούς συναντάμε τα ισομερή L μορφής , ενώ σε φυτά και μικροοργανισμούς την D διαμόρφωση. Αντίστοιχη διαφορά εμφανίζουν οι πρωτείνες που περιέχουν τα αμινοξέα αυτά.
Η παρουσία ή η απουσία των ισομερασών έχει συνέπεια την εύρεση του ενός ή του άλλου από τα ισομερή που μπορεί να έχει διαφορετικά αποτελέσματα στην ταχύτητα των αντιδράσεων. Ακόμα δε και η εκλεκτικότητά τους.
Ενώ στην εργαστηριακή σύνθεση αμινοξέων λαμβάνεται ρακεμικό μείγμα, στην φύση, τα πρωτεινικής φύσης ένζυμα που καταλύουν αντιδράσεις σύνθεσης δείχνουν μεγαλύτερη εκλεκτικότητα σε ορισμένες μορφές ασύμμετρης δομής.
Οι Ισομεράσες είναι η φωσφογλυκομουτάση και η ισομεράση της φωσφοεξόζης


6. Συνθετάσες ή Λιγάσες

 Την συνένωση μορίων καταλύουν οι Συνθετάσες ή Λιγάσες
Την συνένωση μορίων καταλύουν οι Συνθετάσες ή Λιγάσες
H πρωτείνη συνθετάση του αμινοα- κυλο-tRNA. που είναι υπέύθυνη για την σύνδεση των αμινιξέων στο tRNA ώστε να μεταφερθούν στα ριβοσώματα και να σχηματίσουν τις πρωτείνες των ευκαρυωτικών κυττάρων (EF-2) . Εάν αλλάξειμε κάποιον τρόπο τότε αδρανοποιείται με συνέπεια να σταματά η σύνθεση πρωτεινών.Μια τέτοια περιπτωση έχουμε από την τοξίνη της διφθερίτιδας που αδρανοποιεί το ένζυμο αυτό γιατί του προσθέτει μια ADP ριβόζη στο διφθαμίδο (τροποποιημένος αμινοξύ της πρωτείνης )
Η ίδια λογική επικρατεί και στην κατασκευή μορίων σε άλλους οργανισμούς όπως σε βακτήρια
 Τι συμβαίνει εάν εμποδιστεί η δράση των συνθετασών
Τι συμβαίνει εάν εμποδιστεί η δράση των συνθετασών
Παράδειγμα συνένωσης πολλών μορίων είναι η κατασκευή κυτταρικών τοιχωμάτων σε βακτήρια με διασταυρούμενη σύνδεση κλώνων πεπτιδογλυκάνης. Το ένζυμο που καταλύει την αντίδραση είναι τρανσπεπτιδάση.
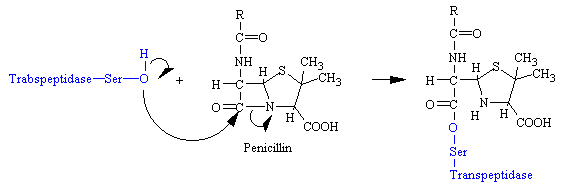
Φάρμακα με πενικιλλίνη εμποδίζουν αυτήν την συνένωση πεπτιδογλυκάνων για την κατασκευή των βακτηριακών τοιχωμάτων γιατί δεσμεύονται μη αντιστρεπτά με βακτηριακές γλυκοπεπτίδιο τρανσπεπτιδάσες.. Για τα βακτήρια αποτελεί δηλητήριο και ανασταλτικό παράγοντα πολλαπλασιασμού τους, ενώ για τον ανθρώπινο οργανισμό όταν πρόκειται για παθογόνα βακτήρια , φάρμακο.
Δήμητρα Σπανού
ΠΗΓΕΣ
Σημειώσεις Βιολογικής Χημείας. Α,Γρανίτσα .1966
Βιοχημεία Τεχνολογικής Κατεύθυνσης Γ τάξη Γενικού Λυκείου
https://en.wikipedia.org/wiki/Hydrolase
https://el.wikipedia.org/wiki/Ένζυμο
https://blogs.sch.gr/costas78/files/2008/08/proteines.pdf
Creatine kinase rxn.png
https://en.wikipedia.org/wiki/Kinase
https://en.wikipedia.org/wiki/Glucose-6-phosphate_isomerase

