H της Δήμητρας Σπανού, χημικού, μόνιμης καθηγήτριας Δ/θμιας Εκπ/σης 1ου Γυμνασίου Δάφνης
από το μουσικό έργο "Εδώ Λιλιπούπολη"(1980)
Το μικρό και το μεγάλο
Το μικρό και το μεγάλο
μια ανοιξιάτικη αυγή
πιάστηκαν από το χέρι
να γυρίσουνε τη Γη
Μπρος να πάνε κανει ζέστη
πίσω κρύο τσουκτερό
πάγωσε και το μεγάλο
έβρασε και το μικρό
Κι έτσι μπήκανε τα δυο τους
μ ένα βάζο τραχανά
σ' ένα ξύλινο σπιτάκι
πάνω στα ψηλά βουνά
Και με κλάματα και γέλια
πέσανε στον καναπέ
κι έμειναν εκεί για πάντα
δεν σηκώθηκαν ποτέ
Κι από το παραθυράκι
αγναντεύουνε μαζύ
μια την ασημένια νυκτα
μια τη μέρα την χρυσή
Το μικρό και το μεγάλο
κάνανε κι ένα μωρό
που δεν ήτανε μεγάλο
αλλά ούτε και μικρό
Και πιασμένα από το χέρι
ζήσανε πολύ καιρό
το χοντρούλι το μεγάλο
και το αδύνατο μικρό
στίχοι Μαριενίνας Kριεζή
ΕΙΣΑΓΩΓΗ
- Ας θυμόμαστε, ότι κατά την οξειδωτική διάσπαση των μεταβολιτών, ελευθερώνεται χημική ενέργεια η οποία αποθηκεύεται
κυρίως μέσω των χημικών δεσμών. Το ποσό που αποθηκεύεται σε χημικούς δεσμούς κυρίως φωσφορικών ενώσεων, μπορεί να υπολογιστεί από την υδρόλυτική διάσπαση των ενώσεων αυτών και εκφράζεται με την διαφορά ελεύθερης Ενέργειας Gibbs μεταξύ προιόντων και αντιδρώντων των χημικών αντιδράσεων. Το ποσό της ενέργειας που αποθηκεύεται είναι άλωτε χαμηλό (φωσφορικές ενώσεις χαμηλής ενέργειας) και άλλωτε μεγάλο (φωσφορικές ενώσεις υψηλής ενέργειας)
Συγκεκριμένα, οι ενεργειακές μεταβολές που συμβαίνουν πραγματοποιούνται με την παρεμβολή συζευγμένων φωσφορικών ενώσεων - φορέων όπως τα συνενζύμων όπως ATP, NAD, NADP, ή το CoASH κ.α, που είναι συνήθως ενώσεις υψηλής ενέργειας και απορροφούν και προσφέρουν ενέργεια με χημικές αντιδράσεις κατά την διάρκεια του μεταβολισμού.
κάποια παραδείγματα
ΑΠΟΦΩΣΦΟΡΥΛΙΩΣΕΙΣ.
( Απομακρύνεται μια φωσφορική ρίζα με ευνοική αντίδραση και ΔG<0)
| Φωσφορικό ακετύλιο | D G o = -47,3 kJ / mol |
| Η τριφωσφορική αδενοσίνη (ΑΤΡ) | D G o = -30,5 kJ / mol |
| 6-φωσφορική γλυκόζη | D Go = -13,8 kJ / mol |
| Φωσφονοενλοπυροσταφυλικό (PEP) | D G ο = -61,9 kJ / mol |
| Φωσφοκρεατίνη | D G o = -43,1 kJ / mol |
ακόμα αναγωγές
NAD + H2O ---> NADH + H+ + 1/2 O2 ΔG= 220 kj/mol
NADP + H2O --> NADPH + H+ + 1/2O2 ΔG= 220 kj/mol
ή φωσφορυλιώσεις ενώσεων
ATP + γλυκόζη ---> ΑDP + Pγλυκόζη ΔG = -13,8 kj/mol
Pi + GDP --> GTP και GTP + ADP --> GDP + ATP. Η ΔG-33,8kj/mol
ή υδρολυσεις
- Πρότυπες ελεύθερες ενέργειες υδρόλυσης μερικών φωσφορυλιωμένων ενώσεων
Ένωση kJ mol21 kcal mol21
Φωσφο-ενολοπυροσταφυλικό – 61,9 –14,8
1,3-Διφωσφογλυκερικό – 49,4 –11,8
Φωσφορική κρεατίνη – 43,1 –10,3
ATP (σε ADP) – 30,5 – 7,3 1
-Φωσφορική γλυκόζη – 20,9 – 5,0
Πυροφωσφορικό – 19,3 – 4,6 6
-Φωσφορική γλυκόζη – 13,8 – 3,3 3
-Φωσφορική γλυκερόλη – 9,2 – 2,2
Ακετυλο-CoA + Η2Ο -> οξικό + CoA + Η+ ΔG°ʹ = –31,4 kJ mol–1 (–7,5 kcal mol–1)
Η ωφέλεια που έχουμε σε ενέργεια από κάθε κύκλο Κρεμπς
- Σε κάθε κύκλο του Κρεμπς:
- σχηματίζεται ένας φωσφορικος δεσμός υψηλής ενέργειας GTP που μεταφέρεται άμμεσα στο ΑTP.
- δημιουργούνται τρια μόρια ανηγμένου NADH από NAD+, Τα δύο δημιουργούνται από καρβοξυλιώσεις και το ένα από οξείδωση.
- Δημιουργείται και ένα μόριο FADH2 (από οξείδωση με μειωμένη ενέργεια σε σχέση με το NADH) .
- Αποσπώνται 4 ζεύγη ηλεκτρονίων υψηλής ενέργειας και εκλύεται ενέργεια που μπορεί να συγκριθεί με ενέργεια 16 δεσμών υψηλής ενέργειας
Γενικά:
ΠΩΣ ΑΠΟ ΤΙΣ ΑΝΤΙΔΡΑΣΕΙΣ ΤΟΥ ΚΥΚΛΟΥ ΤΟΥ ΚΙΤΡΙΚΟΥ ΕΞΑΣΦΑΛΙΖΟΥΜΕ ΕΝΕΡΓΕΙΑ ΓΙΑ ΤΙΣ ΑΝΑΓΚΕΣ ΤΟΥ ΚΥΤΤΑΡΟΥ

Κατά τις οξειδώσεις που γίνονται στην μήτρα των μιτοχονδρίων κατά τον κύκλο του Κρεμπς αποσπώνται 2 άνθρακες από το κιτρικό οξύ που οξειδώνοται πλήρως προς διοξείδιο του άνθρακα.
Ταυτόχρονα από την οξείδωση αυτήν αποσπάται ενέργεια από τους μεταβολίτες. Αυτή η ενέργεια, όση δεν καταναλώνεται άμεσα (θερμότητα) περιλαμβάνεται στην ανηγμένη μορφή των συνενζύμων NADH και FADH2.
Πρέπει όμως να αποθηκευθεί, με τρόπο καταλληλότερο, ώστε να αποδίδεται ευκολότερα ενέργεια για τις ανάγκες του οργανισμου. Αυτός ο τρόπος είναι η ενέργεια σύνδεσης μιας τρίτης φωσφορικής ομάδας στην διφωσφορική αδενοσίνη (ADP) για τον σχηματισμό τριφωσφορικής αδενοσίνης (ATP).
Τα υδρογόνα του κιτρικού οξέος που οξειδώνεται μέσα στον κύκλου του Κρεμπς βρίσκονται στα τέλος του κύκλου, σε ανηγμένα συνένζυμα NADH , FADH2, με δεσμούς που περικλείουν μεγάλα ποσά ενέργειας.
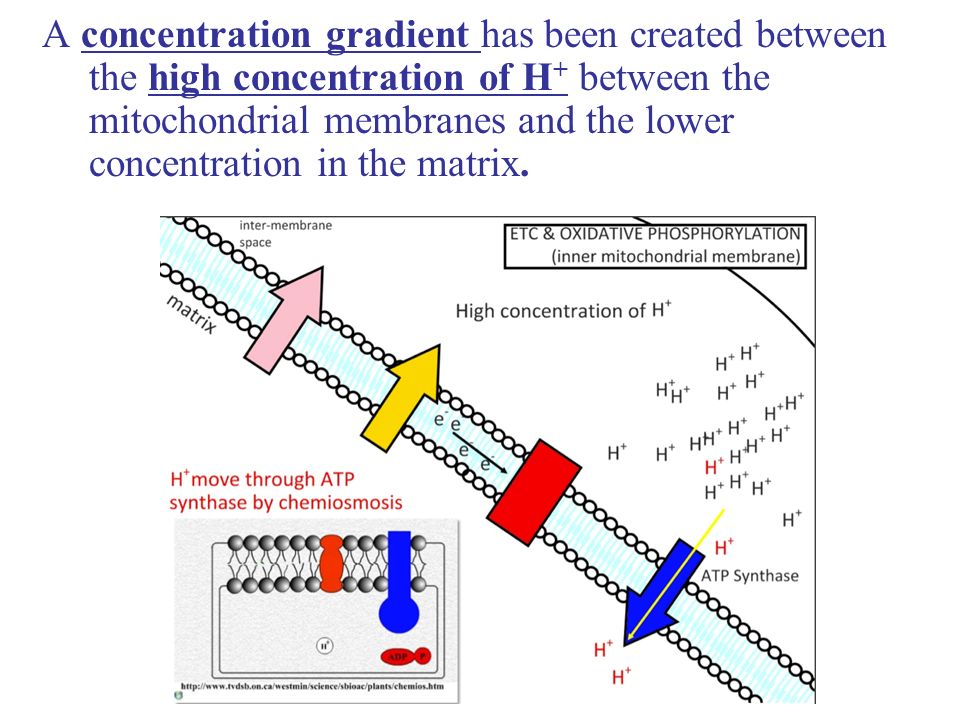
Η ενέργεια αυτή θα αποδεσμευθεί στο στάδιο της αναπνευστικής αλυσίδας και τα υδρογόνα θα καταλήξουν ενωμένα στο οξύγόνο σαν νερό με δεσμούς όμως πολύ χαμηλότερης ενέργειας.
Ας θυμόμαστε πως, κατά τις βιοχημικές αντιδράσεις , το ακέτυλοσυνένζυμοΑ είναι ο ιδανικός μεταφορέας ακετυλομάδων, το ATP είναι ο κυρίως μεταφορέας φωσφορικων ομάδων, ενώ τα ανηγμένα συνένζυμα NADH, NADPH, FADH2 είναι μεταφορείς υψηλής ενέργειας ηλεκτρονίων
Τα ανηγμένα συνένζυμα NADH, FADH2 που παράγονται μέσα στην μήτρα των μιτοχονδρίων από τον κύκλο Κρεμπς αλλά και από την λιπόλυση είναι ανάγκη να οξειδωθούν ώστε
- να εξακολουθήσουν να συμμετέχουν στον κύκλο (εφόσον οι ποσότητές τους είναι περιορισμένες), αλλά
- και για να αποδώσουν την ενέργεια η οποία εγκλείεται στις ανηγμένες μορφές τους.
Στις αντιδράσεις της αναπνευστικής αλυσίδας γίνεται μεταφορά ηλεκτρονίων και υδρογόνων από τα ανηγμένα συνένζυμα NADH και FADH2 που παράγονται στον κύκλο του Κρεμπς, που θα καταλήξουν στο οξυγόνο (που έχει φτάσει στα κύτταρα από τις πνευμονικές κυψελίδες μέσω του αίματος).
Για κάθε ζευγάρι ηλεκτρονίων που θα μεταφερθεί σταδιακά από το συνένζυμο NADH στο Ο2 ελευθερώνεται ενέργεια ΔG = -52,5 kcal/mol
Στο τελευταιο στάδιο του καταβολισμού συμβαίνουν δυο σημαντικές μεταβολικές πορείες συζευγμένες που συμβαίνουν παράλληλα
Α. Η ΕΠΑΝΑΔΗΜΙΟΥΡΓΊΑ ΟΞΕΙΔΩΜΕΝΩΝ ΣΥΝΕΝΖΥΜΩΝ ΜΕ ΜΕΤΑΦΟΡΑ ΤΩΝ ΗΛΕΚΤΡΟΝΙΩΝ ΚΑΙ ΤΩΝ ΥΔΡΟΓΟΝΩΝ ΑΠΟ ΤΗΝ ΟΞΕΙΔΩΣΗ ΣΤΟ ΟΞΥΓΟΝΟ ΚΑΙ
Β. Η ΦΩΣΦΟΡΥΛΙΩΣΗ ADP ΠΡΟΣ ATP
Α. ΑΝΤΙΔΡΑΣΕΙΣ ΑΝΑΠΝΕΥΣΤΙΚΗΣ ΑΛΥΣΙΔΑΣ
Τι είναι αναπνευστική αλυσίδα
Τα ηλεκτρόνια αυτά δεν μεταφέρονται απ ευθείας στο οξυγόνο αλλά η μεταφορά γίνεται σταδιακά με την βοήθεια 4 συμπλόκων και 2 μεταφορέων που στα ευκαριωτικά κύτταρα βρίσκονται τοποθετημένα στην εσωτερική μεμβράνη των μιτοχονδρίων. Η σειρά τους επαναλαμβάνεται κατά μήκος της μεμβράνης.
 Όλα μαζύ αποτελούν την αναπνευστική αλυσίδα.
Όλα μαζύ αποτελούν την αναπνευστική αλυσίδα.
Τα σύμπλοκα της εσωτερικής μιτοχονδριακής μεμβρανης που συμμετέχουν στην αναπνευστική αλυσίδα είναι τα εξής: NADH αφυδρογονάση (αναγωγάση) η ηλεκτρική οξειδάση, η ουβικινόνη (Q) , η κυτοχρωμική αναγωγάση, το κυτόχρωμα c και η κυτοχρωμική οξειδάση, πρωτόνια, αντλία πρωτονίων που συλλέγει πρωτόνια και τα επαναφέρει στην μήτρα.
Από αυτά τα δύο είναι βοηθητικά και αποτελούν υποστρώματα μεταφοράς ηλεκτρονίων και είναι η ουβικινόνη και το κυτόχρωμα c
(Να σημειώσουμε ότι αντίστοιχη αναπνευστική αλυσίδα υπάρχει και στους αερόβικά βακτήρια που είναι τοποθετημένη στην πλασματική μεμβράνη.
Επίσης χημικός μηχανισμός αποθήκευσης ενέργειας σε ανηγμένα συνένζυμα, μεταφορά ηλεκτρονίων στο οξυγόνο και αποθήκευση ενέργειας στο ΑΤP εμφανίζονται στα φυτά κατά την φωτοσύνθεση)
΄Τρία από αυτά τα σύμπλοκα I, II, IV μεταφέρουν πρωτόνια από την μήτρα των μιτοχονδρίων στον ενδιάμεσο χώρο. Συνέπεια αυτού είναι η πτώση του PH στον ενδιάμεσο χώρο C.
Αναλυτικότερα στην σειρά της αλυσίδας :
- Τα δύο πρώτα στη σειρά σύμπλοκα που είναι η 1.NADH αφυδρογονάση και η 2. ηλεκτρική οξειδάση. Βρίσκεται πάνω στην εσωτερική μιτοχονδριακή μεμβράνη συνδέονται άμεσα με τον κύκλο του κρεμπς και την παραγωγή ανηγμένων συνενζύμων μέσα στην μήτρα του μιτοχονδρίου κατά τις οξειδώσεις του κύκλου.

Το ενεργό κέντρο της NADH αφυδρογονάση βρίσκεται κυρίως στο εσωτερικό του μιτοχονδρίου όπου παράγωνται τα ανηγμένα συνένζυμα τα οποία οξειδώνει,
NADH--> NAD+ + H+ + 2e-
Όμως αλυσίδες πρωτεινών διασχίζουν την εσωτερική μεμβράνη του μιτοχονδρίου προς τον ενδιαμεσο χώρο και μια ειδική υπομονάδα της αποδίδει Η+ στον ενδιάμεσο χώρο.
Η διαφορά της NADH αφυδροογονάσης από την ηλεκτρική οξειδάση είναι πως, στην πρώτη καταυθάνουν NADH συνένζυμα που προκύπτουν από οξειδώσεις που γίνονται μέσα στην μήτρα του μιτοχόνδριου με την βοήθεια ενζύμων κατά τον κυκλο του Κρεμπς.
ενώ η , είναι ένζυμου το
- η ηλεκτρική οξειδ,άση, παρόλο που ακουμπά στην μιτοχονδριακή μεμβράνη είναι ένα ένζυμο οξείδωσης του ίδιου κύκλου του Κρεμπς στο 6ο βήμα του.
 Δεν βρίσκεται όμως μέσα στην μήτρα του μιτοχόνδριου αλλά είναι ενσωματωμένο στην εσωτερική μιτοχονδριακή μεμβράνη και έχει συνένζυμο το FAD. Το FAD προσλαμβάνει τα ηλεκτρόνια και τα υδρογόνα από την οξείδωση του ηλεκτρικού οξέος σε φουμαρικό,
Δεν βρίσκεται όμως μέσα στην μήτρα του μιτοχόνδριου αλλά είναι ενσωματωμένο στην εσωτερική μιτοχονδριακή μεμβράνη και έχει συνένζυμο το FAD. Το FAD προσλαμβάνει τα ηλεκτρόνια και τα υδρογόνα από την οξείδωση του ηλεκτρικού οξέος σε φουμαρικό,
κατά το 6ο βήμα του κύκλου Κρεμπς. (FAD)
Και τα δύο που είπαμε, προμηθεύουν την αναπνευστική αλυσίδα σε ηλεκτρόνια υψηλής ενέργειας, που τα εξάγουν από ανηγμένα συνένζυμα και τα αποδίδουν στον σύμπλοκο- μεταφορέα ουβικινόνη για να τα προωθήσει στα επόμενα σύμπλοκα της αναπνευστικής αλυσίδας .
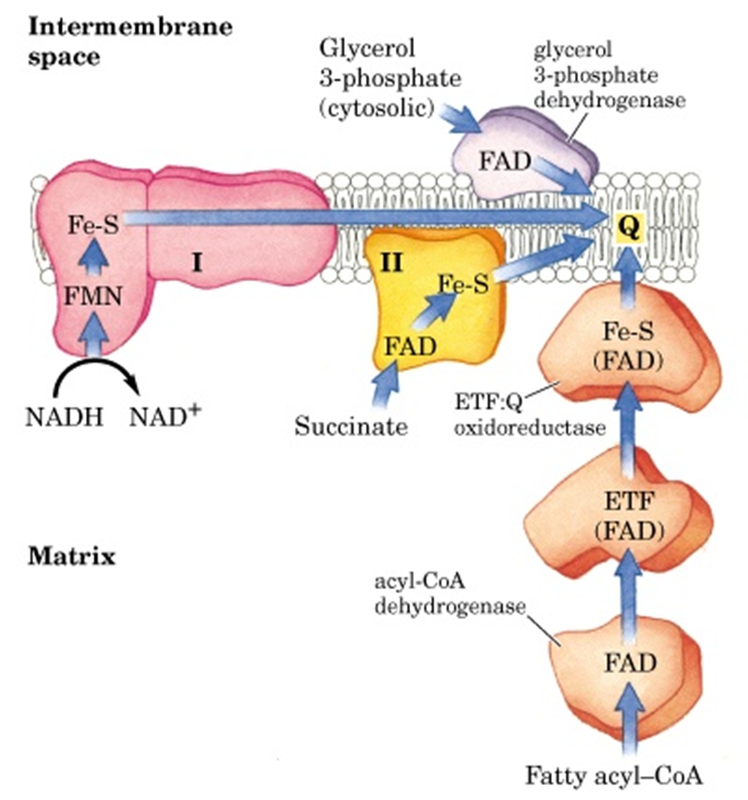
- Υπάρχει όμως και ένα άλλο ένζυμο, που δεν αναφέρεται συνήθως. Eίναι μια φλαβινοπρωτείνη η ETF αφυδρογονάση , που επίσης προμηθεύει υδρογόνα και ηλεκτρόνια την ουβικινόνη, όμως τα μαζεύει από άλλους κύκλους όπως γλυκόλυση ή β οξείδωση κ.α και τα αποδίδει στην ουβικινόνη
Δηλαδή,
Υδρογόνα και ηλεκτρόνια, προσλαμβάνονται αρχικά από τον πρώτο και δεύτερο σύμπλοκο, προωθούνται στην αλυσίδα που συνεχίζει με την ουβικινίνη (μεταφορέας) , το κυτόχρωμα σύμπλοκα που βρίσκονται στην εσωτερική μεμβράνη των μιτοχονδρίων έως ότου καταλήξουν στο οξυγόνο.

όπως αναφέρθηκε,
1. Για την απόσπαση ηλεκτρονίων από το NADH o κατάληλος φορέας είναι η NADH αφυδρογονάση, το πρώτο σύμπλοκο στην σειρά της αναπνευστικής αλυσίδας . Tο πρώτο σύμπλοκο μεταφέρει πρωτόνια και ηλεκτρόνια από τους δότες στους αποδέκτες δια μέσου της μεμβράνης
συγκεκριμένα,
Αρχικά δυο Η, το ένα από το FADH και ένα από το υδρογόνο μεταφέρονται στη κυτταχρωμική οξειδάση.τα ηλεκτρόνια στην NADHαφυδρογονάση μεταφέρονται πρώτα στο συνένζυμο FMN και
Η ενέργεια που ελευθερώνεται εδώ είναι ΔG =9,2 kcal/mol
Στη συνέχεια σε μια χημική ένωση που λέγεται ουμπικινόνη
- To δεύτερο σύμπλοκο η ηλεκτρική οξειδάση που όπως είπαμε βρίσκεται κατ΄εξαίτερη πάνω στην μεμβράνη, (αντί να βρίσκεται στην μήτρα των μιτοχονδρίων όπου γίνονται οι υπόλοιπες αοξειδώσεις του κύκλου), αποσπά υδρογόνα από το ηλεκτρικό οξύ και έχει συνένζυμο μια το FAD που μετατρέπεται σε FADH2 ανηγμένο συνένζυμο Q. Η ενέργεια που ελευθερώνεται από αυτό είναι DG = 4,6kcal/mol .......
-
 Κατά την διάρκεια των οξειδώσεων αυτών από τα δύο πρώτα σύμπλοκα, κατιόντα υδρογόνου και ζευγος ηλεκτρονίων, αφού πρώτα οξειδώσουν την ουβικινόνη (που είναι η επόμενη στην σειρά) μεταφέρονται τα μεν πρωτόνια στον διαμεμβρανιακό χώρο των μιτοχονδρίων (ανάμεσα στην εσωτερική και στην εξωτερική μεμβράνη) και τα δε ηλεκτρόνια στην ουβικινόνη. Αυτό έχει συνέπεια την μεταβολή στο PH και συνεπώς την ανάπτυξη ενός δύναμικού μεταξύ των δυο πλευρών της εσωτερικής μεμβράνης των μιτοχονδρίων. (Πρωτοκινητική δύναμη)
Κατά την διάρκεια των οξειδώσεων αυτών από τα δύο πρώτα σύμπλοκα, κατιόντα υδρογόνου και ζευγος ηλεκτρονίων, αφού πρώτα οξειδώσουν την ουβικινόνη (που είναι η επόμενη στην σειρά) μεταφέρονται τα μεν πρωτόνια στον διαμεμβρανιακό χώρο των μιτοχονδρίων (ανάμεσα στην εσωτερική και στην εξωτερική μεμβράνη) και τα δε ηλεκτρόνια στην ουβικινόνη. Αυτό έχει συνέπεια την μεταβολή στο PH και συνεπώς την ανάπτυξη ενός δύναμικού μεταξύ των δυο πλευρών της εσωτερικής μεμβράνης των μιτοχονδρίων. (Πρωτοκινητική δύναμη) - Tα πρωτόνια επανέρχονται στο εσωτερικό (μήτρας μέσω του τελευταίου σύμπλοκου που είναι η ATP συνθετάση και παίζει ρόλο αντλίας πρωτονίων.
- Η ουμπικινόνη Q είναι o πρώτος κινητός μεταφορέας της αναπνευστικής αυσίδας.
 Συλλέγει και μεταφέρει ηλεκτρόνια από το πρώτο σύμπλοκο (ΝADH αφυδρογονάση) και από το δεύτερο (Ηλεκτρική οξειδάση και FAD) και τα μεταφέρει , προς στο σύμλοκο κυτόχρωμα cb-c1. Εκεί τα ηλεκτρόνια αρχικά παραλαμβάνει το κυττόχρωμα cb, που ανάγεται. Στην συνέχεια το ζευγάρι των ηλεκτρονίων παραλαμβάνεται από το κυττόχρωμα c1 το οποίο ανάγεται, ενώ ταυτόχρονα το κυττόχρωμα cβ οξειδώνεται .
Συλλέγει και μεταφέρει ηλεκτρόνια από το πρώτο σύμπλοκο (ΝADH αφυδρογονάση) και από το δεύτερο (Ηλεκτρική οξειδάση και FAD) και τα μεταφέρει , προς στο σύμλοκο κυτόχρωμα cb-c1. Εκεί τα ηλεκτρόνια αρχικά παραλαμβάνει το κυττόχρωμα cb, που ανάγεται. Στην συνέχεια το ζευγάρι των ηλεκτρονίων παραλαμβάνεται από το κυττόχρωμα c1 το οποίο ανάγεται, ενώ ταυτόχρονα το κυττόχρωμα cβ οξειδώνεται . - Η συνολική ενέργεια και των δυο οξειδαναγωγικών αντιδράσεων που ελευθερώνεται στο τρίτο σύμπλοκο είναι DG= 11,6kcal/mol. Το δυναμικό οξειδοαναγωγης υπολογίζεται μεταξύ του οξειδοαναγωγικού ζεύγους Ουβικινόνη/κυττόχρωμα c
- Το κυττόχρωμα C που είναι κινητό σύμπλοκο ο δεύτερος κινητός μεταφορέας στην αναπνευστική αλυσίδα, μεταφέρει τα ηλεκτρόνια από το τρίτο σύμπλοκο cb-c1 στο τέταρτο σύμπλοκοca-ca3 . Τo τέταρτο σύμπλοκο αποδέκτης των ηλεκτρονίων λέγεται κυτοχρωμική οξειδάση. (ή κυττόχρωμα α) Τα ηλεκτρόνια μεταφέρονται εκεί από το κινητό σύμπλοκο κυττόχρωμα c. ενώ τα Η+ μεταφέρονται εκεί ξεχωριστά.
- Έμμεσα απαιτείται οξυγόνο που είναι ο τελικός αποδέκτης των πρωτονίων που αντλούνται από την αναερόβια γλυκόλυση και από τον κύκλο του Κρεμπς μέσω ανηγμένων συνενζύμων . H ενέργεια που ελευθερώνεται κατά την μεταφορά του ζεύγους ηλεκτρονίων από το κυττόχρωμα α στο οξυγόνο είναι ΔG= 23,1kcal/mol. Η συγκέντρωση οξυγόνου επρρεάζει τον ρυθμό της αναπνευστικής αλυσίδας και οξυδωτικής φωσφορυλίωσης.
Κατά την αναπνευστική αλυσίδα,
Η ενεργεια που ελευθερώνεται από το ανηγμένο συνένζυμο NADH κατά την οξείδωσή του (DG= -152,8kj/mol) είναι ποσοτικά περισσότερη από όση χρειάζεται για την δημιουργία μορίων ATP (DG= -30,5kj/mol) και με δεδομένο ότι μονο τα 40% από αυτήν του συνένζυμου χρεισιμοποιείται για την παραγωγή ΑΤP, για κάθε μόριο NADH που ανάγεται δημιουργουνται 2,5 μόρια ATP. Με αντίστοιχους υπολογισμούς από ένα μόριο ανηγμένου FADH2 η ενέργεια που αποδίδεται είναι ικανή για την δημιουργία 1,5 μορίων ATP από φωσφορυλίωση ADP.
Τα κυττοχρώματα που έχουν ερευνηθεί, περιέχουν σαν προσθετική ομάδα τον δακτύλιο της πρωτοπορφυρίνης ενωμένο με σίδηρο και για αυτόν τον λόγο οι ιδιότητές τους είναι ανάλογες με την αιμοσφαιρίνη..Η αλυσίδα των κυττοχρωμάτων, μεταφέρι μόνο ηλεκτρόνια, όχι υδρογόνα, έτσι η οξείδωση και η αναγωγή στα κυττοχρώματα οφειλεται στο σθένος του σιδήρου).
Τι αποτέλασμα έχει η δράση των 4 πρώτων συμπλόκων
α. η ενέργεια που αποβάλεται από ανηγμένα συνένζυμα ΝΑDH και FADH2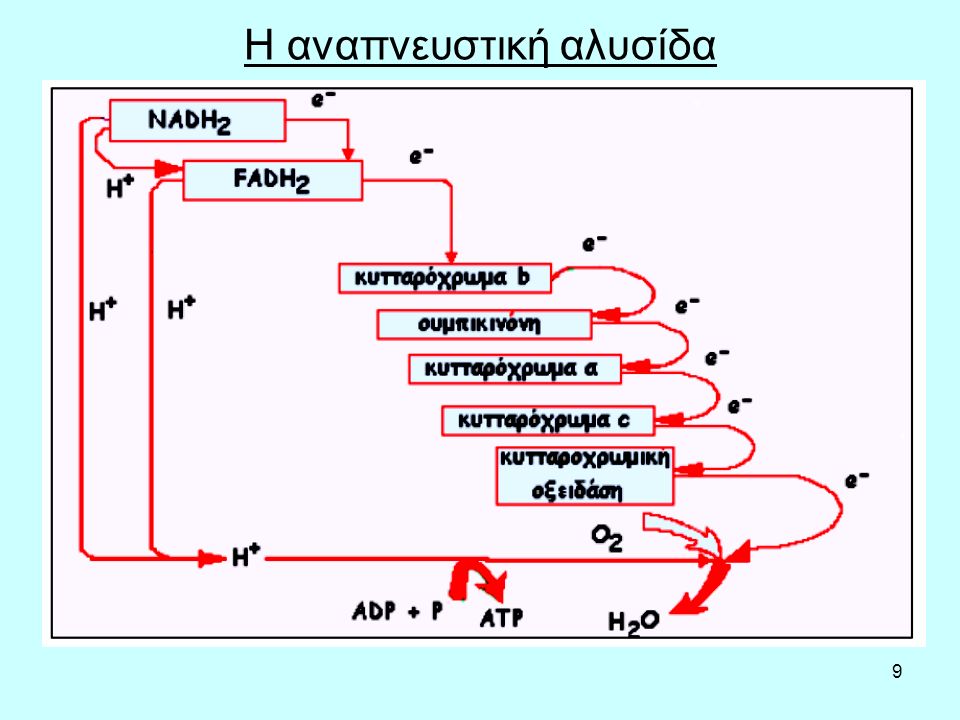
Σε κάθε έναν από αυτούς τους φορείς τα ηλεκτρόνια υψηλής ενέργειας (από NADH FADH2) αποδίδουν ένα μέρος από την ενέργεια αυτήν για να μεταφερθούν τελικά στο οξυγόνο σαν ηλεκτρόνια χαμηλότερης ενέργειας.
Από την ενέργεια που αποσπάται από τα ηλεκτρόνια υψηλής ενέργειας των ανηγμενων συνενζύμων, το 40% αποθηκεύεται στο ATP με την διαδικασία της οξειδωτικής φωσφορυλίωσης.
To οξυγόνο που καταυθάνει στα κύτταρα μέσω της αναπνευστικής οδού, προσλαμβάνοντας πρωτόνια μετατρέπεται σε νερό.
Από το ατμοσφαιρικό οξυγόνο της αναπνοής το95% μετατρέπεται σε νερό.
Το συνολικο φαινόμενο περιγράφεται από την αντίδραση
NADH + H+ + 1/2O2 --> ΝΑD+ + H2O ΔG = - 220kj/mol
Δυναμικό οξειδοαναγωγής μεταξύ οξειδωμένης και ανηγμένης μορφής .
Αρχικά για το οξειδοαναγωγικό ζεύγος ΝADH/NAD έχει δυναμικο οξειδοαναγωγής -320mV ενώ στην τελική τους κατάληξη στο νερό Η2Ο/Ο2 το δυναμικό του οξειαναγωγικού ζεύγους κατεβαίνει στο +810mV
Τα συνένζυμα αυτά εφόσον απομακρύνονται τα υδρογόνα τους, μετατρέπονται σε οξειδωμένα NAD και FAD όπως είναι απαραίτητογια να συνεχίσει ο κύκλος το κιτρικού οξέο.
Επίσης με τα ηλεκτρόνια που απομακρύνονται τα συνένζυμα που οξειδώνονται, ελευθερώνουν ενέργεια.
Οξείδωση ανηγμένου συνένζυμου προς αντίστοιχο οξειδωμένο:NADH --> NAD+ + H+ + 2e DG= -158,2kj/mol
Αναγωγή του μοριακού οξυγόνου προς νερό: 1/2 O2 + 2H+ + 2e- --> H2O DG= --61,9kj/mol
Συνολικό ΔG = -220,1kj/mol

Έτσι η οξείδωση 1 μορίου ΝΑDH τελικά αντιστοιχεί στην παραγωγή 1/2 μορίου νερού και παράγωνται ταυτόχρονα 3 μόρια ΑΤΡ.
3ADP3- + 3 HPO42- + 3H+ --> 3 ATP4- +3 H2O DG =3. 35,5kj/mol = 106,5kj/mol
β . φωσφορυλίωση του ADP προς ATP.
Αυτό το δυναμικό της εσωτερικής μιτοχονδριακής μεμβράνης, είναι η κινητήρια δύναμη για την φωσφορυλίωση του ADP προς ATP.
Η απόσπαση αυτών των ηλεκτρονίων πρωτόνια από τα ανηγμένα συνένζυμα και στην συνέχεια η συσσώρευση των Η+ στο εξωτερικό μέρος της όπως είδαμε γίνεται με την βοήθεια των συμπλόκων Ι, ΙΙ, ΙV.
H μεταφορά τους ξανά στην μιτοχονδριακή μήτρα επιτυγχάνεται με το σύμπλοκο V που είναι η ΑΤP συνθετάση. Το σύμπλοκο αυτό αποτελείται από πρωτείνες με διαφορετικές λειτουργίες.
Η ηλεκτροχημική δύναμη που αναπτύσεται μπορεί να εκτονωθεί μονο μέσα από ειδικές πύλες όπως η συνθετάση του ΑΤP . Αυτό το μεγάλο διαμεμβρανιακό ένζυμο δημιουργεί ειδικές διόδους πρωτονίων. Καθώς τα πρωτόνια διαπερνούν τις διόδους αυτές, προωθούν μια μη ευνοική αντίδραση . Την φωσφορυλίωση της ADP προς ΑΤP. κατά την αντίδραση
|
|
|
ADP3- + HPO42- + H+ --> ATP4- + H2O DG = 35,5kj/mol
ΟΞΕΙΔΩΤΙΚΗ ΦΩΣΦΟΡΥΛΙΩΣΗ
Η σύνθεση του ATP από ΑDP και HPO4- σε ξεχωριστό χώρο αλλά πολύ κοντά στην αναπνευστική αλυσίδα.
Κατά την διαδικασία της αναπνευστικής αλυσίδας στο μιτοχόνδριο, τα Η+ που παράγωνται από την υδρόλυση του NADH και FADH2 διαπερνούν λόγω ωσμωτικών φαινομένων και στην εκλεκτική διαπερατότητα την εσωτερική μιτοχονδριακή μεμβράνη και συσσωρεύονται στο εξωτερικό μέρος της μεμβράνης αυτής, μεταξύ της εξωτερική και εσωτερικής μτοχονδριακής μεμβράνης .
Όμως Η+ μεταφέρονται στον ίδιο χώρο και Τα Η+ που συσσωρεύονται στο εξωτερικό μέρος της μεμβράνης αυτής, έχουν σαν αποτέλεσμα να δημιουργείται ηλεκτροχημική κλίση γραμμικά μεταβαλλόμενη μεταξύ των δυο πλευρών της μεμβράνης. Δημιουργείται ηλεκτρική διπλοστοιβάδα από τις δυο πλευρές της μιτοχονδριακής μεμβράνης αυτήν προς την μήτρα και την άλλη προς τον ενδιάμεσο χώρο.
Η ηλεκτροχημική δύναμη που αναπτύσεται μπορεί να εκτονωθεί μονο μέσα από ειδικές πύλες όπως η συνθετάση του ΑΤP . Αυτό το μεγάλο διαμεμβρανιακό ένζυμο δημιουργρεί ειδικές διόδους πρωτονίων.Τα πρωτόνια επανέχονται στην μήτρα με την ΑΤP συνθετάση. Καθώς τα πρωτόνια διαπερνούν τις διόδους της μιτοχονδριακής ATP συνθετάσης, προωθούν μια μη ευνοική αντίδραση . Την φωσφορυλίωση της ADP προς ΑΤP. κατά την αντίδραση αυτή ενέργεια
|
|
|
Για την φωσφορυλίωση του ADP απαιτούνται 35,5kj/mol ADP3- + HPO42- + H+ --> ATP4- + H2O DG = 35,5kj/mol
που ελευθερώνεται από την οξείδωση του NADH στο σύμπλοκοΙ NADH + H+ + 1/2O2 --> ΝΑD+ + H2O ΔG = - 220kj/mol
το σύμπλοκο V που είναι η ΑΤP συνθετάση. Το σύμπλοκο αυτό αποτελείται από πρωτείνες με διαφορετικές λειτουργίες.
ΚΙΝΗΣΗ ΣΩΜΑΤΩΝ ΔΙΑ ΜΕΣΟΥ ΤΗΣ ΜΙΤΟΧΟΝΔΡΙΑΚΗΣ ΜΕΜΒΡΑΝΗΣ
Για να συμβούν όμως Η οξειδωτική φωσφορυλίωση και η αναπνευστική αλυσίδα, , είναι απαραίτητη η δυνατότητα κίνησης ουσιών που συμετέχουν δια μέσου της εσωτερικής μιοχονδριακής μεμβράνης . Η ώσμωση είναι συνήθως η δύναμη που κινεί ουσίες διαμέσου της μεμβράνης. Μικρά μόρια μπορούν να περνούν από την μεμβράνη με αυτόν τον τρόπο αλλά όχι μικρά ιόντα
Το ATP που δημιουργείται στην μιτοχονδριακή μήτρα είναι αρνητικά φορτισμένο
Tα φωσφορικά που απαιτούνται για την οξειδωτική φωσφορυλίωση, η μεταφορά τους γίνεται από ειδικό ένζυμο και σε ουδέτερο PH.
ο μηχανισμός πρέπει να περιλαμβάνει είτε την ανταλλαγή Η2ΡΟ4 - για την ΟΗ, είτε την αμοιβαία μεταφορά Η2ΡΟ4 - με Η + .
Η2ΡΟ4 - ί + ΟΗ - R = Η2ΡΟ4 - Κ + ΟΗ - Ι ή Η2ΡΟ4 - L + Η + L <==> Η2ΡΟ4 - Κ + Η + Κ
Η μεταφορά κατιόντων υδρογόνου στην μήτρα του μιτοχόνδριου, γίνεται μέσω του συμπλέγματος V που είναι η συνθετάση της ATP
Δήμητρα Σπανού
ΠΗΓΕΣ
ΒΙΟΧΗΜΕΊΑ pETER Karlson
https://www.ncbi.nlm.nih.gov/books/NBK9903/
https://legacy.cup.gr/Files/files/stryer-chap-15.pdf
https://legacy.cup.gr/Files/files/stryer-chap-15.pdf
Σημειώσεις Βιοχημείας
The cell Α molecular approache. Cooper GM
https://slideplayer.gr/slide/11571075/
akatergasto
ακετυλ CoA και παράγεται ένα μόριο NADH στη διαδικασία. Το συνένζυμο Α (CoA-SH) είναι ένας γενικός φορέας ττομάδων ακυλίου σε μία ποικιλία αντιδράσεων.
ΠΗΓΕΣ
https://mde-didaktiki.biol.uoa.gr/mde10/vlondartsik/organ9.html
https://slideplayer.com/slide/8081600/
ακατεργαστο
μεταφορά ΑΤΡ, ADP και φωσφορικού άλατος μέσω της μεμβράνης μιτοχονδρίων
Η σύνθεση ή υδρόλυση του ΑΤΡ με άθικτα μιτοχόνδρια συμβαίνει στο χώρο της μήτρας, επειδή οι καταλυτικές θέσεις είναι στην κεφαλή F1 της γλειφιτζούρας της συνθετάσης ΑΤΡ, η οποία προβάλλει στην πλευρά της μήτρας (Ν-φάση) της μεμβράνης. Παρ 'όλα αυτά, τα μιτοχόνδρια είναι ικανά να υδρολύουν ταχέως εξωτερικά προστιθέμενο ΑΤΡ και να συνθέσουν ΑΤΡ εκτός από προστιθέμενη ΑϋΡ και φωσφορικά. Αυτό είναι δυνατό λόγω δύο συστημάτων μεταφοράς που επιτρέπουν σε αυτούς τους μεταβολίτες να διασχίζουν τη μεμβράνη:
- Ο μεταφορέας νουκλεοτιδίου αδενίνης .
Αυτό το ένζυμο καταλύει την ανταλλαγή του ΑΤΡ για ADP διαμέσου της εσωτερικής μιτοχονδριακής μεμβράνης. Οι χρεώσεις επί των υποστρωμάτων είναι τέτοιες ώστε η ΑΤΡ φέρει καθαρό υπερβάλλον φορτίο -1 σε σύγκριση με την ADP.
Η αντίδραση ανταλλαγής είναι επομένως ηλεκτρογόνος και οδηγείται από το ηλεκτρικό στοιχείο ( Dy ) της βαθμίδας πρωτονίων, έτσι ώστε να ευνοείται η είσοδος της ADP και η έξοδος του ΑΤΡ.Σε, ή Ν-φάση  Out ή P-φάση
Out ή P-φάσηΗ θερμοδυναμική αυτής της διαδικασίας , συζητείται λεπτομερέστερα εδώ.
- Ο μεταφορέας φωσφορικών .
Ο μεταφορέας φωσφορικών ήταν ο πρώτος από τους μεταφορικούς μιτοχονδριακούς μεταφορικούς φορείς που πρέπει να αποδειχθούν (Chappell and Crofts, 1965). Το ένζυμο καταλύει την καθαρή μεταφορά Η3ΡΟ4 κατά μήκος της μεμβράνης με ουδέτερη διαδικασία. Δεδομένου ότι το κυρίαρχο ιοντικό είδος που υπάρχει στο ουδέτερο pH είναι H 2 PO 4 - , ο μηχανισμός πρέπει να περιλαμβάνει είτε την ανταλλαγή Η2ΡΟ4 - για την ΟΗ, είτε την αμοιβαία μεταφορά Η2ΡΟ4 - με Η + .Η2ΡΟ4 - ί + ΟΗ - R = Η2ΡΟ4 - Κ + ΟΗ - Ι ή
Η2ΡΟ4 - L + Η + L <==> Η2ΡΟ4 - Κ + Η + Κ
Η ανταλλαγή επιτρέπει στο χημικό συστατικό της βαθμίδας πρωτονίων (-Z D pH) να οδηγεί την πρόσληψη φωσφορικού άλατος στο μιτοχόνδριο.
Η καθαρή επίδραση αυτών των δύο διεργασιών μεταφοράς είναι ότι η βαθμίδα πρωτονίων οδηγεί τη συγκέντρωση ADP και φωσφορικών στο εσωτερικό του μιτοχονδρίου και την εξαγωγή του ΑΤΡ, εις βάρος της σύνθεσης 1H + / ATP.
Περισσότερες γενικές πτυχές της θερμοδυναμικής των μεταφορών καλύπτονται εδώ.
Μεταβολική μεταφορά
Τα μιτοχόνδρια έχουν ποικίλες μεταβολικές λειτουργίες, οι οποίες ποικίλλουν από ιστό σε ιστό. Στα μιτοχόνδρια του ήπατος, μια μεγάλη ποικιλία εξωτερικά προστιθέμενων υποστρωμάτων μπορεί να υποβληθεί σε επεξεργασία από το μιτοχονδριακό μεταβολικό μηχανισμό. Τα ένζυμα είναι κατά κύριο λόγο στη μήτρα, απαιτώντας τα υποστρώματα να μεταφέρονται διαμέσου της εσωτερικής μεμβράνης μιτοχονδρίων. Η μεταφορά καταλύεται από μια υπεροικογένεια πρωτεϊνών, οι οποίες παρουσιάζουν ισχυρή ομολογία αλληλουχίας σε όλο το φάσμα του ευκαρυωτικού κόσμου, αλλά δεν υπάρχει προφανής προκαρυωτικός πρόδρομος. Οι μεταφορείς μεταβολιτών γενικώς καταλύουν ουδέτερες ανταλλαγές, αλλά μερικές είναι ηλεκτρογενείς, ή περιλαμβάνουν μεταφορές H + ή ανταλλαγή ΟΗ, έτσι ώστε η ισορροπία μεταφοράς να καθορίζεται από τη βαθμίδα πρωτονίων.
Η διόγκωση των μιτοχονδρίων στα άλατα αμμωνίου των ασθενών οξέων ή μεταβολιτών
Οι δραστηριότητες μεταφοράς για τα συστήματα μεταβολίτη επιδείχθηκαν για πρώτη φορά με τη χρήση μιας απλής και κομψής τεχνικής που εισήγαγε ο Brian Chappell. Η τεχνική εξαρτάται από τα ακόλουθα:
- Τα μιτοχόνδρια συμπεριφέρονται ως τέλεια όσμωρα. Ανταποκρίνονται σε μεταβολές στην οσμωτική πίεση του μέσου εναιώρησης με συρρίκνωση (ή διόγκωση) καθώς το νερό ρέει διαμέσου της μεμβράνης για να αντισταθμιστεί η διαφορά δραστικότητας όταν τα οσμολύματα προστίθενται (ή απομακρύνονται) από το εξωτερικό μέσο.
- Η μιτοχονδριακή μεμβράνη είναι αδιαπέραστη σε μικρά ιόντα, όπως H + , K + , Na + , NH4 + , CI - , ΝΟ3 - , κλπ.
- Η μιτοχονδριακή μεμβράνη είναι διαπερατή σε μικρά μη φορτισμένα μόρια όπως σάκχαρα 02, CO2, Ν2, 3-C ή 4-C, κλπ.
- Αν και η μεμβράνη είναι αδιαπέραστη σε μικρά ιόντα (στοιχείο 2) και συνεπώς σε οξικό - και NH4 + , είναι διαπερατή στο οξικό οξύ και στα NH 3 , τα οποία είναι ουδέτερα μικρά μόρια (στοιχείο 3).
Ως συνέπεια αυτών των ιδιοτήτων διαπερατότητας, τα μιτοχονδριακά δεν θα διογκωθούν σε NH4CI ή σε οξικό Κ, επειδή η μεμβράνη είναι αδιαπέραστη από τα ιόντα. Εντούτοις, θα διογκωθούν αν εναιωρηθούν σε οξικό ΝΗ4, επειδή οι ουδέτερες μορφές μπορούν να διασχίσουν τη μεμβράνη.
Στην παρακάτω εικόνα, το μιτοχονδριακό πρήξιμο μετρήθηκε σε ένα απλό φωτόμετρο σκέδασης φωτός. Με την προσθήκη υποπολλαπλασίων μιτοχονδριακού εναιωρήματος σε αποσταγμένο νερό ή 100 mM των αλάτων που εμφανίζονται (ρΗ προσαρμοσμένο στο 7.0), μετά τη μείωση σε αρχικό επίπεδο λόγω απορρόφησης φωτός από τα προστιθέμενα μιτοχόνδρια, η μετάδοση αυξήθηκε καθώς τα μιτοχόνδρια διογκώθηκαν. Πολύ γρήγορα σε νερό, πολύ αργά σε KCl, οξικό Κ ή NH4Cl, ταχέως σε οξικό ΝΗ4:


Σε παρόμοια πειράματα, τα μιτοχόνδρια προστέθηκαν στα ΝΗ4 - σόλα διαφόρων μιτοχονδριακών υποστρωμάτων:

Τα μιτοχόνδρια διογκώθηκαν ταχέως σε ΝΗ4 - φωσφορικό, αλλά όχι στα άλλα NH4 - σαλτσάρια. Ωστόσο, με την προσθήκη καταλυτικών ποσοτήτων Κ-φωσφορικού άλατος στο πείραμα μηλικού ή ηλεκτρικού ή Κ-φωσφορικού και Κ-μηλεϊνικού άλατος προς το πείραμα κιτρικού, ισοκυτταρικού ή -κετογλουταρικού, παρατηρήθηκε ταχεία διόγκωση. Τα αποτελέσματα ερμηνεύθηκαν όπως φαίνεται στο παρακάτω σχήμα:

- Αριστερά: Η παρουσία ενός φορέα φωσφορικού άλατος επέτρεψε την ανταλλαγή Η2ΡΟ4 - για την ανταλλαγή ΟΗ - διαμέσου της μεμβράνης. Αυτό επέτρεψε αποτελεσματικά στο φωσφορικό να διασχίσει τη μεμβράνη σαν να ήταν ασθενές οξύ, οπότε η κατάσταση ήταν οξεία.
- Κέντρο: Ο μεταφορέας ανταλλαγής μηλικού 2- - HPO 4 2 επέτρεψε να εισέλθει μηλικό, αλλά μόνο αν υπήρχε καταλυτική ποσότητα εξωτερικού φωσφορικού άλατος για να επιτρέψει την ταχεία μετατροπή του μεταφορέα φωσφορικών. Ουσιαστικά, η δραστηριότητα των δύο φορέων επιτρέπει στο malate 2 να εισέλθει σε ανταλλαγή με 2ΟΗ - .
- Δεξιά: Ο μεταφορέας κιτρικού άλατος επέτρεψε να εισέλθει 2- (μία από τις τρεις καρβοξυλικές ομάδες πρωτονιωμένη) με κιτρικό άλας σε αντάλλαγμα για το μηλικό 2- , αλλά αυτό θα μπορούσε να συμβεί μόνο γρήγορα εάν υπήρχαν επαρκή εξωτερικά μηλικά και φωσφορικά για να επιτρέψουν την ταχεία αναστροφή Των μεταφορέων τους. Πράγματι, το κιτρικό οξύ εισέρχεται ως ουδέτερο είδος (ή σε αντάλλαγμα για 3OH - ).
Σε κάθε περίπτωση, οι φορείς επιτρέπουν στους μεταβολίτες να εισέλθουν ως ουδέτερα είδη. Οι ανταλλαγές ανιόντων για έναν ισοδύναμο αριθμό φορτίων ΟΗ, και αυτό επιτρέπει να εισέλθει ένας ισοδύναμος αριθμός μορίων ΝΗ3 και να πρωτονιωθεί σε ΝΗ4 + , επιτρέποντας την καθαρή είσοδο του ΝΗ4 - άλατος και διόγκωση των μιτοχονδρίων.
Οικογένεια, ακολουθίες, δομή
Η οικογένεια πρωτεϊνών που περιλαμβάνει τα πέντε μέλη που συζητήθηκαν παραπάνω (μεταφορέας φωσφορικών, μεταφορέας νουκλεοτιδίου αδενίνης, μεταφορέας τρικαρβοξυλικού, μεταφορέας μηλικού, μεταφορέας 2-οξογλουταρικού) έχει μελετηθεί εκτενώς τα τελευταία χρόνια. Υπάρχουν πολλές ακολουθίες διαθέσιμες, από τις οποίες ένα δείγμα μπορεί να βρεθεί σε αυτόν τον σύνδεσμο.
Η οικογένεια περιλαμβάνει επίσης μια ενδιαφέρουσα πρωτεΐνη η οποία είναι ενεργή στα μιτοχόνδρια από το δαγκωμένο λιπώδη ιστό. Τα μιτοχόνδρια "καφέ-λιπαρά" είναι αποσυνδεδεμένα - η έκφρασή τους θεωρείται ότι επιτρέπει την προθέρμανση των χειμερινωδών ζώων, με τη δημιουργία θερμότητας. Ο μηχανισμός παραγωγής θερμότητας περιλαμβάνει την ενεργοποίηση της πρωτεΐνης αποσύνδεσης, η οποία δρα ως φορέας πρωτονίων.
Η προγονική οικογένεια των μιτοχονδρίων μεταφορέων είναι ασαφής.
Δεν υπάρχει ακόμη τριτογενής δομή για πρωτεΐνη μεταφοράς. Η μιτοχονδριακή οικογένεια φαίνεται να έχει μια συντηρημένη δευτερογενή δομή, με τρία καλά καθορισμένα υδρόφοβα ανοίγματα τα οποία είναι πιθανόν τεμπεμβρανικές έλικες και ένα τέταρτο άνοιγμα με υδρόφοβο και αμφιπαθητικό χαρακτήρα, το οποίο μπορεί επίσης να είναι διαμεμβρανικό. Υπήρξε μεγάλη εικασία σχετικά με το ρόλο αυτού και άλλων αμφιπαθητικών διαστημάτων στον μηχανισμό μεταφοράς.
Ιοντοφόρα και μεταφορά κατιόντων από μιτοχόνδρια
Τα πρώτα στοιχεία για την χημειοσmoτική υπόθεση προέρχονταν από μελέτες μεταφοράς ιόντων από μιτοχόνδρια. Έχουν μελετηθεί τρεις τύποι μεταφορών:
-
Μεταφορά δισθενών κατιόντων
Όταν μια βαθμίδα πρωτονίων παράγεται από συζευγμένη μεταφορά ηλεκτρονίων ή από υδρόλυση ΑΤΡ, τα μιτοχονδριακά δεσμεύουν το Ca2 + από το εξωτερικό μέσο. Η πρόσληψη Ca2 + καταλύεται από έναν φορέα Ca2 + στην εσωτερική μεμβράνη που ανταλλάσσει Ca2 + για Η + (καθαρή ηλεκτρογενετικότητα, 1 + φορτίο). Όταν υπάρχει επίσης φωσφορικό άλας, λαμβάνει χώρα καθαρή πρόσληψη φωσφορικού ασβεστίου, η οποία κατακρημνίζεται μέσα στα μιτοχόνδρια ως υδροξυαπατίτη, ορατή ως πυκνές κόκκοι σε ηλεκτρονικές μικρογραφίες. Εάν υπάρχει ασθενώς όξινο όξινο οξικό ανιόν στο μέσο εναιώρησης, συσσωρεύεται οξικό ασβέστιο και τα μιτοχόνδρια διογκώνονται οσμωτικά λόγω του αυξημένου διαλυτού άλατος στο εσωτερικό του.Η μεταφορά του Ca2 + παίζει έναν φυσιολογικό ρόλο σε αυτές τις κυτταρικές διεργασίες οι οποίες ενεργοποιούνται ή αναστέλλονται από μεταβολές στην δραστηριότητα Ca2 + στο κυτταρόπλασμα. Η μιτοχονδριακή μεταφορά έχει Km στο φυσιολογικό εύρος, έτσι η πρόσληψη ρυθμίζει το εσωτερικό [Ca2 + ].
Το μιτοχόνδριο θα μεταφέρει το Mn 2+ ή το Sr 2+ αντί του ασβεστίου. -
Μεταφορά ιόντων καταλυόμενη από ιονοφόρα
Ο χαρακτηρισμός των μηχανισμών των ιονοφόρων διαδραμάτισε καθοριστικό ρόλο στην κατανόηση της βαθμίδας πρωτονίων και του ρόλου της στη χημειοσωμική σύζευξη. Τέσσερις ιονοφόροι μηχανισμοί αποδείχθηκαν ιδιαίτερα χρήσιμοι:-
Βαλινομυκίνη
Η βαλινομυκίνη καταλύει το φορτίο του K + (και άλλων μονοσθενών κατιόντων παρόμοιων ακτίνων όπως Rb + ή Cs + , αλλά όχι Na + ) ως φορτισμένο είδος σε βιολογικές μεμβράνες (ή σε υδρόφοβες φάσεις γενικά). Η μεταφορά γίνεται με μηχανισμό μεταφοράς. Κατά συνέπεια, το ηλεκτροχημικό δυναμικό για τα μεταφερόμενα είδη είναι ίσο σε ολόκληρη τη μεμβράνη και ισχύει η κατάσταση ισορροπίας.
Η κατανομή ιόντων (συνήθως ισοτοπικά επισημασμένη Rb + χρησιμοποιείται) μεταξύ εσωτερικής και εξωτερικής φάσης παρουσία βαλινομυκίνης υπήρξε μια αγαπημένη μέθοδος για τη μέτρηση του δυναμικού της μεμβράνης .
Ως αποτέλεσμα αυτού του μηχανισμού, τα μιτοχόνδρια θα αναλάβουν K + σε βάρος της βαθμίδας πρωτονίων που οδηγείται από συζευγμένη μεταφορά ηλεκτρονίων ή υδρόλυση ΑΤΡ.
Υπό την παρουσία περίσσειας Κ + , το ηλεκτρικό συστατικό ( Dy ) της βαθμίδας πρωτονίων καταρρέει, τουλάχιστον κατά τη διάρκεια του χρόνου που απαιτείται για τη συσσώρευση μιας ουσιαστικής κλίσης Κ + . -
Nigericin
Η νιγερικίνη καταλύει την ουδέτερη ανταλλαγή μονοσθενών κατιόντων σε βιολογικές μεμβράνες, με ευρεία ειδικότητα. Εάν ένα κατιόν υπερισχύει, το κατιόν ανταλλάσσεται με Η + . Κατά συνέπεια, όταν η νιγηρίνη προστίθεται στα μιτοχόνδρια παρουσία περίσσειας Κ + , το συνιστώσα -Ζ D της βαθμίδας πρωτονίων καταρρέει. Ο μηχανισμός της νιγηρίνης συζητείται λεπτομερέστερα εδώ. -
Gramicidin
Η γραμιμιδίνη καταλύει μια ηλεκτρογενή ροή μικρών μονοσθενών κατιόντων, συμπεριλαμβανομένων των πρωτονίων, διαμέσου βιολογικών μεμβρανών μέσω ενός πόρου σχηματιζόμενου από δύο μόρια από άκρο σε άκρο που καλύπτει τη μεμβράνη. Ο πόρος γραμιμιδίνης μελετάται πολύ και συζητείται λεπτομερέστερα στο πλαίσιο της αγωγιμότητας πρωτονίων.
Ως συνέπεια του μηχανισμού, η γραμιμιδίνη δρα ως παράγοντας αποσύνδεσης. Με την παρουσία περίσσειας μονοσθενούς κατιόντος (όπως το Κ + ), η μεταφορά του Κ + ευνοείται έναντι της διαρροής ή της Η + και η γραμιμιδίνη θα καταλύει την πρόσληψη Κ + από τα μιτοχόνδρια, παρόμοια με αυτή που παρατηρείται με τη βαλινομυκίνη. -
Πρωτονόφαρα
Ο Μίτσελ πρότεινε ότι οι αποσυνδέτες θα ενεργούν βραχυκυκλώνοντας την κλίση των πρωτονίων, - ενεργώντας ως αγωγοί πρωτονίων. Αυτή η πρωτονωφορική δραστηριότητα έχει διερευνηθεί σε μεγάλο βαθμό και η απόδειξη μιας ισχυρής συσχέτισης μεταξύ της πρωτονωφορικής δραστηριότητας σε τεχνητά συστήματα μεμβράνης και της δραστηριότητας αποσύνδεσης ήταν ένα ισχυρό τεκμήριο που ευνοούσε την χημειοσμοτική υπόθεση. Ο προτεινόμενος μηχανισμός Mitchell απεικονίζεται εδώ για την κλασσική αποσυνδεδεμένη 2,4-δινιτροφαινόλη.

-
Μεταβολική επικοινωνία μεταξύ του κυτταροπλάσματος και της μιτοχονδριακής μήτρας
Η ενσωμάτωση του ευβακτηριακού μεταβολισμού του μιτοχονδρίου και ο μεταβολισμός του κυττάρου-ξενιστή έχει οδηγήσει σε κατανομή πολλών μεταβολικών οδών και σε κυκλοφορία μεταβολιτών σε όλη την μιτοχονδριακή μεμβράνη, καταλυόμενη από τα συστήματα μεταφοράς μεταβολιτών. Μερικά παραδείγματα δίνονται παρακάτω:
Γλυκονογένεση
Το γαλακτικό προϊόν επιστρέφει στο ήπαρ από την παραγωγή στον μυ στις συνθήκες υψηλής ζήτησης, ανακυκλώνεται πίσω στη γλυκόζη , χρησιμοποιώντας την ενέργεια από την οξείδωση ενός κλάσματος του γαλακτικού. Η οδός ονομάζεται γλυκονεογένεση και το κύτταρο χρησιμοποιεί πολλά από τα ένζυμα της γλυκόλυσης που λειτουργούν στην αντίθετη κατεύθυνση. Για να κινηθεί η αντίδραση με αντίστροφο τρόπο, το κύτταρο αυξάνει τη συγκέντρωση του υποστρώματος εισόδου, πυροσταφυλική φωσφοενόλη (PEP) και παρακάμπτει τις αντιδράσεις κινάσης με τις οποίες «ενεργοποιείται» η γλυκόζη (οι οποίες έχουν υψηλό Δ.Ο. Κατεύθυνση της γλυκόλυσης) χρησιμοποιώντας φωσφατάσες. Προκειμένου να ξεπεραστεί η σχετικά υψηλός -DG o 'της αντίδρασης της πυροσταφυλικής κινάσης, το κύτταρο χρησιμοποιεί ένζυμα στη μιτοχονδριακή μήτρα για να επιτρέψει την παραγωγή της PEP μέσω καρβοξυλίωσης του πυροσταφυλικού οξέος προς το οξαλοξεικό (ΟΑΑ), τη μετατροπή προς το μηλικό, την εξαγωγή στο κυτταρόπλασμα , Μετατροπή πίσω στο ΟΑΑ και αποκαρβοξυλίωση με φωσφορυλίωση για την παραγωγή ΡΕΡ. Αυτή η σειρά αντιδράσεων επιτρέπει την χρήση της ελεύθερης ενέργειας από την υδρόλυση δύο μορίων ΑΤΡ για να μετατραπεί το πυροσταφυλικό σε PEP.

phosphorylation |
|
|
(8) |
oxidation |
|
|
(9) |
reduction |
|
|
(10) |
The net reaction is obtained by summing the coupled reactions, as shown in Equation 11, below.
|
|
(spontaneous) |
(11) |
The molecular changes that occur upon oxidation of NADH are shown in Figure 5, below.
 |
Figure 5This is a two-dimensional (ChemDraw) representation showing the change that occurs when NADH is oxidized to NAD+. "R" represents the part of the structure that is shown in black in the drawing of NADH in Table 1, and does not change during the oxidation half-reaction. The molecular changes that occur upon oxidation are shown in red. |
In this tutorial, we have seen that nonspontaneous reactions in the body occur by coupling them with a very spontaneous reaction (usually the ATP reaction shown in Equation 3). We have just seen that ATP is produced by coupling the phosphorylation reaction with NADH oxidation (a very spontaneous reaction). But we have not yet answered the question: by what mechanism are these reactions coupled?
 Coupling Reactions in Biological Systems
Coupling Reactions in Biological Systems
Every day your body carries out many nonspontaneous reactions. As discussed earlier, if a nonspontaneous reaction is coupled to a spontaneous reaction, as long as the sum of the free energies for the two reactions is negative, the coupled reactions will occur spontaneously. How is this coupling achieved in the body? Living systems couple reactions in several ways, but the most common method of coupling reactions is to carry out both reactions on the same enzyme. Consider again the phosphorylation of glycerol (Equations 2-4). Glycerol is phosphorylated by the enzyme glycerol kinase, which is found in your liver. The product of glycerol phosporylation, glycerol-3-phosphate (Equation 2), is used in the synthesis of phospholipids.
Glycerol kinase is a large protein comprised of about 500 amino acids. X-ray crystallography of the protein shows us that there is a deep groove or cleft in the protein where glycerol and ATP attach (see Figure 6, below). Because the enzyme holds the ATP and the glycerol in place, the phosphate can be transferred directly from the ATP to glycerol. Instead of two separate reactions where ATP loses a phosphate (Equation 3) and glycerol picks up a phosphate (Equation 2), the enzyme allows the phosphate to move directly from ATP to glycerol (Equation 4).
The coupling in oxidative phosphorylation uses a more complicated (and amazing!) mechanism, but the end result is the same: the reactions are linked together, the net free energy for the linked reactions is negative, and, therefore, the linked reactions are spontaneous.
 |
| Figure 6
This is a schematic representation of ATP and glycerol bound (attached) to glycerol kinase. The enzyme glycerol kinase is a dimer (consists of two identical subuits). There is a deep cleft between the subunits where ATP and glycerol bind. Since the ATP and phosphate are physically so close together when they are bound to the enzyme, the phosphate can be transferred directly from ATP to glycerol. Hence, the processes of ATP losing a phosphate (spontaneous) and glycerol gaining a phosphate (nonspontaneous) are linked together as one spontaneous process. |
-
Μεταφορά ιόντων καταλυόμενη από ιονοφόρα
Ο χαρακτηρισμός των μηχανισμών των ιονοφόρων διαδραμάτισε καθοριστικό ρόλο στην κατανόηση της βαθμίδας πρωτονίων και του ρόλου της στη χημειοσωμική σύζευξη. Τέσσερις ιονοφόροι μηχανισμοί αποδείχθηκαν ιδιαίτερα χρήσιμοι:-
Βαλινομυκίνη
Η βαλινομυκίνη καταλύει το φορτίο του K + (και άλλων μονοσθενών κατιόντων παρόμοιων ακτίνων όπως Rb + ή Cs + , αλλά όχι Na + ) ως φορτισμένο είδος σε βιολογικές μεμβράνες (ή σε υδρόφοβες φάσεις γενικά). Η μεταφορά γίνεται με μηχανισμό μεταφοράς. Κατά συνέπεια, το ηλεκτροχημικό δυναμικό για τα μεταφερόμενα είδη είναι ίσο σε ολόκληρη τη μεμβράνη και ισχύει η κατάσταση ισορροπίας.
Η κατανομή ιόντων (συνήθως ισοτοπικά επισημασμένη Rb + χρησιμοποιείται) μεταξύ εσωτερικής και εξωτερικής φάσης παρουσία βαλινομυκίνης υπήρξε μια αγαπημένη μέθοδος για τη μέτρηση του δυναμικού της μεμβράνης .
Ως αποτέλεσμα αυτού του μηχανισμού, τα μιτοχόνδρια θα αναλάβουν K + σε βάρος της βαθμίδας πρωτονίων που οδηγείται από συζευγμένη μεταφορά ηλεκτρονίων ή υδρόλυση ΑΤΡ.
Υπό την παρουσία περίσσειας Κ + , το ηλεκτρικό συστατικό ( Dy ) της βαθμίδας πρωτονίων καταρρέει, τουλάχιστον κατά τη διάρκεια του χρόνου που απαιτείται για τη συσσώρευση μιας ουσιαστικής κλίσης Κ + . -
Nigericin
Η νιγερικίνη καταλύει την ουδέτερη ανταλλαγή μονοσθενών κατιόντων σε βιολογικές μεμβράνες, με ευρεία ειδικότητα. Εάν ένα κατιόν υπερισχύει, το κατιόν ανταλλάσσεται με Η + . Κατά συνέπεια, όταν η νιγηρίνη προστίθεται στα μιτοχόνδρια παρουσία περίσσειας Κ + , το συνιστώσα -Ζ D της βαθμίδας πρωτονίων καταρρέει. Ο μηχανισμός της νιγηρίνης συζητείται λεπτομερέστερα εδώ. -
Gramicidin
Η γραμιμιδίνη καταλύει μια ηλεκτρογενή ροή μικρών μονοσθενών κατιόντων, συμπεριλαμβανομένων των πρωτονίων, διαμέσου βιολογικών μεμβρανών μέσω ενός πόρου σχηματιζόμενου από δύο μόρια από άκρο σε άκρο που καλύπτει τη μεμβράνη. Ο πόρος γραμιμιδίνης μελετάται πολύ και συζητείται λεπτομερέστερα στο πλαίσιο της αγωγιμότητας πρωτονίων.
Ως συνέπεια του μηχανισμού, η γραμιμιδίνη δρα ως παράγοντας αποσύνδεσης. Με την παρουσία περίσσειας μονοσθενούς κατιόντος (όπως το Κ + ), η μεταφορά του Κ + ευνοείται έναντι της διαρροής ή της Η + και η γραμιμιδίνη θα καταλύει την πρόσληψη Κ + από τα μιτοχόνδρια, παρόμοια με αυτή που παρατηρείται με τη βαλινομυκίνη. -
Πρωτονόφαρα
Ο Μίτσελ πρότεινε ότι οι αποσυνδέτες θα ενεργούν βραχυκυκλώνοντας την κλίση των πρωτονίων, - ενεργώντας ως αγωγοί πρωτονίων. Αυτή η πρωτονωφορική δραστηριότητα έχει διερευνηθεί σε μεγάλο βαθμό και η απόδειξη μιας ισχυρής συσχέτισης μεταξύ της πρωτονωφορικής δραστηριότητας σε τεχνητά συστήματα μεμβράνης και της δραστηριότητας αποσύνδεσης ήταν ένα ισχυρό τεκμήριο που ευνοούσε την χημειοσμοτική υπόθεση. Ο προτεινόμενος μηχανισμός Mitchell απεικονίζεται εδώ για την κλασσική αποσυνδεδεμένη 2,4-δινιτροφαινόλη.

-
Μεταβολική επικοινωνία μεταξύ του κυτταροπλάσματος και της μιτοχονδριακής μήτρας
Η ενσωμάτωση του ευβακτηριακού μεταβολισμού του μιτοχονδρίου και ο μεταβολισμός του κυττάρου-ξενιστή έχει οδηγήσει σε κατανομή πολλών μεταβολικών οδών και σε κυκλοφορία μεταβολιτών σε όλη την μιτοχονδριακή μεμβράνη, καταλυόμενη από τα συστήματα μεταφοράς μεταβολιτών. Μερικά παραδείγματα δίνονται παρακάτω:
Γλυκονογένεση
Το γαλακτικό προϊόν επιστρέφει στο ήπαρ από την παραγωγή στον μυ στις συνθήκες υψηλής ζήτησης, ανακυκλώνεται πίσω στη γλυκόζη , χρησιμοποιώντας την ενέργεια από την οξείδωση ενός κλάσματος του γαλακτικού. Η οδός ονομάζεται γλυκονεογένεση και το κύτταρο χρησιμοποιεί πολλά από τα ένζυμα της γλυκόλυσης που λειτουργούν στην αντίθετη κατεύθυνση. Για να κινηθεί η αντίδραση με αντίστροφο τρόπο, το κύτταρο αυξάνει τη συγκέντρωση του υποστρώματος εισόδου, πυροσταφυλική φωσφοενόλη (PEP) και παρακάμπτει τις αντιδράσεις κινάσης με τις οποίες «ενεργοποιείται» η γλυκόζη (οι οποίες έχουν υψηλό Δ.Ο. Κατεύθυνση της γλυκόλυσης) χρησιμοποιώντας φωσφατάσες. Προκειμένου να ξεπεραστεί η σχετικά υψηλός -DG o 'της αντίδρασης της πυροσταφυλικής κινάσης, το κύτταρο χρησιμοποιεί ένζυμα στη μιτοχονδριακή μήτρα για να επιτρέψει την παραγωγή της PEP μέσω καρβοξυλίωσης του πυροσταφυλικού οξέος προς το οξαλοξεικό (ΟΑΑ), τη μετατροπή προς το μηλικό, την εξαγωγή στο κυτταρόπλασμα , Μετατροπή πίσω στο ΟΑΑ και αποκαρβοξυλίωση με φωσφορυλίωση για την παραγωγή ΡΕΡ. Αυτή η σειρά αντιδράσεων επιτρέπει την χρήση της ελεύθερης ενέργειας από την υδρόλυση δύο μορίων ΑΤΡ για να μετατραπεί το πυροσταφυλικό σε PEP.

Εισαγωγή αναγωγικών ισοδυνάμων από κυτταροπλασματικό NADH
Η μιτοχονδριακή μεμβράνη είναι αδιαπέραστη από δινουκλεοτίδια αδενίνης νικοτιναμιδίου (NAD + , NADH, NADP + , NADPH). Παρ 'όλα αυτά, το NADH που παράγεται στο κυτταρόπλασμα με γλυκόλυση οξειδώνεται από την αλυσίδα της αποκατάστασης. Αυτό επιτυγχάνεται με δύο κύριες οδούς, το λεωφορείο γλουταμινικού / ασπαρτικού και το φορείο της φωσφορικής διυδροξυακετόνης (DHAP), που χρησιμοποιούνται κυρίως στο ήπαρ και στους μύες αντίστοιχα.
- Το λεωφορείο γλουταμινικού / ασπαρτικού
Αυτή η οδός χρησιμοποιεί τα συστήματα μεταφοράς μιτοχονδρίων μεταβολίτη όπως φαίνεται παρακάτω:

- Το λεωφορείο DHAP
Αυτή η οδός δεν περιλαμβάνει μεταφορά μεταβολίτη. Αντίθετα, εξαρτάται από τη δραστικότητα δύο διαφορετικών ενζύμων γλυκερόλης-3-φωσφορικής αφυδρογονάσης, το ένα χρησιμοποιώντας ζεύγος NAD / NADH και το άλλο, ένα δεσμευμένο με FAD ένζυμο συνδεδεμένο με μεμβράνη, το οποίο μειώνει την συγκέντρωση ουβικινόνης. Η οδός για την οξείδωση του κυτταροπλασμικού NADH φαίνεται παρακάτω:
Εξαγωγή θραυσμάτων 2-C για τη σύνθεση λιπαρών οξέων
Το Acetyl-CoA είναι το υπόστρωμα για τη σύνθεση λιπαρών οξέων, αλλά η παραγωγή ακετυλο-ΟοΑ εμφανίζεται κυρίως στη μήτρα μιτοχονδρίων. Τρεις κύριες πηγές ακετυλ-ΟοΑ είναι:- Πυρουβική αφυδρογονάση
- Η κατανομή των λιπαρών οξέων
- Καταβολισμός κετογόνων αμινοξέων

ΑΤΡ-εξαρτώμενη μεταφορά ιόντων
Δύο κύριες οικογένειες,Εξισώσεις για μεταφορικές, χημικές και ηλεκτροχημικές δυναμικές κλίσεις
Επιστρέψτε στη Διάλεξη 9 για την αναθεώρηση των εξισώσεων μεταφοράς.-
Μεταφορά ιόντων καταλυόμενη από ιονοφόρα
Ο χαρακτηρισμός των μηχανισμών των ιονοφόρων διαδραμάτισε καθοριστικό ρόλο στην κατανόηση της βαθμίδας πρωτονίων και του ρόλου της στη χημειοσωμική σύζευξη. Τέσσερις ιονοφόροι μηχανισμοί αποδείχθηκαν ιδιαίτερα χρήσιμοι:-
Βαλινομυκίνη
Η βαλινομυκίνη καταλύει το φορτίο του K + (και άλλων μονοσθενών κατιόντων παρόμοιων ακτίνων όπως Rb + ή Cs + , αλλά όχι Na + ) ως φορτισμένο είδος σε βιολογικές μεμβράνες (ή σε υδρόφοβες φάσεις γενικά). Η μεταφορά γίνεται με μηχανισμό μεταφοράς. Κατά συνέπεια, το ηλεκτροχημικό δυναμικό για τα μεταφερόμενα είδη είναι ίσο σε ολόκληρη τη μεμβράνη και ισχύει η κατάσταση ισορροπίας.
Η κατανομή ιόντων (συνήθως ισοτοπικά επισημασμένη Rb + χρησιμοποιείται) μεταξύ εσωτερικής και εξωτερικής φάσης παρουσία βαλινομυκίνης υπήρξε μια αγαπημένη μέθοδος για τη μέτρηση του δυναμικού της μεμβράνης .
Ως αποτέλεσμα αυτού του μηχανισμού, τα μιτοχόνδρια θα αναλάβουν K + σε βάρος της βαθμίδας πρωτονίων που οδηγείται από συζευγμένη μεταφορά ηλεκτρονίων ή υδρόλυση ΑΤΡ.
Υπό την παρουσία περίσσειας Κ + , το ηλεκτρικό συστατικό ( Dy ) της βαθμίδας πρωτονίων καταρρέει, τουλάχιστον κατά τη διάρκεια του χρόνου που απαιτείται για τη συσσώρευση μιας ουσιαστικής κλίσης Κ + . -
Nigericin
Η νιγερικίνη καταλύει την ουδέτερη ανταλλαγή μονοσθενών κατιόντων σε βιολογικές μεμβράνες, με ευρεία ειδικότητα. Εάν ένα κατιόν υπερισχύει, το κατιόν ανταλλάσσεται με Η + . Κατά συνέπεια, όταν η νιγηρίνη προστίθεται στα μιτοχόνδρια παρουσία περίσσειας Κ + , το συνιστώσα -Ζ D της βαθμίδας πρωτονίων καταρρέει. Ο μηχανισμός της νιγηρίνης συζητείται λεπτομερέστερα εδώ. -
Gramicidin
Η γραμιμιδίνη καταλύει μια ηλεκτρογενή ροή μικρών μονοσθενών κατιόντων, συμπεριλαμβανομένων των πρωτονίων, διαμέσου βιολογικών μεμβρανών μέσω ενός πόρου σχηματιζόμενου από δύο μόρια από άκρο σε άκρο που καλύπτει τη μεμβράνη. Ο πόρος γραμιμιδίνης μελετάται πολύ και συζητείται λεπτομερέστερα στο πλαίσιο της αγωγιμότητας πρωτονίων.
Ως συνέπεια του μηχανισμού, η γραμιμιδίνη δρα ως παράγοντας αποσύνδεσης. Με την παρουσία περίσσειας μονοσθενούς κατιόντος (όπως το Κ + ), η μεταφορά του Κ + ευνοείται έναντι της διαρροής ή της Η + και η γραμιμιδίνη θα καταλύει την πρόσληψη Κ + από τα μιτοχόνδρια, παρόμοια με αυτή που παρατηρείται με τη βαλινομυκίνη. -
Πρωτονόφαρα
Ο Μίτσελ πρότεινε ότι οι αποσυνδέτες θα ενεργούν βραχυκυκλώνοντας την κλίση των πρωτονίων, - ενεργώντας ως αγωγοί πρωτονίων. Αυτή η πρωτονωφορική δραστηριότητα έχει διερευνηθεί σε μεγάλο βαθμό και η απόδειξη μιας ισχυρής συσχέτισης μεταξύ της πρωτονωφορικής δραστηριότητας σε τεχνητά συστήματα μεμβράνης και της δραστηριότητας αποσύνδεσης ήταν ένα ισχυρό τεκμήριο που ευνοούσε την χημειοσμοτική υπόθεση. Ο προτεινόμενος μηχανισμός Mitchell απεικονίζεται εδώ για την κλασσική αποσυνδεδεμένη 2,4-δινιτροφαινόλη.

-
Μεταβολική επικοινωνία μεταξύ του κυτταροπλάσματος και της μιτοχονδριακής μήτρας
Η ενσωμάτωση του ευβακτηριακού μεταβολισμού του μιτοχονδρίου και ο μεταβολισμός του κυττάρου-ξενιστή έχει οδηγήσει σε κατανομή πολλών μεταβολικών οδών και σε κυκλοφορία μεταβολιτών σε όλη την μιτοχονδριακή μεμβράνη, καταλυόμενη από τα συστήματα μεταφοράς μεταβολιτών. Μερικά παραδείγματα δίνονται παρακάτω:Γλυκονογένεση
Το γαλακτικό προϊόν επιστρέφει στο ήπαρ από την παραγωγή στον μυ στις συνθήκες υψηλής ζήτησης, ανακυκλώνεται πίσω στη γλυκόζη , χρησιμοποιώντας την ενέργεια από την οξείδωση ενός κλάσματος του γαλακτικού. Η οδός ονομάζεται γλυκονεογένεση και το κύτταρο χρησιμοποιεί πολλά από τα ένζυμα της γλυκόλυσης που λειτουργούν στην αντίθετη κατεύθυνση. Για να κινηθεί η αντίδραση με αντίστροφο τρόπο, το κύτταρο αυξάνει τη συγκέντρωση του υποστρώματος εισόδου, πυροσταφυλική φωσφοενόλη (PEP) και παρακάμπτει τις αντιδράσεις κινάσης με τις οποίες «ενεργοποιείται» η γλυκόζη (οι οποίες έχουν υψηλό Δ.Ο. Κατεύθυνση της γλυκόλυσης) χρησιμοποιώντας φωσφατάσες. Προκειμένου να ξεπεραστεί η σχετικά υψηλός -DG o 'της αντίδρασης της πυροσταφυλικής κινάσης, το κύτταρο χρησιμοποιεί ένζυμα στη μιτοχονδριακή μήτρα για να επιτρέψει την παραγωγή της PEP μέσω καρβοξυλίωσης του πυροσταφυλικού οξέος προς το οξαλοξεικό (ΟΑΑ), τη μετατροπή προς το μηλικό, την εξαγωγή στο κυτταρόπλασμα , Μετατροπή πίσω στο ΟΑΑ και αποκαρβοξυλίωση με φωσφορυλίωση για την παραγωγή ΡΕΡ. Αυτή η σειρά αντιδράσεων επιτρέπει την χρήση της ελεύθερης ενέργειας από την υδρόλυση δύο μορίων ΑΤΡ για να μετατραπεί το πυροσταφυλικό σε PEP.


