Δήμητρα Σπανού, Χημικός, συνταξιούχος καθηγήτρια Β/θμιας Εκπαίδευσης
ΕΙΣΑΓΩΓΗ
Ο ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ
Δύο ή περισσότερα άτομα αλληλεπιδρούν και σχηματίζουν ένα σταθερότερο σύστημα από 2 ή περισσότερα άτομα. Βασίζεται σε θεωρίες ηλεκρονιακών αλληλεπιδράσεων στις οποίες συμμετέχουν κυρίως τα ηλεκτρόνια του τελευταίου ή του προτελευταίου ηλεκτρονιακού ενεργειακού επιπέδου. Τα ημιτελή στρώματα ηλεκτρονίων των εξωτερικών στοιβάδων των ατόμων είναι ασταθή και τέτοια άτομα προσπαθούν να συνδυαστούν με άλλα άτομα με στόχο την αναδιάρθωση των ηλεκτρονίων αυτών.
Ο χημικός δεσμός συνοδεύεται από μεταβολή της συνολικής ενέργειας του συστήματος και υπάρδιαφορετικοί τρόποι που πραγματοποιείται και εξηγείται έχοντας υπ' όψη με την ενέργεια ιοντισμού των χημικών στοιχείων, την ηλεκτραρνητικότητα, την ηλεκτροσυγγένεια
Πληρέστερες ερμηνείες για την δημιουργια των χημικών ενώσεων από τα χημικά στοιχεία και για τους χημικούς δεσμούς έχουν διατυπωθεί:
ΜΕ ΒΑΣΗ ΤΗΝ
Α. ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΣΤΑΘΕΡΟΤΗΤΑ ΓΙΑ ΤΗΝ (ΜΕΓΑΛΥΤΕΡΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΣΤΑΘΕΡΟΤΗΤΑ)
Οι τυχόν μεταβολές των συστημάτων που συνοδεύουν, όταν προχωρούν σε σχηματισμό νέων ουσιών όπως είναι οι χημικές ενώσεις, με κριτήριο την συμφερότερη μεταβολή της εσωτερικής τους ενέργειας και της ενθαλπίας τους (θερμοδυναμική σταθερότητα)
Β. ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΚΗ ΘΕΩΡΙΑ (ΓΙΑ ΗΛΕΚΤΡΟΝΙΑΚΗ ΙΣΟΡΡΟΠΙΑ ΤΩΝ ΕΞΩΤΕΡΙΚΩΝ ΗΛΕΚΤΡΟΝΙΩΝ)
Η τάση των χημικών στοιχείων να αποκτούν σταθερότερη ηλεκτρονιακή τοποθέτηση στην κατανομή των ηλεκτρονίων της εξωτερικής τους στοιβάδας (ηλεκτρονιακή ισορροπία)
Γ. ΚΒΑΝΤΙΚΗ ΘΕΩΡΙΑ (ΓΙΑ ΤΗΝ ΚΑΛΥΤΕΡΗ ΚΑΤΑΝΟΜΗ ΤΟΥ ΗΛΕΚΤΡΟΝΙΑΚΟΥ ΦΟΡΤΙΟΥ ΣΤΟΝ ΧΩΡΟ)
Ο συνδυασμος ατομικών τροχιακών για την δημιουργία μοριακών τροχιακών για την νέα κατανομή του ηλεκτρονιακού φορτίου στον χώρο βάσει της προσσέγγισης νέων φορτισμένων σωματιδίων στον χώρο
Ας θυμώμαστε πάντα πως, κατά τον σχηματισμό και διατήρηση των χημικών ενώσεων ισχύουν αρχές και νόμοι κάποιοι εκ των οποίων είναι οι Μεγάλοι Γενικοί Νόμοι της Φυσικής και της Φύσης, όπως για παράδειγμα οι νόμοι της θερμοδυναμικής, ο νόμος του ισοζυγίου, της διατήρησης και της μεταφοράς εφαρμοσμένοι στις χημικές διαδικασίες.
Εδώ όμως δεν επεκτεινόμαστε τόσο και περιοριζόμαστε να επεξηγούμε την δημιουργία χημικών ενώσεων
Σε Μέταλλα ευκολότερη η απομάκρυνση
Na (g) - e-→ Na+ (g) με ΔΗ = 496 Kcal/mole,
ενώ σε άλλα δυσκολότερη (αμέταλλα)
F (g) - e-→ F+ (g) με ΔΗ = 1680 Kcal/mole,
στα ευγενή αέρια είναι ακόμα πιο δύσκολο
Ne (g) - e-→ Ne+ (g) με ΔΗ = 2080 Kcal/mole,
- ΜΕΤΑΤΡΟΠΗ ΑΤΟΜΩΝ ΣΕ ΚΑΤΙΟΝΤΑ
- Η μετατροπή ατόμων σε ιόντα και η δημιουργία ιοντικού δεσμού εξαρτάται
- Από το μέγεθος της Ενέργειας Ιοντισμού ( I E) που είναι η Ελεύθερη Ενθαλπία Ιονισμού που περιγράφει την ενέργεια που απαιτείται για την απομάκρυνση ενός ηλεκτρονίου από ένα ουδέτερο άτομο ή μερικώς ιονισμένο. Για ηλεκτρόνια δίνεται σε eV/ άτομο A + I E → A + + e - .
- Σημείωση: Άτομα με ένα ηλεκτρόνιο στο κελύφους σθένους και συμπληρωμένες τις εσωτερικές στοιβάδες, είναι τα περισσότερο δραστικά, επειδή έχουν μικρή ενέργεια πρώτου ιοντισμού, έτσι, μπορούν σχετικά εύκολα να απομακρύνουν το μοναδικό ηλεκτρόνιο της εξωτερικής τους στοιβάδας και να μείνουν με τις εσωτερικές που είναι συμπληρωμένες που σημαίνει ότι μετατρέπονται σε θετικά ιόντα
-
Αλλά εκφράζεται και σε kj/mol και είναι αντίθετη σε πρόσημο με την ενέργεια ιονισμού
Cl (a) + e-→ Cl– (a) +83,2 kcal/mol με ΔΗ = –83,32 Kcal/mole,
-
Ο (a) + e- → Ο– (a) + 53,8 kcal/mol με ΔΗ = –53,8 Kcal/mole
Γενικά υπάρχει σχέση μεταξύ της ενέργειας ιονισμού και της ηλεκτροσυγγένειας. Όσο η ενέργεια ιονισμού αυξάνεται (και η δυσκολία να απομακρυνθεί ηλεκτρόνιο) συνήθως αυξάνεται και η ηλεκτροσυγγένεια (ικανότητα να δεσμεύει ηλεκτρ;oνεια το άτομο)
Αυτό όμως δεν είναι απόλυτο γιατί υπάρχουν διαφορές στους παράγοντες που επιρρεάζουν την ενέργεια ιοντισμού και την ηλεκτροσυγγένεια
Στον πίνακα που ακολουθεί βλέπουμε τις τιμές της ηλεκτροσυγγένειας ε σε eV / atomo. Έχουμε και θετικές τιμές αλλά και αρνητικές τιμές που σημαίνει ότι η αντίδραση πρόσληψης ηλεκτρονίου από το άτομο είναι ενδοενεργειακή ή εξωενεργειακή δηλαδή το αρνητικό ιόν είναι σταθερότερο του ατόμου (Cl, O, Br, Si...) και αντίστροφα το αρνητικό ιόν είναι ασταθέστερο του ατόμου (Ηe, N, Mg, Ca, Cr,...)
Ενέργεια συγγένειας ορισμένων ατόμων για ηλεκτρόνιο, eV
| Элемент | ε | Элемент | ε | Элемент | ε |
|---|---|---|---|---|---|
| H | 0,7542 | Na | 0,548 | K | 0,502 |
| He | -0,54 | Mg | -0,4 | Ca | -0,3 |
| Li | 0,618 | Al | 0,441 | Sc | 0,14 |
| Be | -0,5 | Si | 1,385 | Ti | -0,40 |
| B | 0,277 | P | 0,747 | V | -0,94 |
| C | 1,263 | S | 2,077 | Cr | -0,98 |
| N | -0,07 | Cl | 3,617 | Mn | 1,07 |
| О | 1,461 | Br | 3,365 | Fe | -0,58 |
| F | 3,399 | I | 3,06 | Co | -0,94 |
| Ne | -1,2(2) | Ni | -1,28 | ||
| Cu | -1,80 |
Οι τιμές της ηλεκτραρνητικότητας εξάγονται, λαμβάνοντας υπ όψην την ενέργεια ιοντισμού των ατόμων, την συγγένειά τους με το ηλεκτρόνιο, την μέση τιμή της ενέργειας δέσμευσης των εξωτερικών ηλεκτρονίων κ.α.
Υπάρχουν και άλλες κλίμακες ηλεκτραρνητικότητας που χρησιμοποιούν την μονάδα ενέργειας (eV) για την ηλεκτραρνητικότητα
ΣΥΝΔΕΣΗ ΑΤΟΜΩΝ ΠΡΟΣ ΔΗΜΙΟΥΡΓΙΑ ΧΗΜΙΚΩΝ ΕΝΩΣΕΩΝ ΜΕ ΒΑΣΗ ΤΗΝ ΗΛΕΚΤΡΑΡΝΗΤΙΚΟΤΗΤΑ ΤΟΥΣ
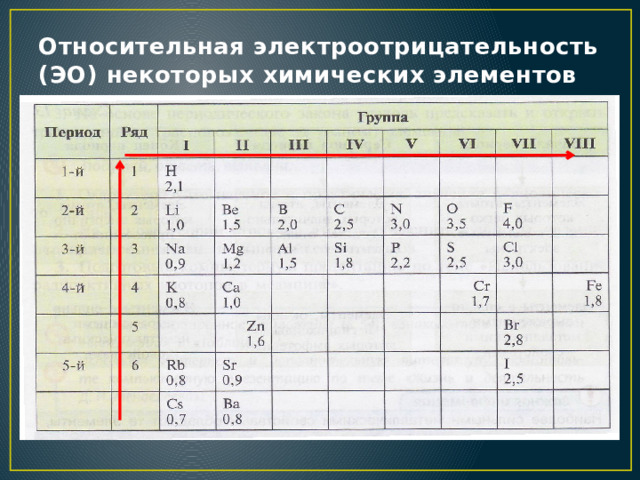 Αν δυο χημικά στοιχεία βρεθούν σε κατάλληλες συνθήκες και υπάρχει διαφορά ηλεκτραρνητικότητας είναι πιθανόν αυτό με την μικρότερη ηλεκτραρνητικότητα να απομακρύνει ή να αποβάλλει ηλεκτρόνια τα οποία θα προσλάβει το άλλο με την μεγαλύτερη σχετικά ηλεκτραρνητικότητα
Αν δυο χημικά στοιχεία βρεθούν σε κατάλληλες συνθήκες και υπάρχει διαφορά ηλεκτραρνητικότητας είναι πιθανόν αυτό με την μικρότερη ηλεκτραρνητικότητα να απομακρύνει ή να αποβάλλει ηλεκτρόνια τα οποία θα προσλάβει το άλλο με την μεγαλύτερη σχετικά ηλεκτραρνητικότητα
ΟΜΟΙΟΠΟΛΙΚΟΣ ΠΟΛΙΚΟΣ ΔΕΣΜΟΣ: ΗΛΕΚΤΡΑΡΝΗΤΙΚΟΤΗΤΑ ΜΙΚΡΟΤΕΡΗ ΤΟΥ 1,7
Αν δυο άτομα διαφορετικής ηλεκτραρνητικότητας συνδεθούν με ομοιοπολικό δεσμό έχουμε ομοιοπολικό πολικό όπου τα ηλεκτρόνια έλκονται περισσότερο από το ηλεκτραρνητικότερο άτομο και το μόριο δημιουργεί δίπολο
Εδώ έχουμε το υδρογόνο με ηλεκτραρνητικότητα 2,1 και το χλώριο με ηλεκτραρνητικότητα 3,0. Τα ηλεκτρόνια έλκονται προς το μέρος του χλωρίου. Το μόριο υδροχλώριο παρουσιάζει διπολική ροπή.
Η διαφορά στην ηλεκτραρνητικότητά τους είναι: 3-2,1 = 0,9< 1,7 άρα ο δεσμός είναι ομοιοπολικός και πολικός εφόσος υπάρχει διαφορά στην ηλεκτραρνητικότητά τους
H2(g) + Cl2 (g) --> 2 Η+δCl-δ ( +δ και -δ δείχνει την πυκνότητα φορτίου σε κάθε άτομο)
ΟΜΟΙΟΠΟΛΙΚΟΣ ΠΟΛΙΚΟΣ ΔΕΣΜΟΣ: ΗΛΕΚΤΡΑΡΝΗΤΙΚΟΤΗΤΑ ΜΕΓΑΛΥΤΕΡΗ ΤΟΥ 1,7
Όσο μεγαλύτερη η διαφορά ηλεκτραρνητικότητα τόσο πολικότερος είναι ο πολικός ομοιοπολικός δεσμός
Σε πολύ μεγάλη διαφορά στην ηλεκτραρνητικότητα όπως το χλώριο και το νάτριο, έχουμε πλήρη απομάκρυνση του ηλεκτρονίου, και σχηματισμό ιόντων και ιοντικού δεσμού
Ηλεκτραρνητικότητα Νατρίου είναι 0,9 και χλωρίου είναι 3,0
Na(s) + Cl (g) --> Na+ + Cl-
Αν δυο άτομα ιδιας ηλεκτραρνητικότητας συνδεθούν με ομοιοπολικό δεσμό έχουμ ομοιοπολικό μη πολικό δεσμοε ο
όπως η δημιουργία μορίου υδρογόνου από δύο άτομα υδρογόνου Η-Η > Η2
Η ΣΗΜΑΣΙΑ ΤΗΣ ΔΙΑΦΟΡΑΣ ΗΛΕΚΤΡΑΡΝΗΤΙΚΟΤΗΤΑΣ ΜΕΤΑΞΥ ΤΩΝ ΑΤΟΜΩΝ
Οι δύο βασικοί τύποι των χημικών δεσμών είναι ο ομοιοπολικός δεσμός και ο ετεροπολικός δεσμός.
Η επιλογή των ατόμων εάν θα συνδεθούν με ομοιοπολικό ή ετεροπολικό δεσμό εξαρτάται από την διαφορά στην ηλεκτραρνητικότητά τους,
δηλαδή την τάση του ατόμου να έλκει προς το μέρος του το κοινό ζευγάρι των ηλεκτρονίων ενός ομοιοπολικού δεσμού (βλέπε κατωτέρω)
Αυτή η διαφορά στην ηλεκταρνητικότητα είναι που διαχωρίζει τους χημικούς δεσμούς σε ετεροπολικό (μεγάλη διαφορά - προσεταιρισμός ηλεκτρονίων από το ένα άτομο ηλεκτρονίων) , σε ομοιοπολικό πολικό (υπάρχει διαφορά αλλά όχι αρκετή για πλήρη απομάκρυνση ηλεκτρονίων)και σε ομοιοπολικό μή πολικό (Διαφορά ηλεκτραρνητικότητα μηδενική )
Περισσότερα για τον ομοιοπολικό και ετεροπολικό δεσμό και την κατασκευή μορίων χημικών ενώσεων θα βρούμε στο κεφάλαιο
.jpg)
Δήμητρα Σπανού
ΠΗΓΕΣ
Ενέργεια ιονισμού και συγγένεια ηλεκτρονίων - τι είναι: ορισμός, χαρακτηριστικά και τύποι