Δήμητρα Σπανού, συνταξιούχος καθηγήτρια χημικός Β/θμιας Εκπ/σης
ΕΙΣΑΓΩΓΗ
Ο ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ
Δύο ή περισσότερα άτομα αλληλεπιδρούν και σχηματίζουν ένα σταθερότερο σύστημα από 2 ή περισσότερα άτομα. Βασίζεται σε θεωρίες ηλεκρονιακών αλληλεπιδράσεων στις οποίες συμμετέχουν κυρίως τα ηλεκτρόνια του τελευταίου ή του προτελευταίου ηλεκτρονιακού ενεργειακού επιπέδου. Τα ημιτελή στρώματα ηλεκτρονίων των εξωτερικών στοιβάδων των ατόμων είναι ασταθή και τέτοια άτομα προσπαθούν να συνδυαστούν με άλλα άτομα με στόχο την αναδιάρθωση των ηλεκτρονίων αυτών.
Ο χημικός δεσμός συνοδεύεται από μεταβολή της συνολικής ενέργειας του συστήματος και υπάρδιαφορετικοί τρόποι που πραγματοποιείται και εξηγείται έχοντας υπ' όψη με την ενέργεια ιοντισμού των χημικών στοιχείων, την ηλεκτραρνητικότητα, την ηλεκτροσυγγένεια
Πληρέστερες ερμηνείες για την δημιουργια των χημικών ενώσεων από τα χημικά στοιχεία και για τους χημικούς δεσμούς έχουν διατυπωθεί:
ΜΕ ΒΑΣΗ ΤΗΝ
Α. ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΣΤΑΘΕΡΟΤΗΤΑ ΓΙΑ ΤΗΝ (ΜΕΓΑΛΥΤΕΡΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΣΤΑΘΕΡΟΤΗΤΑ)
Οι τυχόν μεταβολές των συστημάτων που συνοδεύουν, όταν προχωρούν σε σχηματισμό νέων ουσιών όπως είναι οι χημικές ενώσεις, με κριτήριο την συμφερότερη μεταβολή της εσωτερικής τους ενέργειας και της ενθαλπίας τους (θερμοδυναμική σταθερότητα)
Β. ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΚΗ ΘΕΩΡΙΑ (ΓΙΑ ΗΛΕΚΤΡΟΝΙΑΚΗ ΙΣΟΡΡΟΠΙΑ ΤΩΝ ΕΞΩΤΕΡΙΚΩΝ ΗΛΕΚΤΡΟΝΙΩΝ)
Η τάση των χημικών στοιχείων να αποκτούν σταθερότερη ηλεκτρονιακή τοποθέτηση στην κατανομή των ηλεκτρονίων της εξωτερικής τους στοιβάδας (ηλεκτρονιακή ισορροπία)
Γ. ΚΒΑΝΤΙΚΗ ΘΕΩΡΙΑ (ΓΙΑ ΤΗΝ ΚΑΛΥΤΕΡΗ ΚΑΤΑΝΟΜΗ ΤΟΥ ΗΛΕΚΤΡΟΝΙΑΚΟΥ ΦΟΡΤΙΟΥ ΣΤΟΝ ΧΩΡΟ)
Ο συνδυασμος ατομικών τροχιακών για την δημιουργία μοριακών τροχιακών για την νέα κατανομή του ηλεκτρονιακού φορτίου στον χώρο βάσει της προσσέγγισης νέων φορτισμένων σωματιδίων στον χώρο
Ας θυμώμαστε πάντα πως, κατά τον σχηματισμό και διατήρηση των χημικών ενώσεων ισχύουν αρχές και νόμοι κάποιοι εκ των οποίων είναι οι Μεγάλοι Γενικοί Νόμοι της Φυσικής και της Φύσης, όπως για παράδειγμα οι νόμοι της θερμοδυναμικής, ο νόμος του ισοζυγίου, της διατήρησης και της μεταφοράς εφαρμοσμένοι στις χημικές διαδικασίες.
Στοιχεία για να αποφασίσουμε εάν θα σχηματιστεί κάποια χημική ένωση ή οχι, μας δίνει η κατανομή των ηλεκτρονίων και οι πληροφορίες που μπορούμε να αντλήσουμε για το δεύτερο θέμα που μπορεί να είναι το δυναμικό ιοντισμού ενέργεια ιοντισμού και η ενεργεια δέσμευσης του δεσμού
Η ΗΛΕΚΤΡΟΝΙΑΚΗ ΙΣΟΡΡΟΠΙΑ ΚΑΙ ΤΡΟΧΙΑΚΑ ΤΩΝ ΗΛΕΚΤΡΟΝΙΩΝ
Α. ΤΑ ΑΤΟΜΙΚΑ ΤΡΟΧΙΑΚΑ
( μεταφορά από το κεφάλαιο: Η ΧΗΜΕΙΑ ΠΕΡΙΓΡΑΦΕΙ ΤΗΝ ΥΛΗ ΜΕΣΑ ΑΠΟ ΤΗΝ ΣΥΓΧΡΟΝΗ ΦΥΣΙΚΗ: Δόμηση των ατόμων 3. Κατανομή των ηλεκτρονίων των ατόμων σε ηλεκτρονιακές στοιβάδες. Ατομικά τροχιακά. Μοριακά τροχιακά)
Οι θεωρία της κυματοειδούς φύσης των ηλεκτρονίων του Schrodinger που δίνουν την χωρική κατανομή του φορτίου του ηλεκτρονίου που θεωρείται σαν ηλεκτρικό κύμα,
αλλά και η στατιστκή ερμηνεία του Max Born που δίνει την πιθανότητα να βρίσκεται το ηλεκτρόνιο - σωματίδιο σε διάφορα σημεία του χώρου στον οποίο κινείται,
δίνουν μια νέα εικόνα για την δομή του ατόμου αυτήν των ατομικών τροχιακών
Εδώ, Τα ηλεκτρόνια δεν περιστρέφονται γύρω από τον πυρήνα αλλά βρίσκονται σαν στάσιμα κύματα λάμβάνοντας κάθε φορά την χαμηλότερη δυνατή ενέργεια σύμφωνα με τα καβαντικά πρότυπα. Αυτή η οπτική είναι αναμενόμενη, εφόσον οι διαστάσεις μεγεθών σε αυτούς τους χώρους δεν είναι μετρήσιμες. Χαπακτηριστικά. Διάμετρος ατόμου υδρογόνου είναι 0,1nm και ταχύτητα περιστροφής ηλεκτρονίου 2,2.106m/sec
Την θεωρία των ατομικών και μοριακών τροχιακών πρότεινε Robert Sanderson Mulliken, το 1932 ξεκινώντας από την εξίσωση
Σρέντινγκερ. Η λύση της εξίσωσης Η λύση της εξίσωσης δίνει ένα σύνολο κυματοσυναρτήσεων καθεμία από τις οποίες αντιστοιχεί σε συγκεκριμένη τιμή ενέργειας του ηλεκτρονίου και αποτελεί το τροχιακό 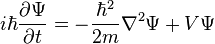
Όταν ορίσουμε την ενέργεια του ηλεκτρονίου Εn,
η επίλυση της εξίσωσης Schrödinger οδηγεί στις κυματοσυναρτήσεις ψ που περιγράφουν την κατάσταση του ατομικού τροχιακού.
Αν και ο τρόπος που θα κινηθεί ένα ηλεκτρόνια δεν είναι ανεξάρτητος από τις κινήσεις και τις αλληλοεπιδράσεις με άλλα ηλεκτρόνια, θεωρητικά από την επίλυση της εξίσωσης Schrödinger,
για κάθε ηλεκτρόνιο υπάρχει ένας μοναδικός και συγκεκριμένος τρόπος να κινείται στο άτομο ο οποίος καθορίζεται από 4 κβαντικούς αριθμούς* (n, l, ml, ms)
Για να ξεπεράσουμε τις αλληλοεπιδράσεις και να μπορέσουμε να δώσουμε τον χώρο που θα περιγράφει ένα ατομικό τροχιακό, επιλέγουμε το άτομο του υδρογόνου το οποίο έχει ένα ηλεκτρόνιο άρα οι αλληλοεπιδράσεις αποκλείονται.
Εαν θέλουμε να περιγράψουμε ατομικά τροχιακά πολυηλεκτρονιακών ατόμων παίρνουμε αυτό το ατομικό τροχιακό του υδρογόνου που έχουμε, σαν σημεία εκκίνησης για την προσσέγγιση άλλων κυματοσυναρτήσεων που εξαρτώνται από ταυτόχρονες συντεταγμένες όλων των ηλεκτρονίων.
Ακόμα επειδή στην εξίσωση ο Schrodinger θεωρεί ότι το ηλεκτρόνιο δεν είναι παρά ένα φορτισμένο νέφος δύσκολο να εντοπιστεί, ορίζεται στην συνέχεια η πυκνότητα αυτού του νέφους σαν το τετράγωνο της συνάρτησης Schrodinger στο συγκεκριμένο σημείο. Αυτό έρχεται σε συμφωνία με την πιθανοτική ερμηνεία του τετραγώνου της κυματοσυνάρτησης από τον Max Bohr
Σημειώνεται ότι η θεωρία των ατομικών τροχιακών έρχεται κατ αρχάς σε αντίθεση με το μοντέλο του Bohr που θεωρεί τοά ηλεκτρόνιο σαν σωματίδιο που κινείται σε τροχαιά γύρω από τον πυρή
TA ATOΜΙΚΑ ΤΡΟΧΙΑΚΑ ΓΙΑ ΤΙΣ ΥΠΟΣΤΟΙΒΑΔΕΣ s, p, d:
 Κάθε ένα από τα ατομικά τροχιακά της κάθε στοιβάδων συμπληρώνεται ανάλογα: με 2 ηλεκτρόνια (s υποστοιβάδα) 6 ηλεκτρόνια (p υποστοιβάδα), 10 ηλεκτρόνια (d υποστοιβάδα), κ.λ.π Τα ατομικά τροχιακά μιας υποστοιβάδας έχουν ίδιο κύριο και δευτερεύοντα κβαντικό αριθμό
Κάθε ένα από τα ατομικά τροχιακά της κάθε στοιβάδων συμπληρώνεται ανάλογα: με 2 ηλεκτρόνια (s υποστοιβάδα) 6 ηλεκτρόνια (p υποστοιβάδα), 10 ηλεκτρόνια (d υποστοιβάδα), κ.λ.π Τα ατομικά τροχιακά μιας υποστοιβάδας έχουν ίδιο κύριο και δευτερεύοντα κβαντικό αριθμό
Η υποστοιβάδα s (l=0) διαθέτει ένα μόνο επίπεδο περιστροφής και συμπληρώνεται με δύο ηλεκτρόνια.
Η υποστοιβάδα p(l=1) διαθέτει τρία επίπεδα περιστροφής τα x, y, z και συμπληρώνεται με 2x3=6 ηλεκτρόνια.
Η υποστοιβάδα d(l=2) διαθέτει πέντε επίπεδα περιστροφής και συμπληρώνεται με 2x5=10 ηλεκτρόνια.
ΑΠΟ ΤΑ ΑΤΟΜΙΚΑ ΣΕ ΜΟΡΙΑΚΑ ΤΡΟΧΙΑΚΑ
Οι όροι ατομικό τροχιακό και μοριακό τροχιακό εισήχθησαν από τον Robert S Mulliken to 1932

Όταν δύο ή περισσότερα άτομα συνδυάζονται χημικά για να σχηματίσουν μόριο, τα ατομικά τροχιακά συνδυάζονται επίσης ώστε να σχηματίσουν μοριακά τροχιακά και οι θέσεις των ηλεκτρονίων στα άτομα επίσης.
Αυτό σημαίνει ότι η εξισώση Schrodinger του ατομικού τροχιακού του ηλεκτρονίου στα άτομα, δίνει κάποιες κατά προσέγγιση λύσεις λαμβάνοντας υπ όψη και τα ηλεκτρόνια του πεδίου του πυρήνα των ατόμων στο μόριο .
.
Πρακτικά, τα μοριακά τροχιακά προκύπτουν από τον συνδυασμό ατομικών τροχιακών ή υβριδικών τροχιακών κάθε ατόμου στο μόριο που χρησιμοποιούνται μόνο όταν το άτομο προκειται να σχηματίσει χημικούς δεσμούς
Η κατασκευή των μοριακών τροχιακών από ατομικά βασίζεται στην αρχή της υπέρθεσης που είναι ο συνδυασμος ατομικών τροχιακών για την δημιουργία μοριακών τροχιακών εάν οι συμμετρίες μεταξύ των ατομικών τροχιακών είναι συμβατές μεταξύ τους, δηλαδή εάν υπάρχει αλληλοεπικάλυψη των ατομικών τροχιακών γιατί αυτό δείχνει πόσο αλληλοεπιδρούν τα ατομικά τροχιακά μεταξύ τους κυρίως εκείνα που είναι παραπλήσια ενεργειακά
Ας θυμηθούμε....
Τα τελευταία ηλεκτρόνια του ατόμου τοποθετούνται στην εξωτερική στοιβάδα ή εξωτερικό κέλυφος ή φλοιός
Η εξωτερική στοιβάδα ή εξωτερικό κέλυφος ή στοιβάδα σθένους διαθέτει από 1 έως 8 ηλεκτρόνια, εκτός από την πρώτη που διαθέτει από 1 έως 2
Τα γεμάτα εσωτερικά κελύφη ηλεκτρονίων έχουν συνολική μαγνητική ροπή από περιστροφή ηλεκτρονίων ίση με μηδέν αφού όλα τα ηλεκτρόνια είναι με αντίθετες περιστροφές. Αυτά είναι τα άτομα των ευγενών αερίων στα οποία δεν κάνουν χημικούς δεσμούς
Έτσι, τα άτομα "επιθυμούν" την σταθερότητα με την απόκτηση ηλεκτρονιακής δομής ευγενών αερίων
ΠΗΓΕΣ
Ατομικό τροχιακό - Βικιπαίδεια
σημείωση *
ΟΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ
μεταφορά από το κεφάλαιο: Η ΧΗΜΕΙΑ ΠΕΡΙΓΡΑΦΕΙ ΤΗΝ ΥΛΗ ΜΕΣΑ ΑΠΟ ΤΗΝ ΣΥΓΧΡΟΝΗ ΦΥΣΙΚΗ: Δόμηση των ατόμων 3. Κατανομή των ηλεκτρονίων των ατόμων σε ηλεκτρονιακές στοιβάδες. Ατομικά τροχιακά. Μοριακά τροχιακά
Για να γίνει αυτό λαμβάνουμε υπ' όψην μας ότι κάθε ένα από τα ηλεκτρόνια του ατόμου είναι διαφορετικά ορισμένο από τους 4 κβαντικούς αριθμούς και τοποθετείται σε συγκεκριμένης απόσταση από τον πυρήνα που καθορίζεται από την ενέργειά τους και περιγράφεται με αυτούς τους κβαντικούς αριθμούς
Κύριος κβαντικός αριθμός n (1,2,3,4,5,6,7) που προσδιορίζει απόσταση από τον πυρήνα απόσταση από τον πυρήνα του ηλεκτρονίου και ταυτόχρονα της ενέργειας σε ακίνητη κατάσταση Είναι (K/n=1, L/n=2, M/n=3, N/n=4, O/n=5, Q/n=6,
Τον Δευτερεύοντα κβαντικό αριθμο l που προσδιορίζει τις υποστοιβάδες που περιλαμβάνει υποομάδες ηλεκτρονίων (υποστοιβάδες) της κάθε στοιβάδας ανάλογα με τον χώρο κατανομής τους . Δίνει το σχήμα του ηλεκτρονιακού νέφους
Παίρνει τιμές l= 0, 1, 2 ,3, 4, (n-1) . Οι υποστοιβάδες είναι οι s, p, d, f, g,h,i
Ηλεκτρόνια με ίδιο n και l βρίσκονται στην ίδια υποστοιβάδα
Ο μαγνητικός κβαντικός αριθμός ml καθορίζει τον προσανατολισμό του ηλεκτρονιακού νέφους σε σχέση με τους άξονες x, y, z,
δηλαδή, τα επίπεδα που θα κινηθεί το κάθε περιστρεφόμενο ηλεκτρόνιο
Σε κάθε υποστοιβάδα που εμφανίζει λόγω αυτής της περιστροφής του μαγνητική ροπή και μηχανική ροπή λόγω αυτής, που καθορίζεται από τον μαγνητικό αριθμό ml .
Τιμές του μαγνητικού κβαντικού αριθμού αντιστοιχεί στο τροχιακά l. και είναι: -l, ...0...+l
Ο κβαντικός αριθμός ms καθορίζεται από το άθροισμα των διανυσμάτων l και s δηλαδή περιλαμβάνει
την γωνιακή ορμή του ηλεκτρονίου που προκαλείται από την ιδιοπεριστροφή του (ορμή spin). Παίρνει τιμές 1/2 για στροφορμή παράλληλη με το Β του πεδίο και -1/2 για στροφορμή αντιπαράλληλη με το Β του πεδίου
Ηλεκτρόνια με ίδιο n, l, ml βρίσκονται στο ίδιο τροχιακό
Από ΤΟΝ ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΣΜΟ
- Αυτό συμβαίνει με δύο τρόπους,ως εξής:
- Α. Με ΟΜΟΙΟΠΟΛΟΚΟ ΔΕΣΜΟ Συμπλήρωση των μονήρων τροχιακών με σύζευξη των τροχιακών των δύο ατόμων σε μοριακό τροχιακό, κι αυτό εάν
- υπάρχει πλησίον άλλο άτομο με μικρή διαφορά στην ενέργεια ιοντισμού και την ηλεκτροσυγγένεια
- Το μοριακό τροχιακό ανήκει και στα δύο προσκείμενα άτομα και συμπληρωμένο είναι με μηδενική η τροχιακή στροφορμή για μεγαλύτερη σταθερότητα
- Αυτός είναι ομοιοπολικός δεσμός
- Οι ομοιοπολικοί δεσμοί σχηματίζουν ζεύγη ηλεκτρονίων σθένους με μηδενικό spin και τροχιακές ροπές , άρα μηδενικές μαγνητικές ροπές
- Β. ΜΕ ΕΤΕΡΟΠΟΛΙΚΟ ή ΙΟΝΤΙΚΟ ΔΕΣΜΟ
- Με την απομάκρυνση μη συζευγμένων ηλεκτρόνιων της εξωτερικής τους στοβάδας,(ΙΟΝΤΑ και ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ)
Οι Ιοντικοί δεσμοί έχουν συνήθως μηδενική μαγνητική ροπή εφόσος και στα κατιόντα και στα ανιόντα η ηλεκτρονική δομή μιμείται αυτήν των ευγενών αερίων
- Β. ΕΠΕΞΗΓΗΣΕΙΣ
- ΑΠΟ ΤΗΝ ΣΥΓΧΡΟΝΗ ΦΥΣΙΚΗ
- τι είναι το ΑΤΟΜΙΚΟ ΤΡΟΧΙΑΚΟ
- H Κυματοσυναρτηση που προκύπτει από την επίλυση της εξίσωσης Schrondinger που προσδιορίζει την περιοχή του τρισδιάστατου χώρου στην οποία υπάρχει πιθανότητα να βρεθεί το ηλεκτρόνιο ενός ατόμου που έχει μια συγκεκριμένη ενέργεια. Κάθε ηλεκτρόνιο του ατόμου βρίσκεται σε συγκεκριμένο τροχιακό.
- Σε πολλές περιπτώσεις, τα ατομικά τροχιακά επικαλύπτονται και αυτό δημιουργεί νέα μοριακά που ονομάζονται τροχιακά δεσμών ή δεσμικά τροχιακά
-
Η θεωρία της κυματοειδούς φύσης των ηλεκτρονίων του Schrodinger που δίνουν την χωρική κατανομή του φορτίου του ηλεκτρονίου που θεωρείται σαν ηλεκτρικό κύμα,
αλλά και η στατιστκή ερμηνεία του Max Born που δίνει την πιθανότητα να βρίσκεται το ηλεκτρόνιο - σωματίδιο σε διάφορα σημεία του χώρου στον οποίο κινείται,
Αυτά δίνουν μια νέα εικόνα για την δομή του ατόμου, την εικόνα των ατομικών τροχιακών
- Η ΧΗΜΙΚΗ ΕΝΩΣΗ προκύπτει όταν δύο ή περισσότερα άτομα συνδυάζονται χημικά για να σχηματίσουν μόριο, οπότε ατομικά τροχιακά τους συνδυάζονται επίσης ώστε να σχηματίσουν μοριακά τροχιακά και οι θέσεις των ηλεκτρονίων στα άτομα επίσης καταλαμβάνονται ανάλογα.
-
Τα μοριακά τροχιακά είναι μια κατά προσέγγιση επίλυση της εξίσωσης Schrondinger για τα ηλεκτρόνια
-
Οι γραμμικοί συνδυασμοί ατομικών τροχιακών ή τα αθροίσματα ή οι διαφορές τους παρέχουν λύσεις στις εξισώσεις Hartee- Fock που αντιστοιχούν στην προσέγγιση ανεξάρτητων σωματιδίων της μοριακής εξίσωσης Schrondinger.
-
.jpg)
- Δήμητρα Σπανού
ΠΗΓΕΣ
Ηλεκτραρνητικότητα - Βικιπαίδεια
Νόμος της σταθερότητας - Βικιπαίδεια (wikipedia.org)
Η ΧΗΜΕΙΑ ΠΕΡΙΓΡΑΦΕΙ ΤΗΝ ΥΛΗ ΜΕ ΤΟΝ ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΣΜΟ: 5ο μέρος. Μετατροπή ατόμων σε ιόντα . Ο ρόλος της μαγνητική ροπή των ηλεκτρονίων
Η ΧΗΜΕΙΑ ΠΕΡΙΓΡΑΦΕΙ ΤΗΝ ΥΛΗ ΜΕΣΑ ΑΠΟ ΤΗΝ ΚΛΑΣΣΙΚΗ ΦΥΣΙΚΗ . 3ο . Μεταβολές στην Εσωτερική Ενέργεια και Ενθαλπία κατά τον σχηματισμό μορίων, ιοντικών πλεγμάτων, συσσωματώσεων των δομικών μονάδων της Ύλης
Μοριακό τροχιακό - Βικιπαίδεια (wikipedia.org)
Ατομικό τροχιακό - Βικιπαίδεια
| Στοιχείο | ε | Στοιχείο | ε | Στοιχείο | ε |
|---|---|---|---|---|---|
| H | 0,7542 | Να | 0,548 | K | 0,502 |
| Αυτός | -0,54 | Mg | -0,4 | Γ | -0,3 |
| Λι | 0,618 | Αλ | 0,441 | Sc | 0,14 |
| Είμαι | -0,5 | Σι | 1,385 | Τι | -0,40 |
| B | 0,277 | P | 0,747 | V | -0,94 |
| C | 1,263 | S | 2,077 | Κρ | -0,98 |
| N | -0,07 | Κλ | 3,617 | Mn | 1,07 |
| Περίπου | 1,461 | Br | 3,365 | Φε | -0,58 |
| F | 3,399 | Εγώ | 3,06 | Σία | -0,94 |
| Ne | -1,2(2) | Νι | -1,28 | ||
| Cu | -1,80 |

