Δήμητρα Σπανού συνταξιούχος χημικός καθηγήτρια Βθμιας Εκπαίδευσης
ΘΕΡΜΙΚΗ ΑΓΩΓΙΜΟΤΗΤΑ ΥΛΙΚΩΝ
Η θερμική αγωγιμότητα είναι η ικανότητα μιας ουσίας να μεταφέρει θερμότητα μέσα της.
Αποτελεί μια σημαντική ιδιότητα για τα χημικά στοιχεία, που γίνεται μέσω της χαοτικής κίνησης των στοιχειωδών σωματιδίων των σωμάτων (άτομα, μόρια, ηλεκτρόνια) και καθορίζεται από τις ιδιότητες των ατόμων και των μορίων τους και την δομή τους, την θέση τους στον περιοδικό πίνακα και τις φυσικές τους ιδιότητες όπως η πυκνότητά τους, η αντοχή τους η θερμοχωρητικότητα, η σκληρότητα.
Επίσης καθορίζεται από την κλίση των θερμοκρασιών (grad). Δηλαδή, η θερμική αγωγιμότητα εξαρτάται από τις συνθήκες μεταφοράς όπως από την κλίση της θερμοκρασίας, δηλαδή την διαφορά θερμοκρασίας μεταξύ των περιοχών που μεταφέρεται θερμότητα.
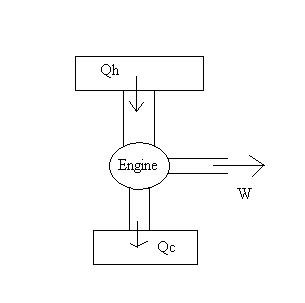
Εξηγείται μέσω της αλληλεπίδρασης των σωματιδίων της ύλης: τα μόρια σε θερμότερα μέρη του σώματος κινούνται και μεταφέρουν ενέργεια μέσω των συγκρούσεων σε πιο αργά σωματίδια σε ψυχρότερα μέρη του σώματος
 Δεν έχουν όλα τα χημικά στοιχεία την ίδια ικανότητα να μεταφέρουν θερμότητα. Υπάρχουν χημικά στοιχεία με υψηλή θερμική αγωγιμότητα όπως τα μέταλλα και άλλα με χαμηλότερη και συνεχίζεται έως ότου επιτευχθεί η θερμοδυναμική ισορροπία σύμφωνα με τον δεύτερο νόμο της Θερμοδυναμικής
Δεν έχουν όλα τα χημικά στοιχεία την ίδια ικανότητα να μεταφέρουν θερμότητα. Υπάρχουν χημικά στοιχεία με υψηλή θερμική αγωγιμότητα όπως τα μέταλλα και άλλα με χαμηλότερη και συνεχίζεται έως ότου επιτευχθεί η θερμοδυναμική ισορροπία σύμφωνα με τον δεύτερο νόμο της Θερμοδυναμικής
Η μέτρηση της θερμικής αγωγιμότητας γίνεται σε μονάδες watt ανά μέτρο επί βαθμό Κέλβιν W/m.K
Παραθέτω ορισμένα χημικά στοιχεία από όπου φαίνεται ότι άλλα από αυτά έχουν μεγάλη θερμική αγωγιμότητα και είναι κατάλληλα για την μεταφορά θερμότητας και άλλα μικρή και χρησιμοποιούνται σαν μονωτές
ΣΥΝΤΕΛΕΣΤΗΣ ΘΕΡΜΙΚΗΣ ΑΓΩΓΙΜΌΤΗΤΑΣ ΣΤΟΙΧΕΙΩΝ
Αργό 0,016284 W/(m·K) Άζωτο 0,02583 W/(m·K), Οξυγόνο 0,026184 W/(m·K), Υδρογόνο 0,1805 W/(m·K), Μόλυβδος 35 W/(m.K),
Σίδηρος 80.19 W/(m·K), Αργίλιο 205 W/(m·K), Χαλκός 401 W/(m·K), Ασημί 429 W/(m·K), Διαμάντι 2200 W/(m·K)
Για την μεταφορά θερμότητας λαμβάνεται υπ ίψην και ο συντελεστής θερμικής αγωγιμότητας λ στον οποίο συμπεριλαμβάνεται και το πάχος του αγωγού με τον οποίο μεταφέρεται η θερμότητα
|
N |
0,02583 |
0,026 |
|
|
O |
0,02658 |
0,027 |
|
|
F |
0,02591 |
0,028 |
|
|
Ne |
0,0491 |
0,0493 |
|
|
Να |
142 |
142 |
|
|
Mg |
156 |
156 |
|
|
Αλ |
237 |
237 |
|
|
Σι |
149 |
149 |
|
Χημικό Στοιχείο |
Ατομικός αριθμός/ ομάδα/περίοδος |
Λ (W/m.K) |
Ρ( kg/m3) |
Ατομική ακτίνα pm |
Ενέργεια ιοντ(ι)σμού KJ/mol |
Σημείο τήξης Co |
|
Αργό |
18/18/3 |
0,016184 |
|
71 |
|
-189 |
|
Θείο |
16/16/3 |
0,205 |
1960 |
88 |
999,6 |
115,21 |
|
Άζωτο |
14/15/2 |
0,02583 |
|
56 |
|
-210,1 |
|
Οξυγόνο |
8/16/2 |
0,026184 |
|
48 |
|
-218 |
|
Υδρογόνο |
1/1/1 |
0,1805 |
|
53 |
|
-259,9 |
|
Ιώδιο |
53/17/5 |
0,449 |
4,940 |
115 |
1008,4 |
113,7 |
|
Τελλούριο |
52/16/5 |
3 |
6240 |
123 |
869,3 |
449,51 |
|
Ακτίνιο |
89/ακτινίδες/7 |
12 |
10070 |
|
499 |
1050 |
|
Λανθάνιο |
57/λανθανίδες/6 |
13 |
6146 |
|
538,1 |
919,9 |
|
Πρασεοδύμιο |
59/λανθανίδες/6 |
13 |
6640 |
247 |
527 |
930,9 |
|
Ουράνιο |
92/ακτινίδες/7 |
27 |
19500 |
|
597,6 |
1135 |
|
Κασσίτερος |
50/14/5 |
67 |
7310 |
145 |
708,6 |
231,93 |
|
Σίδηρος |
26/8/4 |
80,19 |
7870 |
156 |
762,5 |
1538 |
|
Ινδιο |
49/13/5 |
82 |
7310 |
156 |
558,3 |
156,6 |
|
Λίθιο |
3/1/2 |
85 |
535 |
167 |
520,2 |
180,54 |
|
Μόλυβδος |
82/14/6 |
35 |
11340 |
154 |
715,6 |
327,46 |
|
Νάτριο |
11/1/3 |
140 |
968 |
190 |
495,8 |
97,92 |
|
Πυρίτιο |
14/14/3 |
150 |
2330 |
111 |
786,5 |
1414 |
|
Μαγνήσιο |
12/2/3 |
160 |
1738 |
145 |
737,7 |
650 |
|
Αργίλιο |
13/13/3 |
235 |
2700 |
118 |
577,5 |
660,32 |
|
Χρυσός |
79/11/6 |
320 |
19300 |
174 |
890,1 |
1064,18 |
|
Χαλκός |
29/11/4 |
401 |
8940 |
145 |
745,5 |
1084,62 |
|
Ασήμι |
47/11/5 |
430 |
10500 |
165 |
731 |
961,68 |
|
Άνθρακας |
6/14/2 |
140 |
2260 |
67 |
1085,5 |
3642 |
|
Αμερίκιο |
95/ακτινιδες/7 |
10 |
13670 |
|
578 |
1176 |
|
Νεοδύμιο |
60/λανθανίδες/6 |
17 |
7010 |
206 |
533,1 |
1021 |
|
Κρυπτό |
36/18/4 |
0,00943 |
3,75 |
88 |
1350,8 |
-157,36 |
 (1).jpg)
μια λίστα χημικών στοιχείων και η θερμική τους αγωγιμότητα.
Το αλουμίνιο είναι ένα από τα πιο θερμικά αγώγιμα μέταλλα, με θερμική αγωγιμότητα περίπου 205 W/(m·K).
Το ασήμι είναι το πιο θερμικά αγώγιμο μέταλλο, η θερμική του αγωγιμότητα φτάνει τα 429 W/(m·K).
Ο χαλκός έχει επίσης υψηλή θερμική αγωγιμότητα (398 W/(m·K)), επομένως χρησιμοποιείται ευρέως στην ηλεκτρονική και την ηλεκτρική μηχανική.
Σίδηρος – η θερμική αγωγιμότητα αυτού του μετάλλου είναι περίπου 80 W/(m·K).
Μόλυβδος – σε αντίθεση με τα προηγούμενα στοιχεία, ο μόλυβδος έχει χαμηλή θερμική αγωγιμότητα (35 W/(m·K)), επομένως χρησιμοποιείται συχνά για προστασία από την ακτινοβολία.
Источник: https://granit.dartaygi.ru/himiya/teploprovodnost-vsekh-khimicheskikh-elementov
Τα ακόλουθα είναι μερικά από τα χημικά στοιχεία ταξινομημένα με βάση τη θερμική τους αγωγιμότητα:
Αργό – 0,016284 W/(m·K)
Άζωτο – 0,02583 W/(m·K)
Οξυγόνο – 0,026184 W/(m·K)
Υδρογόνο – 0,1805 W/(m·K)
Αλουμίνιο – 237 W/(m·K)
Σίδηρος – 80.19 W/(m·K)
Χαλκός – 401 W/(m·K)
Ασημί – 429 W/(m·K)
Διαμάντι – 2200 W/(m·K)
Источник: https://granit.dartaygi.ru/himiya/teploprovodnost-vsekh-khimicheskikh-elementov

