Δήμητρα Σπανού, χημικός, συνταξιούχος καθηγήτρια Μέσης Εκπαίδευσης από 30-6-2025
υπό κατασκευή

ΔΙΑΣΠΑΣΗ ΕΚΦΥΛΙΣΜΕΝΩΝ d ΤΡΟΧΙΑΚΩΝ ΜΕΤΑΒΑΤΙΚΟΥ ΙΟΝΤΟΣ
Σε ένα ελεύθερο άτομο ή ιόν στοιχείων μεταπτώσεως, στην αέρια φάση, όλα όλα τα d τροχιακά είναι ενεργειακά ισότιμα (εκφυλισμένα) ώστε ένα ηλεκτρόνιο να έχει ίδια πιθανότητα να βρεθεί σε ένα από αυτά
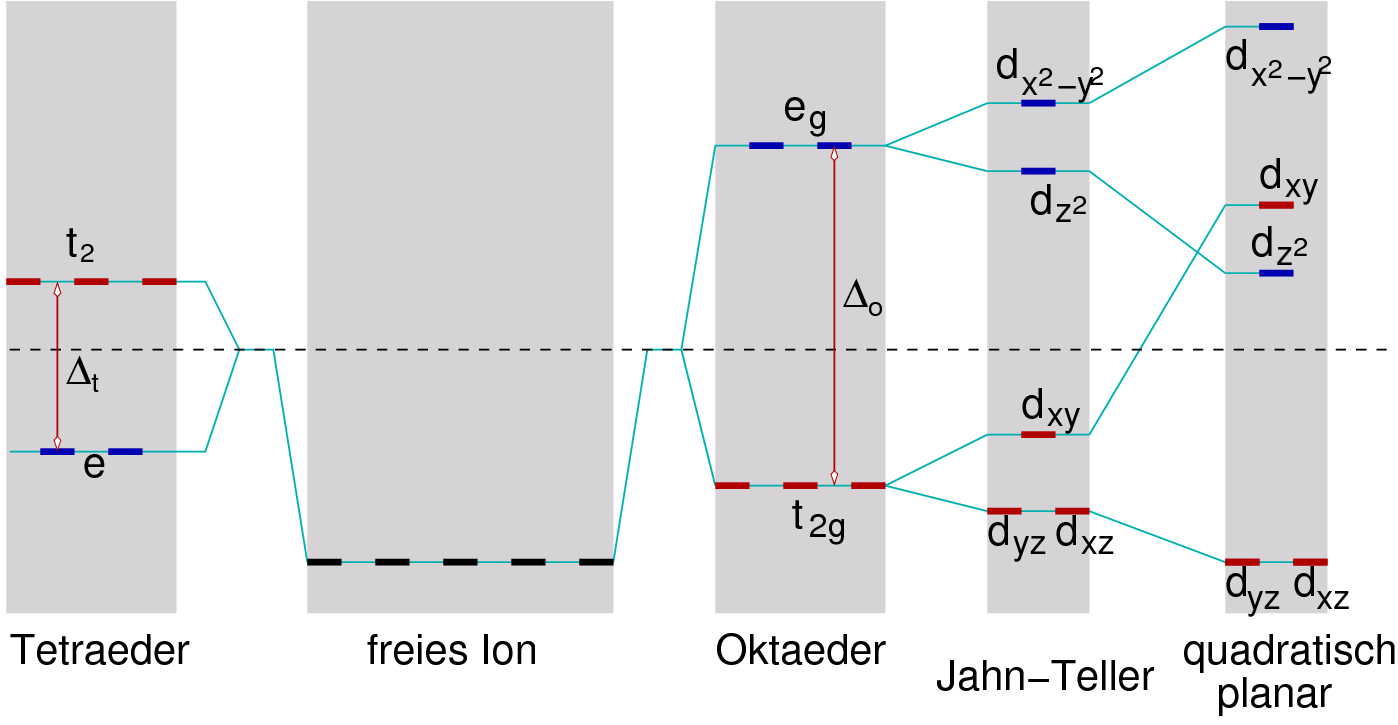
Όταν σχηματίζεται σύμπλοκο τα d τροχιακά υφίστανται διάσπαση (splitting) σε διαφορετικά ενεργειακά επίπεδα λόγω του ηλεκτροστατικού πεδίου των υποδοχέων (Ligands)
Δ. ή 10Dq ENEΡΓΕΙΑ ΔΙΑΧΩΡΙΣΜΟΥ ΚΡΥΣΤΑΛΛΙΚΟΥ ΠΕΔΙΟΥ Είναι η διαφορά ενέργειας μεταξύ χαμηλών ενεργειακών σταθμών των τροχιακών t2g και υψηλών eg. Η μέση ενέργεια των d τροχιακών αποτελεί το βαρύκεντρο.
Α. Η Δ ή 10Dq ENEΡΓΕΙΑ ΔΙΑΧΩΡΙΣΜΟΥ ΚΡΥΣΤΑΛΛΙΚΟΥ ΠΕΔΙΟΥ
Εξαρτάται
1. Από την οξειδωτική κατάσταση του μετάλλου (Αύξηση οξειδωτικής κατάτασης- Αύξηση της Δ)
Όσο υψηλότερη είναι η κατάσταση οξείδωσης του μετάλλου τόσο ισχυρότερο είναι το πεδίο του υποκαταστάτη. Κι αυτό επειδή αυξημένο φορτίο συστέλλει την ιοντική ακτίνα και αυξάνει την αλληλεπίδραση των αρνητικά φορτισμένων υποκαταστατών. Αυτά αυξάνουν την ενέργεια διαχωρισμού του κρυσταλλικού πεδίου Δ.
2. Από τη φύση του μεταλλικού ιόντος
α. Η θέση του μεταλλοιόντος στον περιοδικό πίνακα όπου στην ίδια περίοδος (σειρά) με την Αύξηση του Ατομικού αριθμού το Δο μειώνεται.
β. Στην ίδια ομάδα με την Αύξηση του Ατομικού αριθμού, Αυξάνεται το Δ
Παράδειγμα: Tο μεταλλοιόν Αu+2 6ης περιόδου στον περιοδικό πίνακα και 3ης σειρά στα μέταλλα μεταπτώσεως, εμφανίζει ενέργεια διαχωρισμού κρυσταλλικού πεδίου μεγαλύτερη σε σχέση με τον Cu+2 που βρίσκεται στην ίδια περίοδο αλλά στην 1η σειρά των στοιχείων μεταπτώσεως
Ο Pt+2 και Pb+2 ανήκουν στην 3η και στην 2η σειρά ώστε ο Pt+2 προκαλούν μεγαλύτερη διάσχιση πεδίου. Τα δύο ελεύθερα ηλεκτρόνια δεν μπορούν να σταθεροποιηθούν και ευνοούνται τα επίπεδα τετραγωνικά σύμπλοκα
3. Από τη φύση του Υποκαταστάτη
Υποκαταστάτες ισχυρού πεδίου όπως το CN- αυξάνουν το Δ και υποκαταστάτες χαμηλού πεδίου όπως το Ι- προκαλούν μικρότερο διαχωρισμό Δ
Αυτό δίνεται από την φασματοσκοπική σειρά των υποκαταστατών: Υποκαταστάτες που προκαλούν απο μικρό Δ προς μεγάλο Δ : I-, Br-, S2-, SCN-, Cl-, NO3-, N3-, F-, OH-, H2O, NCS-, CH3CN-, Pyridini, NH3, αιθυλενοδιαμίνη, 2,2΄διπυριδίνη, phen(1,10)- , NO2, τριφαινυλοφωσφίνη, CN-, CO,
Ε. Σ. Κ.Π. (CFSE) ΕΝΕΡΓΕΙΑ ΣΤΑΘΕΡΟΠΟΙΗΣΗΣ ΚΡΥΣΤΑΛΛΙΚΟΥ ΠΕΔΙΟΥ . Υπολογίζεται εάν αθροίσουμε την ενέργεια όλων των ηλεκτρονίων της d υπολογίζοντας αύξηση της ενέργειας για τροχιακά υψηλής ενέργειας και αντίστροφα. Παράδειγμα στο οκτάεδρο έχουμε ενέργεια διαχωρισμού Δο και αύξηση κατά 3/5 Δο για κάθε ηλεκτρόνιο σε eg (αποσταθεροποίηση) και -2/5 για κάθε ηλεκτρόνιο που τοποθετείται σε χαμηλή t2g (σταθεροποίηση)
Ε.Σ.Κ.Π. = [-(nt2g .2Δο/5) + (neg .3Δο/5)]
Στα στοιχεία μεταπτώσεως, τη σύνδεση των υποκαταστατών και η υπαρξη επιπλέον πεδίου υποκαταστατών, κάνει τα αρχικά εκφυλισμένα 5 d τροχιακά διασπώνται αναλόγως. Σε οκταεδρικό σύμπλοκο για παράδειγμα η διάσπαση γίνεται σε τρία χαμηλότερης ενέργειας t2g (2Δο/5) και δύο υψηλότερης ενέργειας eg. (3Δο/5)
Για την ΕΣΚΠ κάθε συμπλόκου, :
Αντικαθιστώ στο Ε.Σ.Κ.Π. = [-(nt2g .2Δο/5) + (neg .3Δο/5)] Για κάθε ηλεκτρόνιο που τοποθετείται στο επίπεδο t2g έχω σταθεροποίηση κατά ο,4Δο ενώ αν τοποθετείται στο eg έχω αποσταθεροποίηση 0,6 Δο
P ή Π ΕΝΕΡΓΕΙΑ ΣΥΖΕΥΞΗΣ (Pairing energy)
Eίναι η ενέργεια που απαιτείται για να βρεθούν δύο ηλεκτρόνια με αντίθετο σπιν στο ίδιο τροχιακό και είναι αντίθετο με την ενέργεια που ελευθερώνεται εάν απομακρυνθουν αυτά από το τροχιακό (ενέργεια διάσπασης)
Οι ενέργειες των δυο ηλεκτρονίων είναι συνήθως διαφορετικές και εξαρτάται από το κεντρικό μέταλλο και το οξειδωτικό του επίπεδο.
Η ΣΤΑΘΕΡΟΤΗΤΑ ΤΩΝ ΚΡΥΣΤΑΛΛΙΚΩΝ ΔΟΜΩΝ.
Β. Η ΣΧΕΣΗ ΤΗΣ ΕΝΕΡΓΕΙΑ ΣΥΖΕΥΞΗΣ Ρ ΚΑΙ ΤΗΣ ΕΝΕΡΓΕΙΑΣ ΔΙΑΧΩΡΙΣΜΟΥ ΕΠΙΡΡΕΑΖΕΙ ΤΗΝ ΔΟΜΗ ΤΟΥ ΣΥΜΠΛΟΚΟΥ
Συγκρίνεται με την ενέργεια διαχωρισμού Δ ως εξής:
Αν Δ> P ευνοείται η κατάσταση χαμηλού σπιν και ωδηγεί σε ισχυρά πεδία
Αν Δ< P ευνοείται η κατάσταση υψηλόυ σπιν και ωδηγεί σε ασθενή πεδία
Κατ' αρχή, για να είναι το σύμπλοκο ιόν όσο το δυνατόν σταθερότερο θα πρέπει το κεντρικό ιόν να περιβάλεται από τον μεγαλύτερο δυνατό αριθμό συνδετών υπό την προυπόθεση βέβαια ότι οι δεσμοί αυτοί ελλατώνουν την συνολική ενέργεια. Οι συνδέτες και το κεντρικό ιόν θα πρέπει επίσης να ταιριάζουν μεταξύ τους και ως προς τις ιοντικές τους ακτίνες.
ΚΑΤΑΣΤΑΣΕΙΣ SPIN 
Από την τοποθέτηση των ηλεκτρονίων στα d τροχιακά εξαρτάται η Ενέργεια Διαχωρισμού πεδίου Δ και το μέγεθος της Δ καθορίζει την κατανομή των ηλεκτρονίων στα d τροχιακά και στην συνέχεια την κατάσταση σπιν του συμπλόκου
Οι διαμορφώσεις σπιν μπορούν να γίνουν νκατανοητές από την θεωρία κρυσταλλικού πεδίου και από την θεωρία πεδίου υποκαταστατών
Για αρκετές καταστάσεις οξείδωσης
- τα μέταλλα της πρώτης σειράς του τομέα d (Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn) μπορούν να υιοθετήσουν διαμορφώσεις υψηλού ή χαμηλού spin
- σημειώνουμε ότι
-
Μόνο τα μέταλλα της πρώτης σειράς του τομέα d (Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn) μπορούν να υιοθετήσουν διαμορφώσεις υψηλού spin
- τα μέταλλα 2ης και 3ης σειράς του τομέα d έχουν πάντα χαμηλό spin
ΜΕΤΑΒΟΛΗ ΣΤΗΝ ΑΚΤΙΝΑ ΣΤΗ ΣΕΙΡΑ ΤΩΝ ΜΕΤΑΒΑΤΙΚΩΝ ΜΕΤΑΛΛΩΝ
Η ιοντική τους ακτίνα αναμένεται να μειώνεται με την αύξηση του πυρηνικού φορτίου και λόγω του εκφυλισμού των d τροχιακών .
Η μεταβολή στη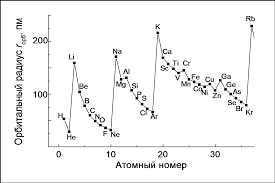 ν ακτίνα στη σειρά μεταβατικών μετάλλων δεν είναι μονότονη λόγω της επίδρασης του κρυσταλλικού πεδίου (ενέργεια σταθεροποίησης κρυσταλλικού πεδίου - CFSE) και της άρσης του εφυλισμού των d τροχιακών. Η ιοντική ακτίνα αυξάνεται επίσης κάθε φορά που γίνεται εισαγωγή ηλεκτρονίων στο eg τροχιακό
ν ακτίνα στη σειρά μεταβατικών μετάλλων δεν είναι μονότονη λόγω της επίδρασης του κρυσταλλικού πεδίου (ενέργεια σταθεροποίησης κρυσταλλικού πεδίου - CFSE) και της άρσης του εφυλισμού των d τροχιακών. Η ιοντική ακτίνα αυξάνεται επίσης κάθε φορά που γίνεται εισαγωγή ηλεκτρονίων στο eg τροχιακό
d1, d2, d3 Τόσο στα υψηλά όσο και στα χαμηλά σπιν, η διαμόρφωση είναι η ίδια (γεμάτη). Η ακτίνα μειώνεται με την αύξηση του πυρηνικού φορτίου.
d4, d5, d6, d7 : Η διαφορά γίνεται σημαντική.
Υψηλό σπιν (d4, d5, d6 d7) Τα ηλεκτρόνια κινούνται προς eg Η ακτίνα είναι μεγαλύτερη.
Χαμηλού σπιν (d4, d5, d6, d7) : Τα ηλεκτρόνια παραμένουν στο t2g
d8, d9, d10 Οι διαμορφώσεις ευθυγραμμίζονται και πάλι με τον αριθμό των ηλεκτρονίων στα
-τροχιακά.
ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΙΑΜΟΡΦΩΣΗ ΓΙΑ ΣΤΟΙΧΕΙΑ ΜΕΤΑΠΤΩΣΕΩΣ
ΣΕ ΠΕΡΙΠΤΩΣΕΙΣ ΠΟΥ ΙΣΧΥΕΙ /ΔΕΝ ΙΣΧΥΕΙ Ο ΝΟΜΟΣ ΤΟΥ ΗUND (ΥΨΗΛΗ ΚΑΤΑΣΤΑΣΗ ΟΞΕΙΔΩΣΗΣ ΜΕΤΑΛΛΟΥ- ΙΣΧΥΡΟ ΠΕΔΙΟ ΥΠΟΚΑΤΑΣΤΑΤΩΝ)
ΔΙΑΜΟΡΦΩΣΗ ΤΩΝ d ΑΠΕΙΚΟΝIΣΕΩΝ ΗΛΕΚΤΡΟΝΙΩΝ ΣΕ ΣΥΜΠΛΟΚΑ. ΙΣΧΥΕΙ ΓΕΝΙΚΑ Ο ΚΑΝΟΝΕΣ ΤΟΥ HUND
Κανόνας του Hund: Ηλεκτρόνια που καταλαμβάνουν εκφυλισμένα τροχιακά (ιδιας υποστοιβάδας), τοποθετούνται πρώτα με παράλληλα σπιν κι έτσι ελαχιστοποιούνται οι απώσεις προσδίδοντας την χαμηλότερη δυνατή ενέργεια . Δηλαδή, γεμίζουν πρώτα μονά ηλεκτρόνια κάθε διαθέσιμο τροχιακό κι μόλις όλα τα τροχιακά έχουν από ένα ηλεκτρόνιο αρχίζει η σύζευξη με αντίθετη φορά με στόχο την ελαχιστοποίηση των ηλεκτροστατικών απώσεων και μεγαλύτερη σταθερότητα
Ακόμα επιρρεάζουν:
Το φορτίο του μεταλλικού ιόντος. Όσο υψηλότερη είναι η κατάσταση οξείδωσης του μετάλλου τόσο ισχυρότερο είναι το πεδίο του υποκαταστάτη. Κι αυτό επειδή αυξημένο φορτίο συστέλλει την ιοντική ακτίνα και αυξάνει την αλληλεπίδραση των αρνητικά φορτισμένων υποκαταστατών. Αυτά αυξάνουν την ενέργεια διαχωρισμού του κρυσταλλικού πεδίου Δ.
Οι Υποκαταστάτες επηρεάζουν το μέγεθος του Δ των d τροχιακών ανάλογα με την ένταση του πεδίου των υποκαταστατών όπως περιγράφεται στη φασματοσκοπική σειρά.
Υποκαταστάτες ισχυρού πεδίου όπως το CN- αυξάνουν το Δ και υποκαταστάτες χαμηλού πεδίου όπως το Ι- προκαλούν μικρότερο διαχωρισμό και πιθανόν υψηλότερο spin.
ΕΤΣΙ, ΠΑΡΑΔΕΙΓΜΑ
ΓΙΑ Τα ΟΚΤΑΕΔΡΙΚΑ ΣΥΜΠΛΟΚΑ
ΟΤΑΝ ΙΣΧΥΕΙ ΚΑΙ ΟΤΑΝ ΔΕΝ ΙΣΧΥΕΙ Ο ΚΑΝΟΝΑΣ ΤΟΥ HUND
ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΙΑΜΟΡΦΩΣΗ ΓΙΑ ΣΤΟΙΧΕΙΑ ΜΕΤΑΠΤΩΣΕΩΣ
ΤΟ SPIN ΤΟΥΣ ΤΟ ΕΣΚΠ ΚΑΙ ΙΟΝΤΚΕΣ ΤΟΥΣ ΑΚΤΙΝΕΣ
Η κατανομή των ηλεκτρονίων στα d τροχιακά ενός μεταβατικού μετάλλου σε οκταεδρικό σύμπλοκο,
έχει ως εξής:
Για την 1η σειρά των μεταβατικών μετάλλων (μεταπτώσεως) τα στοιχχεία σε d1, d2, d3 τροχιακά τοποθετούνται σύμφωνα με τον νόμο του Hund.
Αν πρόκειται για d4 σύμπλοκο υπάρχει περίπτωση να ακλουθεί τον Hund με 4 ασύζευκτα ηλεκτρόνια (Cr+2, Cr+3, Mn+3 με υποκαταστάτες που δεν επιρρεάζουν τον αριθμό οξείδωσης του μετάλλου) Υψηλό σπιν. Είναι παραμαγνητικό. Ιοντική ακτίνα 64,5 pm ΕΣΚΠ -0,6Δο σταθεροποιητική
ή με 2 ασύζευκτα ηλεκτρόνια όταν το Δ είναι μεγάλο και το 4ο ηλεκτρόνιο δεν συμπληρώνει το e τροχιακό υψηλής ενέργειας αλλά ζευγαρώνει ένα από τα t2 . Παραμαγνητικό. Περιλαμβάνει το Cr+2 και το Μn+3 . Χαμηλού σπιν .Ιοντική ακτίνα: 58 μm -1,2Δο Ε.Σ.Κ.Π. απόσταθεροποητική
Αν πρόκειται για d5 σύμπλοκο υπάρχει περίπτωση να ακλουθεί τον Hund me 5 ασύζευκτα ηλεκτρ'ονια (Fe+3, Mn+2) Yψηλού σπιν, Ιοντική ακτίνα 64,5μm παραμαγνητικό ΕΣΚΠ με συνολική 0Δο
και υπάρχει περίπτωση να μην ακλουθεί τον Hund με 1 ασύζευκτο ηλεκτρ'ονιο χαμηλού σπιν παραμαγνητικό Fe+3 , [Fe(CN)6]-3 ιΟντική ακτίνα: 55νm
Αν πρόκειται για d6 σύμπλοκο υπάρχει περίπτωση να ακλουθεί τον Hund me 4 ασύζευκτα ηλεκτρ'ονια Fe+2, Co+3, Υψηλό spin Iοντική ακτίνα Co+3 είναι 61pm. Παραμαγνητικό ΕΣΚΠ -0,4Δο σταθεροποητική
και υπάρχει περίπτωση να μην ακολουθεί τον νομο του Hund και να είναι χωρίς ασύζευκτα ηλεκτρ'ονια Χαμηλό σπιν Ιοντική ακτίνα είναι 62pm για Mn+3 Co+3 είναι 54,5 pm και Ni+4 είναι 48pm
Αν πρόκειται για d7 σύμπλοκο υπάρχει περίπτωση να ακλουθεί τον Hund me 3 ασύζευκτα ηλεκτρόνια (Fe+3, Mn+2) Yψηλού σπιν, παραμαγνητικό ιονική ακτίνα για Co+2 είναι 74,5 pm ΕΣΚΠ -1,2Δο σταθεροποητική
και υπάρχει περίπτωση να μην ακλουθεί τον Hund με 1 ασύζευκτο ηλεκτρ'ονιο χαμηλού σπιν Fe+3 , [Fe(CN)6]-3, το Co+3 έχει ιοντική ακτίνα 65pm. Παραμαγνητικό ΕΣΚΠ 1,2Δο αποσταθεροποιητική
Αν πρόκειται για d8 σύμπλοκο υπάρχει περίπτωση να ακλουθεί τον Hund με 3 ζεύγη ηλεκτρόνια στο t2 και 2 στο eg Yψηλού σπιν, παραμαγνητικό ιονική ακτίνα για Νι+2 είναι 69 pm ΕΣΚΠ (-1,2Δο) σταθεροποητική
Το ίδιο μπορεί να δώσει και
τετραεδρική διαμόρφωση με 2 ασύζευκτα ηλεκτρ'ονια [Ni(CN)4]-2
επίπεδη τετραγωνική χαμηλού σπιν Ιοντικής ακτίνας 49μm
Αν πρόκειται για d9 σύμπλοκο υπάρχει περίπτωση να ακλουθεί τον Hund με 3 ζεύγη ηλεκτρόνια στο t2 και 1 ζεύγος στο eg Yψηλού και 1 μονήρες σπιν, παραμαγνητικό ιονική ακτίνα για Νι+2 είναι 69 pm ΕΣΚΠ συνολική -0,6Δο σταθεροποητική
Αν πρόκειται για d10 σύμπλοκο ΕΣΚΠ συνολική 0Δο Αυτό σημαίνει ότι η σταθεροποίηση ΕΣΚΠ δεν εξαρτάται από τη γεωμετρία του συμπλόκου (πιθανόν να καταλάβει τετραεδρικές ή και οκταεδρικές θέσεις
Η ηλεκτρονιακή διαμόρφωση επιρρεάζει
Για τις ομάδες 3-12 d block και εάν υποθέσουμε ότι δεν επιρρεάζει πολύ το πεδίο του μεταλλικού ιόντος ή των υποκαταστατών και η ενέργεια διαχωρισμού Δ δεν είναι πολύ μεγάλη κι έτσι εξακολουθεί να ισχύει ο νόμος του Hund ΓΙΑ
ΠΑΡΑΔΕΙΓΜΑΤΑ ΓΙΑ ΕΣΚΠ, ΣΠΙΝ, ΙΟΝΤΙΚΗΣ ΑΚΤΙΝΑΣ
Σε οκταεδρικά σύμπλοκα (κεντροσυμμετρικά g η ΕΣΚΠ είναι ως εξής:
Για την 1η σειρά των μεταβατικών μετάλλων (μεταπτώσεως) τα στοιχχεία σε d1, d2, d3 τροχιακά τοποθετούνται σύμφωνα με τον νόμο του Hund.
Για μεταλλικά ιόντα με d1 ηλεκτρονιακή απεικόνιση (Sc, Y): το μοναδικό d ηλεκτρόνιο καταλαμβάνει ένα από τa τρία t2g τροχιακάμε ενέργεια -2Δο/5 (σταθεροποίηση)
Για μεταλλικά ιόντα με d2 , d3 ηλεκτρονιακές απεικονήσεις καταλαμβάνει τα άλλα δύο από τa τρία t2g τροχιακά με ενέργεια σταθεροποίησης σύμφωνα με τον κανόνα του Hund αντίστοιχα 4Δο/5 ή συνολικές (-0,8Δο) και -6Δο/5 ή (-1,2Δο) ( Ε.Σ.Κ.Π.σταθεροποίηση)
Για μεταλλικά ιόντα με d4 ηλεκτρονιακές απεικονήσεις
Α. με 4 ασύζευκτα ηλεκτρόνια (Cr+2, Cr+3, Mn+3 με υποκαταστάτες που δεν επιρρεάζουν τον αριθμό οξείδωσης του μετάλλου)
Ta 3 πρώτα ηλεκτρόνια καταλαμβάνουν τα τρία t2g τροχιακά και το τέταρτο ηλεκτρόνιο το eg με ενέργεια -6Δο/5 ή
και 0,6Δο (αποσταθεροποιητική) με συνολική -0,6Δο σύμφωνα με τον κανόνα του Hund αντίστοιχα ( Ε.Σ.Κ.Π σταθεροποίηση)
Είναι παραμαγνητικό
Β. ή με 2 ασύζευκτα ηλεκτρόνια όταν το Δ είναι μεγάλο και το 4ο ηλεκτρόνιο δεν συμπληρώνει το e τροχιακό υψηλής ενέργειας αλλά ζευγαρώνει ένα από τα t2 . Συνολική ενέργεια (-1,2Δο Ε.Σ.Κ.Π. απόσταθεροποητική Περιλαμβάνει το Cr+2 και το Μn+3
Για μεταλλικά ιόντα με d5 ηλεκτρονιακές απεικονήσεις
Α. me 5 ασύζευκτα ηλεκτρ'ονια (Fe+3, Mn+2) Yψηλού σπιν, παραμαγνητικό
καταλαμβάνει τα τρία t2g τροχιακά και τα δύο τα υψηλής ενέργειας eg αντίστοιχα -6Δο/5 ή συνολική ΕΣΚΠ με συνολική 0Δο
Β. με 1 ασύζευκτο ηλεκτρόνιαο και με συνολική 0Δο Αυτό σημαίνει ότι η σταθεροποίηση ΕΣΚΠ δεν εξαρτάται από τη γεωμετρία του συμπλόκου (πιθανόν να καταλάβει τετραεδρικές ή και οκταεδρικές θέεις
Για μεταλλικά ιόντα με d6 ηλεκτρονιακές απεικονήσεις
A. υπάρχει περίπτωση να ακλουθεί τον Hund me 4 ασύζευκτα ηλεκτρ'ονια Fe+2, Co+3,
B. και υπάρχει περίπτωση να είναι χωρίς ασύζευκτα ηλεκτρ'ονια Ni+4,
Για μεταλλικά ιόντα με d7 ηλεκτρονιακές απεικονίσεις καταλαμβάνει τα τρία t2g τροχιακά και το τέταρτο και πέμπτο ηλεκτρόνιο το eg και το έκτο και έβδομο σε δύο t2gτροχιακά ζευγαρώνει με αντίστοιχες ενέργειες -6Δο/5 ή (-1,2Δο) σταθεροποητική και 2.0,6 Δο ή(1,2Δο) (αποσταθεροποιητική) και -0,8Δο (σταθεροποιητική) με συνολική -0,8Δο σύμφωνα με τον κανόνα του Hund αντίστοιχα ( Ε.Σ.Κ.Π σταθεροποίηση)
Για μεταλλικά ιόντα με d8 ηλεκτρονιακές απεικονίσεις καταλαμβάνει τα τρία t2g τροχιακά και το τέταρτο και πέμπτο ηλεκτρόνιο το eg και το έκτο και έβδομο και όγδοο σε τρία t2gτροχιακά ζευγαρώνει με αντίστοιχες ενέργειες -6Δο/5 ή (-1,2Δο) σταθεροποητική και 2.0,6 Δο ή(1,2Δο) (αποσταθεροποιητική) και -1,2Δο (σταθεροποιητική) με συνολική -1,2Δο σύμφωνα με τον κανόνα του Hund αντίστοιχα ( Ε.Σ.Κ.Π σταθεροποίηση)
Για μεταλλικά ιόντα με d9 ηλεκτρονιακές απεικονίσεις καταλαμβάνει τα τρία t2g τροχιακά και το τέταρτο και πέμπτο ηλεκτρόνιο το eg και το έκτο και έβδομο και όγδοο ζευγαρώνουν σε τρία t2gτροχιακά χαμηλής ενέργειας και το ένατο ζευγαρώνει σε υψηλής ενέργειας eg με αντίστοιχες ενέργειες -6Δο/5 ή (-1,2Δο) σταθεροποητική και 2.0,6 Δο ή(1,2Δο) (αποσταθεροποιητική) και -1,2Δο (σταθεροποιητική) και 0,6Δο με συνολική -0,6Δο σύμφωνα με τον κανόνα του Hund αντίστοιχα ( Ε.Σ.Κ.Π σταθεροποίηση)
Για μεταλλικά ιόντα με d10 ηλεκτρονιακές απεικονήσεις συμπληρώνονται τρία t2g τροχιακά και τα δύο τα υψηλής ενέργειας eg αντίστοιχα -2,4οΔο σταθεροποητική και 2,4Δο (αποσταθεροποιητική) με συνολική 0Δο Αυτό σημαίνει ότι η σταθεροποίηση ΕΣΚΠ δεν εξαρτάται από τη γεωμετρία του συμπλόκου (πιθανόν να καταλάβει τετραεδρικές ή και οκταεδρικές θέεις
TETΑΕΔΡΙΚΑ ΣΥΜΠΛΟΚΑ

Σε τετραεδρικό σύμπλοκο, (;oχι κεντροσυμμετρικό) αντίθετα με το οκταεδρικο, η ενέργεια σταθεροποιείται σε e ηλεκτρόνια κατά 0,6Δt ενώ εάν τοποθετηθεί ηλεκτρόνιο σε t2 θέση αποσταθεροποιείται κατά 0,4Δt
για σύμπλοκα d1 απεικόνιση Το 1 ηλεκτρόνιο στο χαμηλό τροχιαλό η ενέργεια ελαττώνεται κατά ο,4Δο (σταθεροποίηση)
για σύμπλοκο d2 απεικόνιση με 2d ηλεκτρόνια στο t2 η συνολική ενέργεια ελαττώνεται ( - 0,8Δt -σταθεροποίηση)
ομοίως
σύμπλοκο d3 απεικόνιση συνολική ενέργεια ελαττώνεται ( - 0,8Δt -σταθεροποίηση)
σύμπλοκο d4 απεικόνιση συνολική ενέργεια ελαττώνεται ( - 0,4Δt -σταθεροποίηση)
σύμπλοκο d5 απεικόνιση συνολική ενέργεια ελαττώνεται ( 0Δt )
σύμπλοκο d6 απεικόνιση συνολική ενέργεια ελαττώνεται ( - 0,6Δt -σταθεροποίηση)
σύμπλοκο d7 απεικόνιση συνολική ενέργεια ελαττώνεται ( - 1,2Δt -σταθεροποίηση)
σύμπλοκο d8 απεικόνιση ενέργεια ελαττώνεται ( - 0,8Δt -σταθεροποίηση)
σύμπλοκο d9 απεικόνιση συνολική ενέργεια ελαττώνεται ( - 0,4Δt -σταθεροποίηση)
σύμπλοκο d10 απεικόνιση συνολική ενέργεια ( 0Δt )
Συμπληρωματικά για ηλεκτρονιακές απεικονίσεις (δομές) στα σύμπλοκα των στοιχείων μεταπτώσεως
και φασματοσκοπική σειρά των υποκαταστατών φασματοσκοπική σειρά των υποκαταστατών
Αυτό δίνεται από την φασματοσκοπική σειρά των υποκαταστατών: Υποκαταστάτες που προκαλούν απο μικρό Δ προς μεγάλο Δ : I-, Br-, S2-, SCN-, Cl-, NO3-, N3-, F-, OH-, H2O, NCS-, CH3CN-, Pyridini, NH3, αιθυλενοδιαμίνη, 2,2΄διπυριδίνη, phen(1,10)- , NO2, τριφαινυλοφωσφίνη, CN-, CO,
Επίσης υποκαταστάτες ασθενούς : Η2Ο
Υποκαταστάτες ισχυρού πεδίου CO, CN-, NH3, PPh3
Οι αριστεροί υποκαταστάτες (ασθενέστεροι) δεν προκαλούν βίαιη σύζευξη ηλεκτρονίων εντός του d επιπέδου κι έτσι σχηματίζουν εξωτερικά τροχιακά οκταεδρικά σύμπλοκα με υψηλό σπιν.
 Για τον ίδιο λόγο οι υποκαταστάτες στην δεξιά σειρά (ισχυροί) προκαλούν βίαιη σύζευξη τωνd ηλεκτρονίων και ονομάζονται υποκαταστάτες χαμηλού σπιν
Για τον ίδιο λόγο οι υποκαταστάτες στην δεξιά σειρά (ισχυροί) προκαλούν βίαιη σύζευξη τωνd ηλεκτρονίων και ονομάζονται υποκαταστάτες χαμηλού σπιν
Ορισμένα οκταεδρικά σύμπλοκα εμφανίζουν καταστάσεις υψηλού και χαμηλού σπιν σε δυναμική ισορροπία
ΠΑΡΑΜΟΡΦΩΣΗ ΚΡΥΣΤΑΛΛΙΚΩΝ ΓΕΩΜΕΤΡΙΚΩΝ ΠΛΕΓΜΑΤΩΝ
(Τετραγωνική παραμόρφωση)
Με παραμόρφωση από το οκταεδρικό πλέγμα μετά την απομάκρυνση των δύο υποκαταστατών L1 και L6 που εντοπίζονται κατά μήκος του άξονα z στην οκταεδρική συναρμολόγηση προκύπτει επίπεδο τετραγωνικό κρυσταλλικό πλέγμα συμπλόκου.
Η προσέγγιση των υποκαταστατών L1 και L6 στα d τροχιακά του οκταεδρικού ποικίλει σε ισχύ.
Συνήθως παρατηρείται σε d8 σύστημα ισχυρού πεδίου
Π.χ. Ο Pt+2 και Pb+2 που ανήκουν στην 3η και στην 2η σειρά ώστε ο Pt+2 προκαλούν μεγαλύτερη διάσχιση πεδίου. Τα δύο ελεύθερα ηλεκτρόνια δεν μπορούν να σταθεροποιηθούν και ευνοούνται τα επίπεδα τετραγωνικά σύμπλοκα
Στο επίπεδο τετραγωνικό σύμπλοκο τα τροχιακά που χαρακτηρίζονται από z χαρακτήρα dz2, dzx, dzy, δέχονται μειωμένη άπωση από το πεδίο των υποκαταστατών και επομένως σταθεροποιούνται ενεργειακά.
Τριγωνική παραμόρφωση ή παραμόρφωση από περιστροφή
Με παραμόρφωση από το οκταεδρικό πλέγμα μετά την απομάκρυνση ή πλησίασμα δύο αντιδιαμετρικών πλευρών στο κεντρικό άτομο ή ιόν
Ομοίως, οι δύο αντιδιαμετρικές πλευρές μπορεί να περιστραφούν με αντίθετη φορά η μια από την άλλη
Ακόμη, αν υπάρχει ασύμμετρη υποκατάσταση δηλαδή οι υποκαταστάτες δεν είναι όλοι ίδιοι ή αν οι υποκαταστάτες είναι ογκώδεις ή εάν αλληλεπιδρούν μεταξύ τους τότε τα κανονικά γεωμετρικά σχήματα παραμορφώνονται
Παραδείγματα 8εδρων κρυσταλλικών πεδίων που έχουν όμως διαφοροποίηση στην κατανομή των ηλεκτρονίων στα τροχιακά λόγω διαφορετικών υποκαταστατών [PtCl4]-2 και [PtCl2(ΝH3)2]
ΠΗΓΕΣ
Βασικές Αρχές Ανόργανης Χημείας . Γ. ΠΝΕΥΜΑΤΙΚΑΚΗΣ -Χ. ΜΗΤΣΟΠΟΥΛΟΥ -Κ. ΜΕΘΕΝΙΤΗΣ
https://en.wikipedia.org/wiki/Spin_states_(d_electrons)#:~:text=Ionic%20radii.%20The%20spin%20state%20of%20the,given%20d%2Delectron%20count%2C%20high%2Dspin%20complexes%20are%20larger.
https://en.wikipedia.org/wiki/Spectrochemical_series
https://klouras.chem.upatras.gr/attachments/article/32/3.%20GENERAL%20PROPERTIES%20OF%20TRANSITION%20METALS.pdf
https://en.wikipedia.org/wiki/Spin_states_(d_electrons)#:~:text=Ionic%20radii.%20The%20spin%20state%20of%20the,given%20d%2Delectron%20count%2C%20high%2Dspin%20complexes%20are%20larger.
https://en.wikipedia.org/wiki/Spin_states_(d_electrons)#:~:text=Ionic%20radii.%20The%20spin%20state%20of%20the,given%20d%2Delectron%20count%2C%20high%2Dspin%20complexes%20are%20larger.

