Δήμητρα Σπανού, χημικός, συνταξιούχος καθηγήτρια Μέσης Εκπαίδευσης από 30-6-2025
υπό κατασκευή
ΤΕΣΣΕΡΕΣ ΘΕΩΡΙΕΣ ΓΙΑ ΤΗ ΦΥΣΗ ΤΩΝ ΣΥΜΠΛΟΚΩΝ ΕΝΩΣΕΩΝ
Η φύση του χημικού δεσμού (σε απλές όσο και συνθετες ενώσεις) είναι η ίδια και περιγράφεται σε προηγούμενα κεφάλαια.
Στις σύμπλοκες ενώσεις ο βασικός δεσμός είναι αποτέλεσμα της αλληλεπίδρασης ενός κεντρικού ατόμου και άλλων ιόντων ή μορίων που διαθέτουν ένα μη δεσμικό ζεύγος ηλεκτρονίων. Η φύση της αλληλεπίδρασης και του δεσμού εδώ δεν προσδιορίζεται. Βέβαια, ισχύουν οι γενικότερες θεωρίες για τον χημικό δεσμό, όμως αυτές δεν επαρκούν για να ερμηνεύσουν ορισμένες από τις ειδικές ιδιότητες που παρατηρούνται στα σύμπλοκά, όπως, οι μαγνητικές ιδιότητες, το χρώμα τους και ορισμένες θερμοδυναμικές σταθερές τους. Έτσι λοιπόν τροποποιήθηκαν ώστε να είναι πιο αποτελεσματικές στην ερμηνεία της συμπεριφοράς και των ιδιοτήτων των συμπλόκων
Από τις θεωρίες αυτές οι επικρατέστερες είναι:
Η θεωρία του Sidgwick (Werner)ή συντακτική θεωρία που διατυπώθηκει από τον Alfred Werner to 1893
Η θεωρία του δεσμικού σθένους από Linus Pauling το 1930
Η θεωρία του κρυσταλλικού πεδίου από H. Beth κα J. H. Van Vlek 1930
Η θεωρία του πεδίου των υποκαταστατών - Θεωρία των μοριακών τροχιακών J. S. Griffith , L. G. Orgel 1957
Α. Η θεωρία του Sidgwick ή συντακτική θεωρία ((Werner 1893)
Με βάση την θεωρία του Werner και τη θεωρία του Lewis
Για να σχηματιστούν σταθερές σύμπλοκες ενώσεις πρέπει ο αριθμός των ηλεκτρονίων που περιβάλλουν το κεντρικό ιόν στο σύμπλοκο ( που ονομάστηκε δρων ατομικός αριθμός) πρέπει να ισούται με τον ατομικό αριθμό ενός από τα ευγενή αέρια (Kr=36, Xe=54, Rn=86)
Σύμφωνα με αυτή στο κεντρικό άτομο (μέταλλο) συναντάμε δύο σθένη :
Πρωτεύον σθένος: Είναι ο αριθμός οξείδωσης του κεντρικού ιόντος (μετάλλου) π.χ. Co(NH3)6] Cl3 στο εξαμμινοκοβάλτιοΙΙΙ χλωρίδιο έχουμε το Co+3
Στο εξακυανοσιδηρικό ιόν [Fe(CN)6 ] 4- το πρωτεύον σθένος του σιδήρου είναι +2 ( Fe +2) Στο τετραυδροξοχρυσικό κάλιο Κ[Au(OH)4] το πρωτεύον σθένος του χρυσού είναι +3 (Au+3)
Δευτερεύον σθένος: Λέγεται και αριθμός ένταξης. Είναι ο αριθμός των ομοιοπολικών δεσμών που σχηματίζει γύρω του (με μόρια ή ιόντα) το μέταλλο. Στο εξαμμινοκοβάλτιοΙΙΙ χλωρίδιο Co(NH3)6] Cl3 είναι 6 Στο εξακυανοσιδηρικό χλωρίδιο επίσης είναι 6 [Fe(CN)6 ] 4- Στο τετραυδροξοχρυσικό κάλιο Κ[Au(OH)4]
Πρωτεύων δεσμός Ετεροπολικός δεσμός μεταξύ του κεντρικού ατόμου (μετάλλου) με το θετι κό φορτίο που αντισταθμίζεται με τα αρνητικά ιόντα. Στο Co(NH3)6] Cl3 Στο εξαμμινοκοβάκτιοΙΙΙ χλωρίδιο είναι μεταξύ Co και ανιόντων χλωρίου. Στο εξακυανοσιδηρικό IΙΙ θειϊκό
[Fe(CN)6 ]2(SO4)3 είναι μεταξύ του Fe+3 και των θειϊκών ανιόντων (SO4)-2 Στο τετραυδροξοχρυσικό κάλιο Κ[Au(OH)4] είναι μεταξύ του Αu+3 και των κατιόντων Καλίου
Δευτερεύων δεσμός: όπου μόρια και ιόντα συνδέονται απευθείας με το μεταλλικό ιόν
Τα δευτερεύοντα σθένη έχουν συγκεκριμένη κατεύθυνση κι έτσι προκύπτει μια καθορισμένη γεωμετρία
π.χ. για το κοβάλτιο :
στo εξαμμινοκοβάλτιοΙΙΙ χλωρικό , το κοβάλτιο με αριθμό οξείδωσης +3, [Co(NH3)6]3+ συνδέεται με το άζωτο της αμμωνίας που έχει ασύζευκτο ζεύγος ηλεκτρονίων και έχουμε οκταεδρική διαμόρφωση
στο εξαυδατοκοβάλτιο ιόν, [Co(H2O)6 ] +2 με αριθμό οξείδωσης κοβαλτίου +2, συνδέεται με το οξυγόνο του νερού που έχει ασύζευκτο ζεύγος ηλεκτρονίων
Στο τετραυδροξοχρυσικό* κάλιο Κ[Au(OH)4] με αριθμό οξείδωσης χρυσου +3 συνδέεται με το οξυγόνο του
* Η κατάληξη ικος δίνεται λόγω αρνητικού φορτίου του συμπλόκου
Ο ΚΑΝΟΝΑΣ ΤΩΝ ΟΚΤΩ ΗΛΕΚΤΡΟΝΙΩΝ
Εδώ ο Sidwick διατύπωσε τον κανόνα των 18 ηλεκτρονίων
Για να σχηματιστούν σταθερές σύμπλοκες ενώσεις πρέπει ο αριθμός των ηλεκτρονίων που περιβάλλουν το κεντρικό άτομο που ονομάστηκε (δρων ατομικός αριθμός) να ισούται με τον ατομικό αριθμό ενός από τα ευγενή αέρια (Kr=36, Xe=54, Rn=86)
Από αυτό προκύπτει και η γεωμετρία του συμπλόκου
με αριθμός ένταξης 6
Στο σύμπλοκο [Co(NH3)6]3+ το Co έχει ατομικό αριθμο 27 άρα το σύμπλοκο έχει 24e-. Η κάθε NH3 δρα ως δότης ζεύγους ηλεκτρονίων. Τα 6 μόρια αμμωνίας που περιβάλλουν το κεντρικό ιόν δίνουν σύνολο 6.2=12 ηλεκτρόνια. Τα συνολικά ηλεκτρόνια γύρω από το ιόν κοβαλτίου είναι 36 ηλεκτρόνια που είναι ο ατομικός αριθμός του Κρυπτού
με αριθμό ένταξης 4
Στο σύμπλοκο [Ag(NH3)4]+ ο Άργυρος έχει ατομικό αριθμο 47 άρα το σύμπλοκο έχει 46 e-. Η κάθε NH3 δρα ως δότης ζεύγους ηλεκτρονίων. Τα 4 μόρια αμμωνίας που περιβάλλουν το κεντρικό ιόν δίνουν σύνολο 4.2=8 ηλεκτρόνια. Τα συνολικά ηλεκτρόνια γύρω από το ιόν κοβαλτίου είναι 54 ηλεκτρόνια που είναι ο ατομικός αριθμός του Ξένου
Β. Η θεωρία του δεσμού σθένους Linus Pauling 1930
σ δεσμοί που το ζεύγος των ηλεκτρονίων προέρχεται μόνο από τον υποκαταστάτη δηλαδή το ένα από τα δύο άτομα του δεσμού (δοτικός ομοιοπολικός -παλιά ημιπολικός) και επομένως δρουν σαν βάσεις Lewis****
Η θεωρία δεσμού σθένους βασίστηκε στις διατυπώσεις του Lewis περί σύζευξης ηλεκτρονίων, στηρίζεται στην θεωρία του υβριδισμού* (κεφ 4Β)που αναπτύχθηκε για την ερμηνεία του χημικού δεσμού αλλά διατυπώθηκε από τον Pauling.
Σύμφωνα με αυτήν
α. στο μέταλλο- κεντρικό άτομο του συμπλόκου υβριδοποιούνται ορισμένα ατομικά τροχιακά **
Παράδειγμα: Η ηλεκτρονική δομή του Co είναι [Ar] 3d74s2 → το Co3+ θα έχει δομή [Ar] 3d6
Τα συζευγμένα ηλεκτρόνια και να καταλαμβάνουν μόνο τα 1 από τα 5 της ενεργειακής στοιβάδας 3d
β. ο τύπος του δεσμού των υποκαταστατών με το κεντρικό μέταλλο εξαρτάται από την φύση των υποκαταστατών: αν οι υποκαταστάτες είναι ισχυροί δότες ηλεκτρονίων έχει κυρίως ομοιοπολικό χαρακτήρα***, (ομοιοπολικά σύμπλοκα)
Ο αριθμός των ασύζευκτων ηλεκτρονίων μειώνεται από 4 σε 0
: [Co(CN)6]3+ (διαμαγνητικό) το υποκαταστάτης το κυάνιο πολύ ισχυρός υποκαταστάτης, άρα, θα πρέπει να είναι συζευγμένα τα ηλεκτρόνια στο κοβάλτιο, θα καταλαμβάνουν τώρα στην ενεργειακή υποστοιβάδα 3d τα 3 από τα 5
Οι ομοιοπολικοί δεσμοί με τους συνδέτες (κυάνια) θα καταλαμβάνουν στα στην 4s ενεργειακή υποστοιβάδα ένα από τα 1s τροχιακό και στην 4p ενεργειακή υποστοιβάδα και 3 από τα 3p τροχιακά και 4d ενεργειακή υποστοιβάδα 2 τροχιακά από τα 5 d2sp3
αν έχουμε ασθενείς δότες ηλεκτρονίων κυρίως ιοντικός (ιοντικά σύμπλοκα)
ηλεκτρονική δομή του Co είναι [Ar] 3d74s2 → το Co3+ θα έχει δομή [Ar] 3d6
Τα συζευγμένα ηλεκτρόνια και να καταλαμβάνουν μόνο τα 1 από τα 5 της ενεργειακής στοιβάδας 3d
Παράδειγμα 2: [CoF6]3- (παραμαγνητικό) Το F είναι ασθενής υποκταστάτης
Ο αριθμός των ασύζευκτων ηλεκτρονίων του κοβαλτίου παραμένει ίδιος
Οι ομοιοπολικοί δεσμοί με τους συνδέτες (ιόντα φθορίου) θα καταλαμβάνουν στα 3d ενεργειακή υποστοιβάδα 2 τροχιακά από τα 5 στην 4s ενεργειακή υποστοιβάδα ένα από τα 1s τροχιακό και στην 4p ενεργειακή υποστοιβάδα και 3 από τα 3p τροχιακά sp3d2
Ακόμα
Ο αριθμός των ομοιοπολικών δεσμών στους οποίους μπορεί να συμμετέχει το άτομο με συνεισφορά ηλεκτρονίων του εξαρτάται από τον αριθμό ηλεκτρονίων σθένους έτσι ώστε όλα τα επίπεδα της εξωτερικής στοιβάδας να είναι συμπληρωμένα (Για τον άνθρακα με 4 μονήρη ηλεκτρόνια είναι 4 δεσμοί για το άζωτο με 5 ηλεκτρόνια σθένους εκ των οποίων τα 3 μονήρη είναι 3 δεσμοί που θα δώσουν δομή ευγενούς αερίου, ενώ το οξυγόνο με 6 ηλεκτρόνια εκ των οποίων τα 2 μονήρη, 2 δεσμούς) Ηλεκτρόνια σθένους που δεν συμμετέχουν στον σχηματισμό δεσμών ονομάζονται μονήρη.
Σε ομοιοπολικούς δεσμούς στους οποίους μπορεί να συμμετέχουν υποκαταστάτες που περιέχουν μη δεσμικό ζεύγος ηλεκτρονίων αρκεί να υπάρχει συμμετρία και ενέργεια τροχιακών (ατομικών ή μοριακών) με κενά τροχιακά του μετάλλου
Από τον συνδυασμό αυτόν προκύπτουν σ δεσμοί που το ζεύγος των ηλεκτρονίων προέρχεται μόνο από τον υποκαταστάτη δηλαδή το ένα από τα δύο άτομα του δεσμού (δοτικός ομοιοπολικός -παλιά ημιπολικός) και επομένως δρουν σαν βάσεις Lewis****
Αυτή η θεωρία περιγράφει καλά τις στερεοχημικές δομές των συμπλόκων και επίσης ερμηνεύει τις μετρήσεις των μαγνητικών ιδιοτήτων τους
Όμως η θεωρία αυτή δεν συμπεριλαμβάνει τις διεγερμένες καταστάσεις κι έτσι δεν μπορεί να ερμηνεύσει τα ηλεκτρονιακά φάσματα απορρόφησης υπεριώδους και ορατού και το χρώμα που είναι χαρακτηριστική ιδιότητα των συμπλόκων
.
ΥΒΡΙΔΟΠΟΙΗΣΗ ΤΡΟΧΙΑΚΩΝ ΜΕΤΑΛΛΟΙΟΝΤΟΣ ΚΑΙ ΑΡΙΘΜΟΣ ΕΝΤΑΞΗΣ ΥΠΟΚΑΤΑΣΤΑΤΩΝ ΣΥΜΠΛΟΚΟΥ

. Παραδείγματα υβριδισμού στο μεταλλοιόν είναι οι dsp2, dsp3, d2sp3
Τα υβριδικά τροχιακά χρησιμοποιούνται από το μεταλλοϊόν
Ο αριθμός των υποκαταστατών (ένταξης ή σύνταξης) είναι ίσος με αυτόν τον αριθμό των υβριδοποιημένων
Η γεωμετρία στον χώρο εξαρτάται από τον αριθμό ένταξης και την φύση των υποκαταστατών. Έχουμε:
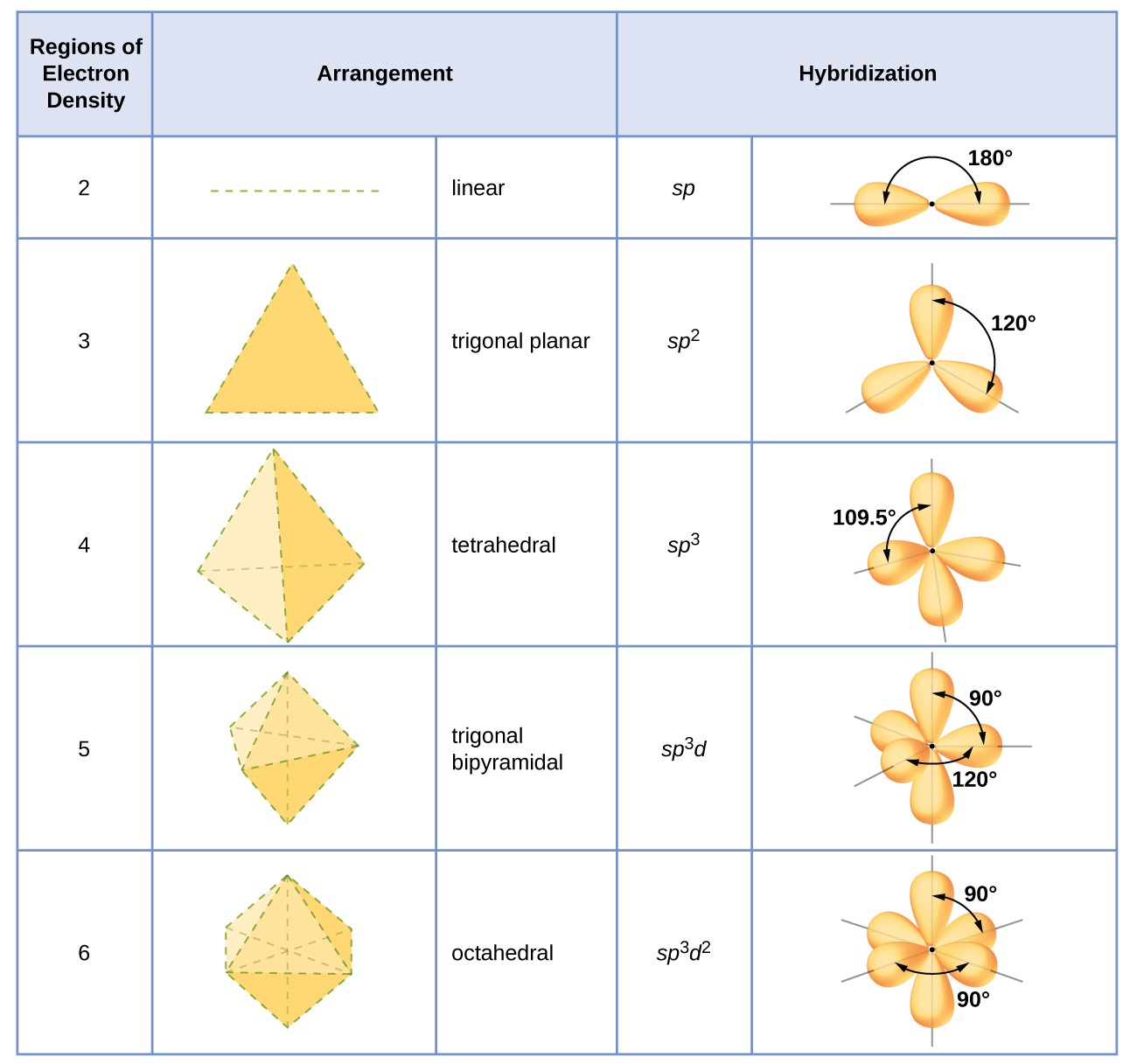
Οκταεδρική δομή των συμπλόκων με αριθμό σύνταξης 6
Στην σύνδεση του κεντρικού ατόμου (μετάλλου συνήθως) τα τροχιακά που συμμετέχουν είναι αμιγώς τροχιακά συνήθως d ή s ή p από n και n-1 στοιβάδα
Τα τροχιακά όμως των υποκαταστατών είναι υβριδοποιημένα. (υψηλού spin)
Παραδείγματα: υβριδισμός sp3d2
υβριδισμός d2sp3
Παραδείγματα οκταεδρικών συμπλόκων
Για το σύμπλοκο εξαυδατοσίδηρος [Fe(H2O)6 ] +2 ΙΙ Ο υβρiδισμός εξωτερικής στοιβάδας για dn (χρησιμοποιούνται d τροχιακά της εξωτερικής στοιβάδας) με τον υποκαταστάτη είναι sp3d2. (4s, 4px, 4py, 4pz, 4dx2y2, 4dz2 με τον μέγιστο αριθμό ασύζευκτων ηλεκτρονίων Το σύμπλοκο είναι παραμαγνητικό εξωτερικής σφαίρας και υψηλού spin
Για To σύμπλοκο εξακυανοσιδηρικό [Fe(CN)6 ] 4- ΙΙ με υβριδισμό d (n-1) όπου χρησιμοποιούνται d τροχιακά της εσωτερικής στοιβάδας, είναι d2sp3 ( 3dx2y2, 3dz2 , 4s, 4px, 4py, 4pz )που έχουν συνήθως λιγότερα ασύζευκτα ηλεκτρόνια (χαμηλού spin) . Το Σύμπλοκο είναι διαμαγνητικό εσωτερικής σφαίρας και χαμηλού spin.
Τα υβριδοποιημένα τροχιακά και στις δύο περιπτώσεις κατευθύνονται στις κορυφές ενός οκτάεδρου
Τετραεδρική ή τετραγωνική δομή με αριθμό σύνταξης 4
Η τετραεδρική βρίσκεται συνήθως σε ιόντα μετάλλων μεταπτώσεως d0 ή d10 .
Σε τετράεδρο, απαιτούμενος υβριδισμός του κεντρικοού ιόντος: ο sp3 ή ο dsp2. Στο επίπεδο τετραγωνικό σε d8 μέταλλα, ειδικά πλατινοειδή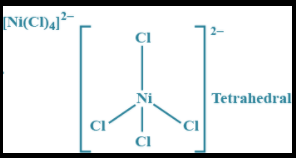
Παραδείγματα:
τετράεδρο
Το σύμπλοκο τετραχλωρονικελικό ιόν [ΝiCl4]-2 υβρυδισμός sp3 ( 4s και 4px , 4py , 4pz ). Τα τέσσερα υβριδικά τροχιακά κατευθύνονται στις κορυφές τετραέδρου. Το Cl- είναι ασθενής υποκαταστάτης έτσι υπάρχουν 2 αζευγάρωτα ηλεκτρόνια στα 3d τροχιακά. Είναι παραμαγνητικό, έλκεται από μαγνητικό πεδίο
επίπεδο τετραγωνικό
Το σύμπλοκο τετρακυανονικελικό ιόν [Νi(CΝ)4]-2 Υβριδισμός dsp2 Το CN- είναι ισχυρός υποκαταστάτης και αναγκάζει όλα τα ηλεκτρόνια να ζευγαρώνουν. Είναι διαμαγνητικό, δεν έχει ελεύθερα ηλεκτρόνια
Τα τέσσερα υβριδικά τροχιακά κατευθύνονται στις κορυφές τετραγώνου.
Το σύμπλοκο τετραχλωρολευκοχρυσικό ιόν [PtCl4]-2 υβριδισμός dsp2( 5dx2y2, 6s, 6px, 6py ). Τα τέσσερα υβριδικά τροχιακά κατευθύνονται στις κορυφές τετραγώνου. Είναι διαμαγνητικό.
Το σύμπλοκο τετραμμινοχαλκόςΙΙ ιόν [Cu(NH3)4]2+ . Υβριδισμός dsp2 ( 3dx2y2, 4s, 4px, 4py) έχουν επίπεδη συμμετρία και κατευθύνονται προς τις κορυφές τετραγώνου. Σε στερεή κατάσταση
Γραμμικά σύμπλοκα Αριθμός σύνταξης 2
Παραδείγματα:
Δικυανοαργυρικό ιόν [Ag(CN)2]
Υβριδικά τροχιακά από ανάμειξη 4dz και 5s μικρής διαφοράς ενέργειας. Τα ηλεκτρόνια που τα καταλαμβάνουν ήταν στο 4dz2
Γραμμικά σύμπλοκα Αριθμός σύνταξης 9 και άνω
ενΒρίσκονται σε λανθανίδες και ακτινίδες λόγω των μεγάλων ατομικών ακτίνων τους
ΣΥΜΠΛΗΡΩΜΑΤΙΚΑ: ΣΗΜΑΝΤΙΚΆ ΣΗΜΕΙΑ ΓΙΑ ΤΗΝ ΘΕΩΡΙΑ ΔΕΣΜΙΚΟΥ ΣΘΕΝΟΥΣ*****
Σημείωση1 Στην θεωρία δεσμού σθένους έχει γίνει η παραδοχή πως τα ηλεκτρόνια των δεσμών προσφέρουν αποκλειστικά οι υποκαταστάτες
Σημείωση2 : Αρχή της ηλεκτροουδετερότητας: Σύμφωνα με εισήγηση του Paulin, η μέγιστη σταθερότητα των ενώσεων ένταξης επιτυγχάνεται όταν η ηλεκτραρνητικότητα των ατόμων- δοτών είναι αρκετή για να πετύχει ουδέτερο φορτίο για το μέταλλο.
Σημείωση 3 Αύξηση σταθερότητας συμπλόκου με την υπαρξη π δεσμού π. Σε ορισμένα σύμπλοκα εκτός από τους σ-δεσμούς ένταξης δημιουργούνται κατ' εξαίρεση και π-δεσμοί. Σε αυτό συμβάλλουν, 1.
(μπορεί να πραγματοποιηθεί, αρκεί να είναι εφικτές "δομές συντονισμού" για τον δεσμό μετάλλου- υποκαταστάτη με τον οποίες απεντοπίζεται η ηλεκτρονιακή πυκνότητα του δεσμού. Οι δεσμοί αυτοί πρααγματοποιούνται
1 μέσω π επανασύνδεσης με όρους μεσομέριας και σύμφωνα με τον κανόνα των 18 ηλεκτρονίων
. π-αλληλοκάλυψης ενός d τροχιακού του μεταλλοϊόντος και ενός κενού τροχιακού του υποκαταστάτη κατάλληλης συμμετρίας
Πρέπει να υπάρχουν μέταλλα σε χαμηλή οξειδωτική κατάσταση που λόγω δέσμευσης σ προσδεμάτων έχει υπερβολικό φορτίο και να γίνει σύνδεση 
αυτών των μετάλλων με υποκαταστάτες χαμηλής ηλεκτραρνητικότητας CΟ, ΝΟ2, ΝΟ, CN. Παράδειγμα το τετρακαρβονύλιο νικελίου Ni(CO)4
Δεσμός σίγμα (αριστερά), σε σύγκριση με την επανασύνδεση π (δεξιά).
.
2. π δεσμός επαναφοράς
μέσω π-αλληλοκάλυψης ενός d τροχιακού του μεταλλοϊόντος υψηλής οξειδωτικής βαθμίδας (5ης και 6ης περιόδου) και ενός d τροχιακού του υποκαταστάτη . H αλληλοκάλυψη επιτυγχάνεται με την συμμετοχή 2 λοβών και δημιουργείται π δεσμός επαναφοράς. Υποκαταστάτες μπορεί να είναι PF3, PR3, AsR3, SR .
3 μέσω π-αλληλοκάλυψης κενού d τροχιακού του μεταλλοϊόντος (4ης περιόδου) και ενός d τροχιακού του υποκαταστάτη πλούσιου σε ηλεκτρόνια (F-, Cl-, OH-. NH2-). Επιτυγχάνεται με την πλευρική αλληλοκάλυψη κατειλημένων P τροχιακών του υποκαταστάτη και κενών d τροχιακών του κεντρικού ιόντος.
Άλλες δυο περιπτώσεις π δεσμών είναι ο π-δοτικός δεσμός ενώσεων που παρατηρείται περίσσεια ηλεκτρονιακού νέφους και οι π δέκτες που συμβαίνουν ανάμεσα σε υποκαταστάτες με π τροχιακά και μονήρη ζεύγη ηλεκτρονίων
Σημείωση 4 Οι μαγνητικές ιδιότητες του συμπλόκου σχετίζονται με τον αριθμό των ασύζευκτων ηλεκτρονίων.
ΕΞΗΓΗΣΗ ΜΑΓΝΗΤΙΚΩΝ ΙΔΙΟΤΗΤΩΝ
.jpeg)
Παρατηρείται ότι η συμπεριφορά των συμπλόκων μετάλλων ως προς τις μαγνητικές τους ιδιότητες είναι πολλές φορές διαφορετική απο αυτήν του μεταλλοιόντος. Παράδειγμα: Ενώ τα μεταλλοϊόντα PdΙΙ καιNiII έιναι παραμαγνητικά, πολλά από τα σύμπλοκά τους είναι διαμαγνητικά

Τα παραμαγνητικό υλικό έχουν θετική μαγνητική δεκτικότητα.
(Μαγνητική δεκτικότητα είναι ο λόγος της Μαγνήτισης προς την Ένταση του Μαγνητικού πεδίου και οι τιμές της κυμαίνονται από -1 έως άπειρο. 
Αυτό συμβαίνει γιατί τα στοιχεία αυτά διαθέτουν μονήρη ηλεκτρόνια που αυξάνουν την μαγνητική ροπή. (βλέπε το ιόν Νικέλιο και την ηλεκτρονιακή διάταξη στο σχήμα)
Εάν τα υλικά έχουν όμως μ< 0,25 (όπως το Νικέλιο) μπορούν να καταταγούν στα παραμαγνητικά στοιχεία
τα σύμπλοκά τους όπως τετρακυανονικελικό ιόν [Νi(CΝ)4]-2 δεν έχουν ελεύθερα ηλεκτρόνια, είναι διαμαγνητικά
Αντίθετα, στο άλλο σύμπλοκο του νικελίου το τετραχλωρονικελικό ιόν [ΝiCl4]-2 με υβρυδισμός sp3 ( 4s και 4px , 4py , 4dz ). , το Cl- είναι ασθενής υποκαταστάτης έτσι υπάρχουν 2 αζευγάρωτα ηλεκτρόνια στα 3d τροχιακά. Είναι παραμαγνητικό, έλκεται από μαγνητικό πεδίο
Σημείωση: Εάν κατά την κατασκευή της σύνθετης ένωσης, δημιουργούνται ισχυρά πεδία, τα μεταλλικά ιόντα παραβιάζουν τον νομο του Hund στην τοποθέτηση ηλεκτρονίων στα τροχιακά προκειμένου να κερδίσουν ενέργεια και να ξεπεράσουν την υψηλή ενέργεια πεδίου (από το μέταλλο ή από τους υποκαταστάτες). Έτσι με την δημιουργία ζευγών σε χαμηλής ενέργειας τροχιακά, αφ' ενός κερδίζουν ενέργεια λόγω χαμηλού τροχιακού, αφ' ετ'ερου προστίθεται η επίπλέον ενέργεια σύνδεσης Ρ λόγω των ζευγών ηλεκτρονίων που δημιουργούνται στα τροχιακά
- Συνολική ενέργεια = Ε.Σ.Κ.Π. +Ρ
**Υβριδοποιημενα τροχιακά στις σύμπλοκες ενώσεις (ενώσεις ένταξης)
Πως δημιουργείται η σύμπλοκος ένωση
Η πλήρωση των κενών υβριδικών τροχιακών του μεταλλοϊόντος που ο αριθμός τους είναι ίσος με τον αριθμό των ατομικών του τροχιακών που λαμβάνουν μέρος στον υβριδισμό, επιτυγχάνεται μέσω του σχηματισμού δοτικών ομοιοπολικών δεσμών μεταξύ υποκαταστατών και κεντρικού ιόντος αφού ο κάθε υποκαταστάτης προσφέρει ένα ζεύγος ηλεκτρονίων στο μεταλλοιόν.
***Ο σχματισμός ομοιοπολικού δεσμού προϋποθέτει την προσέγγιση δύο ατόμων έτσι ώστε να προκύψει αλληλοεπικάλυψη των ατομικών τροχιακών και ο δεσμός είναι ισχυρότερος για μεγαλύτερη αλληλοεπικάλυψη. Τα ηλεκτρόνια έλκονται από τους πυρήνες και των δύο ατόμων
****Έτσι, η θεωρία δεσμού σθένους καθορίζει το μεταλλοιόν ως οξύ κατά Lewis και τους υποκαταστάτες από τους οποίους προέρχονται τα ηλεκτρόνια των ομοιοπολικών δεσμών ένταξης, σαν βάσεις κατά Lewis.
 (1).jpg)
Δήμητρα Σπανού
ΠΗΓΕΣ
Βασικές Αρχές Ανόργανης Χημείας . Γ. ΠΝΕΥΜΑΤΙΚΑΚΗΣ -Χ. ΜΗΤΣΟΠΟΥΛΟΥ -Κ. ΜΕΘΕΝΙΤΗΣ
https://en.wikipedia.org/wiki/Tetrachloronickelate#:~:text=Near%20room%20temperature%2C%20these%20salts,consisting%20of%20octahedral%20Ni%20centers.
ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ - ΟΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ ΚΑΙ ΤΑ ΤΡΟΧΙΑΚΑ | PDF
https://dlefkad.blogspot.com/2017/02/blog-post.html
https://klouras.chem.upatras.gr/attachments/article/30/10.%20CRYSTAL%20FIELD%20THEORY%28PPP%29.pdf
https://en.wikipedia.org/wiki/Crystal_field_theory#:~:text=The%20most%20common%20type%20of%20complex%20is,the%20latter%20and%20therefore%20experiences%20less%20repulsion.
https://courses.lumenlearning.com/suny-mcc-chemistryformajors-1/chapter/hybrid-atomic-orbitals/
file:///C:/Users/user/Downloads/100576_ΑΣΗΜΑΚΟΠΟΥΛΟΣ_
Η ΧΗΜΕΙΑ ΠΕΡΙΓΡΑΦΕΙ ΤΗΝ ΥΛΗ ΜΕ ΤΟΝ ΗΛΕΚΤΡΙΣΜΟ ΚΑΙ ΤΟΝ ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΣΜΟ: 6ο μέρος. Υλικά σιδηρομαγνητικά, διαμαγνητικά, παράμαγνητικά και οι ατομικές μαγνητικές ροπές τους
