Δήμητρα Σπανού, χημικός, συνταξιούχος καθηγήτρια Μέσης Εκπαίδευσης από 30-6-2025
ΤΕΣΣΕΡΕΣ ΘΕΩΡΙΕΣ ΓΙΑ ΤΗ ΦΥΣΗ ΤΩΝ ΣΥΜΠΛΟΚΩΝ ΕΝΩΣΕΩΝ
Η φύση του χημικού δεσμού (σε απλές όσο και συνθετες ενώσεις) είναι η ίδια και περιγράφεται σε προηγούμενα κεφάλαια.
Στις σύμπλοκες ενώσεις ο βασικός δεσμός είναι αποτέλεσμα της αλληλεπίδρασης ενός κεντρικού ατόμου και άλλων ιόντων ή μορίων που διαθέτουν ένα μη δεσμικό ζεύγος ηλεκτρονίων. Η φύση της αλληλεπίδρασης και του δεσμού εδώ δεν προσδιορίζεται. Βέβαια, ισχύουν οι γενικότερες θεωρίες για τον χημικό δεσμό, όμως αυτές δεν επαρκούν για να ερμηνεύσουν ορισμένες από τις ειδικές ιδιότητες που παρατηρούνται στα σύμπλοκά, όπως, οι μαγνητικές ιδιότητες, το χρώμα τους και ορισμένες θερμοδυναμικές σταθερές τους. Έτσι λοιπόν τροποποιήθηκαν ώστε να είναι πιο αποτελεσματικές στην ερμηνεία της συμπεριφοράς και των ιδιοτήτων των συμπλόκων
Από τις θεωρίες αυτές οι επικρατέστερες είναι:
Η θεωρία του Sidgwick (Werner)ή συντακτική θεωρία που διατυπώθηκει από τον Alfred Werner to 1893
Η θεωρία του δεσμικού σθένους από Linus Pauling το 1930
Η θεωρία του κρυσταλλικού πεδίου από H. Beth κα J. H. Van Vlek 1950
Η θεωρία του πεδίου των υποκαταστατών - Θεωρία των μοριακών τροχιακών J. S. Griffith , L. G. Orgel 1957
Δ Η θεωρία του συνδέτη
Είναι μια ανάπτυξη της θεωρίας κρυσταλλικού πεδίου που λαμβάνει υπ' όψην και την Θεωρία δεσμού σθένους .
Εδώ λαμβάνεται υπ' όψη την αλληλεπίδραση των τροχιακών του κεντρικού ιόντος με τα τροχιακά των υποκαταστατών. Σε αντίθεση με την θεωρία κρυσταλλικού πεδίου, οι συνδέτες δεν θεωρούνται σημειακά φορτία και λαμβάνεται υπ' όψη η φύση του χημικού δεσμού και οι επικαλύψεις τροχιακών.
Από τα d ατομικά τροχιακά ενός μεταβατικού του μετάλλου d τομέα
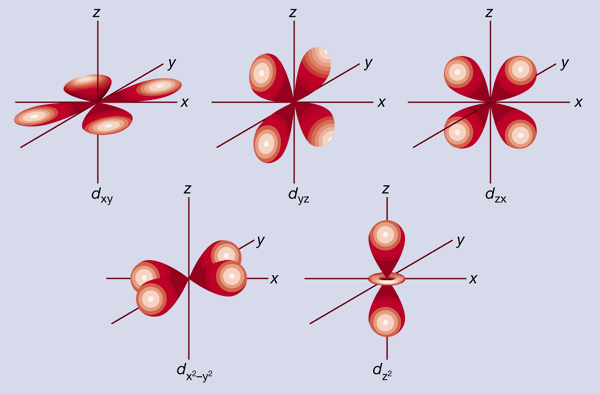
επικαλυπτόμενα με τροχιακα υποκαταστατών
Τα τρία (d-xy, d-xz, d-yz )ανάμεσα στους άξονες και τα δύο dx2-y2, dz2 πάνω στους άξονες
Τα 5 αυτά τροχιακά σε οκταεδρικό πεδίο υφίστανται Απόσχιση (Άρση εκφυλισμού)
με διαφορά ενέργειας e και t2 την Ενέργεια Διαχωρισμού την 10Dq
η Ενέργεια κατανέμεται :
Τα t2g (d-xy, d-xz, d-yz) ενδιαμέσως των αξόνων, 'εχουν λιγότερη επίδραση με υποκαταστάτες ενώ τα e-g (dz2, dx2-y2 )είναι έντονα
Τα t2g είναι τα d-xy, d-xz, d-yz, d τροχιακά που έχουν κέντρο συμμετρίας και η ενέργειά τους είναι μειωμένη κα τά 2/5 Δο για κάθε ηλεκτρόνιο επομένως σταθεροποιείται
Τα e-g είναι τα dz2, dx2-y2 d τροχιακά που έχουν έχουν κέντρο συμμετρίας και η ενέργειά τους είναι αυξημένη κατά 3/5 Δο για κάθε ηλεκτρόνιο επομένως αποσταθεροποιείται
Τα διάφορα d τροχιακά επιρρεάζονται διαφορετικά από ένα γειτονικό πεδίο υποκαταστατώνι η ενέργειά τους αυξάνεται ή μειώνεται πράγμα που επιδρά στην δημιουργία συμπλόκων καθώς και στην γεωμετρική δομή τους
H ενεργειακή απόσταση μεταξύ των ομάδων ονομάζεται παράμετρος διαχωρισμού
Το μέγεθος αυτής εξαρτάται από τη φύση του μετάλλου, το φορτίο του συμπλόκου, τον τύπο των υποκαταστατών και τη θέση τους στην φασματοσκοπική σειρά.
Η βασική ιδέα είναι ότι η αλληλεπίδραση συμβαίνει μεταξύ των τροχιακών του συνδέτη (πληρωμένων ή κενών) με τα d, s, και p τροχιακά του κεντρικού ατόμου.
Η θεωρία του πεδίου των υποκαταστατών - Θεωρία των μοριακών τροχιακών J. S. Griffith , L. G. Orgel 1957΄
ΜΟΡΙΑΚΑ ΤΡΟΧΙΑΚΑ ΘΕΩΡΙΑ ΠΕΔΙΟΥ ΣΥΝΔΕΤΗ
Το αποτέλεσμα της σύνδεσης υποκαταστατών στο μέταλλο , είναι νέα μοριακά τροχιακά που η κατανομή τους καθορίζει την ηλεκτρονική δομή του συμπλόκου ιόντος, το οποίο θεωρείται πλέον σαν σύνολο ατόμων στο οποίο υπάρχουν διακριτές ενεργειακές καταστάσεις μεμονωμένων ηλεκτρονίων (μοριακά τροχιακά). Τα μοριακά τροχιακά είναι πολύκεντρα, δηλαδή μοιράζονται τροχιακά για περισσότερους από έναν ατομικούς πυρήμες. Εδώ έχουμε: μετάλλου + πυρήνες ομάδων υποκαταστατών.
Ανάλογα με την συμμετρία του συμπλόκου το μοριακό τροχιακό έχει διαφορετική εμφάνιση (ανάλογη με τις γεωμετρικές δομές στην θεωρία του κρυσταλλικού πεδίου).
H επικάλυψη είναι εφικτή εφόσον τα επικαλυπτόμενα τροχιακά έχουν παραπλήσιες ενέργειες, περίπου ίδια συμμετρία και σχετικά μικρή απόσταση ώστε να γίνει η επικάλυψη
ΑΚΟΜΑ ΤΙ ΠΡΕΠΕΙ ΝΑ ΘΥΜΟΜΑΣΤΕ ΓΙΑ ΤΑ ΜΟΡΙΑΚΑ ΤΡΟΧΙΑΚΑ
Κάθε μοριακό τροχιακό μπορεί να έχει ένα ή δύο (αντιπαράλληλου σπιν) ή κανένα ηλεκτρόνιο.
Τα μοριακά αυτά χωρίζονται σε
δεσμευτικά ή δεσμικά (ίδιας φάσης), μη δεσμευτικά και χαλαρωτικά (αντίθετης φάσης )
Δεσμικό μοριακό τροχιακό ΒΜΟ είναι το μοριακό που συγκεντρώνει τη μέγιστη ηλεκτρονιακή πυκνότητα ανάμεσα στους πυρήνες των συνδεόμενων ατόμων (σταθεροποίηση)
Αντιδεσμικό μοριακό τροχιακό (χαλαρωτικό)* ΑΜΟ είναι το μοριακό που συγκεντρώνει τη μέγιστη ηλεκτρονιακή πυκνότητα ανάμεσα στους πυρήνες των συνδεόμενων ατόμων (αποσταθεροποίηση)
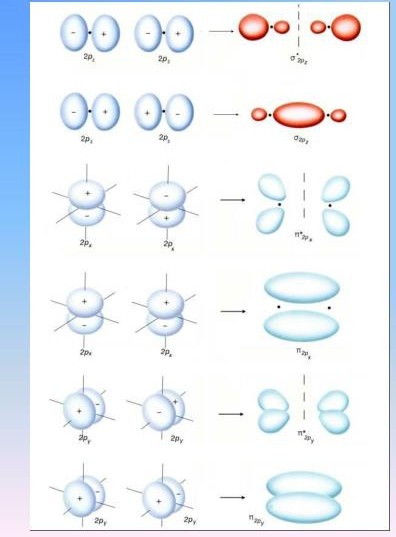

Συμμετρικά τροχιακά η κυματοσυνάρτηση δεν αλλάζει πρόσημο κατά την αναστροφή τους ως προς το κέντρο του μορίου
Αντισυμμετρικά τροχιακά η κυματοσυνάρτηση αλλάζει πρόσημο κατά την αναστροφή τους ως προς το κέντρο του μορίου
.jpg)
Τα μοριακά τροχιακά μπορεί να γίνουν με διαφορετικό προσανατολισμό. Έτσι διακρίνουμε
Μοριακές συνδέσεις σ, π, δ. και φ
με σύνδεση σ: Αν τα άτοιμα τροχιακά συνδεθούν για να δώσουν το μοριακο τροχιακό στον άξονα των πυρήνων τους με επικάλυψη ατομικών τροχιακών όπως: s+s, s+p, s+d, pz+pz, dz2+dz2
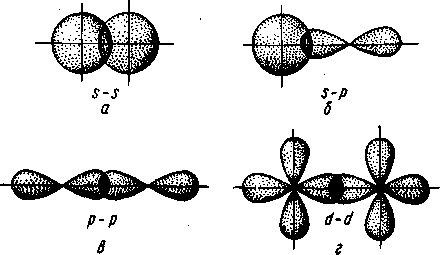

![Molecular Orbital (M. O.) diagram for hexaaquatitanium(III) [Ti(H2O)6]3 ...](https://image.slidesharecdn.com/molecularorbitalsdiagramsoftih2o631-201028041326/85/Molecular-Orbital-M-O-diagram-for-hexaaquatitanium-III-Ti-H2O-6-3-2-320.jpg) Από το Τιτάνιο με σ δεσμούς για να συνδεθούν με το νερό είναι τα 3dx2-y2, 3dz2, 4s, 4px, 4py, 4pz
Από το Τιτάνιο με σ δεσμούς για να συνδεθούν με το νερό είναι τα 3dx2-y2, 3dz2, 4s, 4px, 4py, 4pz με σύνδεση π: Υπάρχουν υποκαταστάτες ( F-, CL-, Br- OH-S2-. O2-) που μπορούν να συνδεθούν με το μέταλλο μέσω π δεσμικών μοριακών δεσμών (σε φάση) ή αντιδεσμικών π* (αντίθετης φάσης) με ηλεκτρόνια κατάλληλου προσανατολισμού και ενέργειας σε μοριακο τροχιακό. Από το μεταλλικό ιόν κατάλληλα είναι τα ατομικά τροχιακά dxy, dxz, dyx
 Διακρίνουμε στο σχήμα αριστερά τα μοριακά τροχιακά ενός απλού μορίου ΝΟ σ και π μοριακά
Διακρίνουμε στο σχήμα αριστερά τα μοριακά τροχιακά ενός απλού μορίου ΝΟ σ και π μοριακά
η επικάλυψη ατομικών τροχιακών γίνεται με πλευρική (παράλληλη) επικάλυψη ατομικών τροχιακών όπως: py+py, px+px, px+dxz, dyz+dyz
Υποκαατάτες π δότες ηλεκτρονίων L->M και υποκαταστάτες π δέκτες M->L
 ΟΙ π δεσμο΄M->L με οπιστοσύνδεση: γίνονται όταν έχουμε υποκαταστάτες με κενά τροχιακά κατάλληλης συμμετρίας (π*) για σχηματισμό π δεσμών που ενεργειακά βρίσκονται πιο ψηλά από τα τροχιακά t2g (dxy, dxz, dyz) του μετάλλου. Έτσι σχηματίζεται σετ t2g μοριακών τροχιακών από t2g δεσμικά τροχιακά χαμηλότερα σε ενέργεια από τα αρχικά και από αντιδεσμικά t2g*
ΟΙ π δεσμο΄M->L με οπιστοσύνδεση: γίνονται όταν έχουμε υποκαταστάτες με κενά τροχιακά κατάλληλης συμμετρίας (π*) για σχηματισμό π δεσμών που ενεργειακά βρίσκονται πιο ψηλά από τα τροχιακά t2g (dxy, dxz, dyz) του μετάλλου. Έτσι σχηματίζεται σετ t2g μοριακών τροχιακών από t2g δεσμικά τροχιακά χαμηλότερα σε ενέργεια από τα αρχικά και από αντιδεσμικά t2g*Τροχιακά μοριακά και ενέργεια
Τα μοριακά τροχιακά που προηγούνται στην δημιουργία μορίου είναι αυτά της χαμηλότερης ενέργειας: παράδειγμα :
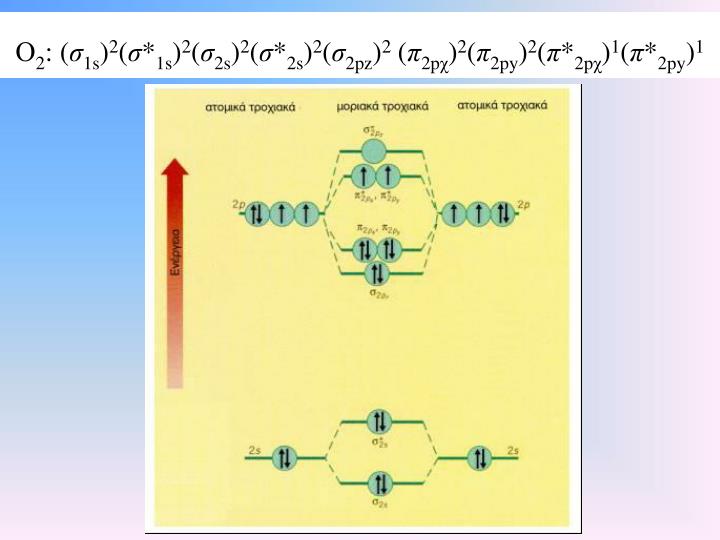

Θα μπορούσαμε ακόμα να δούμε πως συνδυάζονται τα ατομικά τροχιακά δύο μορίων οξυγόνου για να δώσουν τα μοριακά τροχιακά του διατομικού μορίου του οξυγόνου
Τα τροχιακά εκτός δέσμευσης βρίσκονται σε πολύ υψηλότερες ενέργειες
Η διάταξη των τροχιακών στο μέταλλικό ιόν εξαρτάται και από την ενέργεια του υποκααστάτη που ανάλογα με την ισχύ του επιρρεάζει την διάταξη των τροχιακών του μετάλλου.
Μπορούμε να χωρίσουμε τους υποκαταστάτες ανάλογα του μοριακού τροχιακού
1. Υποκαταστάτες ασθενούς πεδίου: I-, Br-, S-2, SCN-, F-, Cl-, OH-, οξαλικά, Ο2-, Η2Ο Προκαλούν μικρό διαχωρισμό Δ Σχηματίζουν π δεσμούς οπιστοσυνθεσης Μ->L
2. Υποκαταστάτες ενδιάμεσου πεδίου Η2Ο, ΝΗ3, διπυριδίνη, δεν σχηματίζουν π δεσμούς
3. Υποκαταστάτες ισχυρού πεδίου ΝΟ2-, PPh3, CN-,CO ,CO-2 Προκαλούν μεγάλο διαχωρισμό Δ Σχηματίζουν ενώσεις χαμηλού σπιν. Σχηματίζουν π δεσμούς L->M
Δεν οδηγούν όλοι οι συνδυασμοί σε μοριακά τροχιακά
Ο συνδυασμός px +py δεν οδηγεί σε δεσμό
Ο συνδυασμός px + s δε οδηγεί σε δεσμό
Ο συνδυασμός pz+ s οδηγεί σε δεσμό των τροχιακών και επιτρέπει την μέγιστη επικάλυψή τους.
Παραδείγματα μοριακών τροχιακών σε σύμπλοκα
Η θεωρία του πεδίου υποκαταστατών δίνει απαντήση στην δημιουργία συμπλόκων ενώσεων με την θεωρία των μοριακών τροχιακών. Θεωρεί ότι για την δημιουργία μοριακών τροχιακά από τα ατομικά τροχιακά σθένους του μετάλλου και τα τροχιακά σθένους των υποκαταστατών. σημαντικός παράγοντας
Η μέθοδος των μοριακών τροχιακών που εφαρμόζεται στις ενώσεις συντονισμού ονομάζεται θεωρία πεδίου συδέτη
Ένα ιόν μεταβατικού μετάλλου έχει εννέα ατομικά τροχιακά:
πέντε από n -d , ένα (n+1)s και τρία (n+1)p τροχιακά
Tetraeder.jpg)
Tetraeder.jpg)
Tertaeder.jpg)
Tetraeder.jpg)
Tertaeder.jpg)
Αυτά έχουν κατάλληλη ενέργεια για να σχηματίσουν δεσμούς αλληλεπίδρασης με υποκαταστάτες.
.jpg)
Η ευχαιρέστερη γεωμετρία για σταθεροποίηση είναι το
Οκταεδρικό σύμπλοκο με έξη υποκαταστάτες.
Τα οκταεδρικά σύμπλοκα σχηματίζονται κυρίως από συνδυασμό s, p και d(eg) τροχιακά του κεντρικού ατόμου με σ τροχιακά των υποκαταστατών
Τα d τροχιακά διασπώνται σε t2g και eg
Ας δούμε αναλυτικότερα:
τον οκταεδρικό συντονισμό με Διάσχιση (διάσπαση υβριδοποιημένων τροχιακών με ενέργεια διαχωρισμού Δo 10Dq) σε τροχιακά χαμηλότερης ενέργειας (t2g =dxy, dxz, dyz) και υψηλότερης ενέργειας (eg=dz2, dx2-y2)
Η Δο για οκταεδρικό σύμπλοκο κυμαίνεται από 5000cm-1 έως 30000cm-1. Αυτό αντιστοιχεί σε ενέργεια από -25 έως -350 kj
Εδώ σε ένα οκταεδρικό σύμπλοκο συμμετάχουν τα έξη ατομικά τροχιακά του συνδέτη (Μέταλλο Μ)
συνδυάζονται με 6 (μοριακά ή ατομικά )τροχιακά υποκαταστατών που είναι καθένα από αυτά μπορεί να επικαλύπτεται με ένα από τα 6 τροχιακά του μετάλλου
Οι συνδέσεις μπορεί να είναι σ ή π

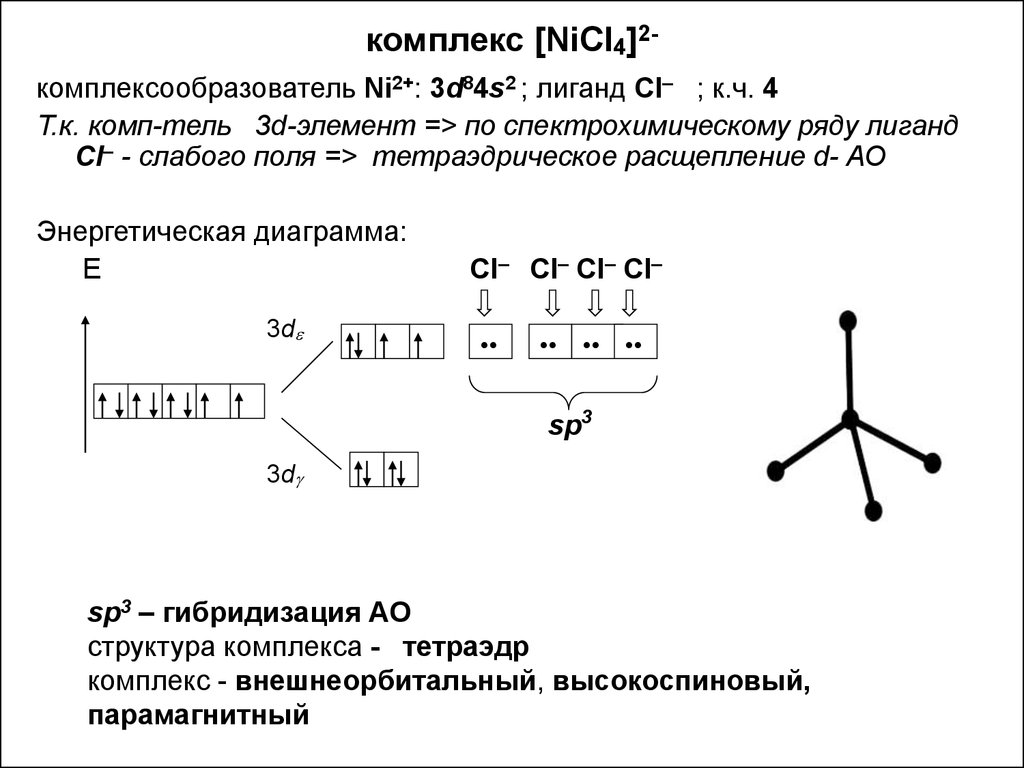
τον τετραεδρικό συντονισμό με π συνδέσεις
Διάσχιση αντίθετη του οκταεδρικού με υψηλότερα ενεργειακά τροχιακά (t2 =dxy, dxz, dyz) και χαμηλής ενέργειας (e = dxy, dxz, dyz). Η διαφορά στην ενέργεια Δt μεταξύ των e και t2 ατομικών τροχιακών του μετάλλου σε τετραεδρικό πεδίο (ενέργεια
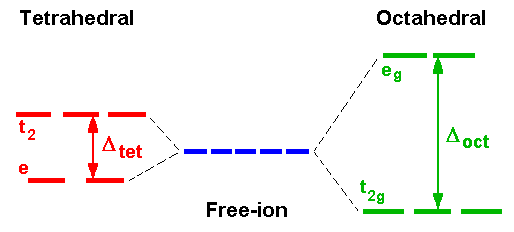
διαχωρισμού) είναι μικρότερη από τα
αντίστοιχα οκταεδρικά ίδιου μετάλλου
Συνεπώς η ενέργεια διαχωρισμού Δt στα τετραεδρικά σύμπλοκα δεν είναι αρκετά μεγάλη και έτσι σε ενώσεις ένταξης τετραέδρου, οι καταστάσεις συνήθως ειναι υψηλού σπιιν . Από υπολογισμούς η απόσταση μετάλλου υποαταστάτη για τα ίδια μεταλλοιόνται είναι: Δtetr = 4/9Δοkt (όχι μεγάλη)
π.x.[Co(NH3)6]2+ ->. Δο = 10200cm-1 και .[Co(NH3)4]2+ ->. Δο = 5900cm-1

τον επίπεδο τετραγωνικό συντονισμό 4]-2.jpg) που δημιουργεί ισχυρή διάσπαση Δt Θεωρείται ότι προέρχεται από αντίστοιχα στα οποία το dx2-y2 γίνεται υψηλότερο σε ενέργεια και δεν χρησιμοποιείται Το επίπεδο τετραγωνικό σύμπλοκο, είναι χαμηλής ενέργειας πιο χαμηλής και από το τετράεδρο και είναι συμμετρικό ( t2g).
που δημιουργεί ισχυρή διάσπαση Δt Θεωρείται ότι προέρχεται από αντίστοιχα στα οποία το dx2-y2 γίνεται υψηλότερο σε ενέργεια και δεν χρησιμοποιείται Το επίπεδο τετραγωνικό σύμπλοκο, είναι χαμηλής ενέργειας πιο χαμηλής και από το τετράεδρο και είναι συμμετρικό ( t2g).
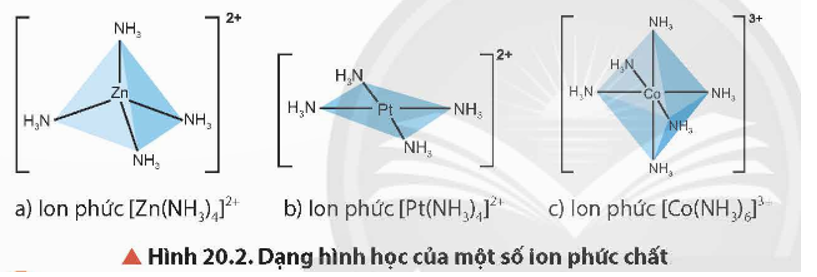 Τα ενεργειακά τροχιακά που το συνθέτουν το επίπεδο τετραγωνικό με t2g είναι : τα dxz, dyz, τα αμέσως υψηλότερης (dz2) και το τελευταίο πιο υψηλής (dxy)
Τα ενεργειακά τροχιακά που το συνθέτουν το επίπεδο τετραγωνικό με t2g είναι : τα dxz, dyz, τα αμέσως υψηλότερης (dz2) και το τελευταίο πιο υψηλής (dxy)
τα υψηλότερης ενέργειας dx2-y2 όπως διαμορφώνονται σε οκταεδρικό σύμπλοκο παραμένει κενό
Η σταθεροποιητική επίδραση μέσω της δημιουργίας μοριακών τροχιακών που ασκείται από τους υποκαταστάτες (ενώσεις ένταξης) στοχεύει στα τροχιακά υψηλής ενέργειας dx2-y2
Τα τροχιακά εκτός δέσμευσης βρίσκονται σε πολύ υψηλότερες ενέργειες


Μαγνητικές ιδιότητες
Η θεωρία του πεδίο συνδέτη - θεωρία του πεδίου των υποκαταστατών ερμηνεύει επίσης τις μαγνητικές ιδιότητες των ενώσεων αυτών βάσει των τιμών των παραμέτρων διαχωρισμού και του αριθμού των συζευγμένων και ασύζευκτων ηλεκτρονίων.
Με ασθενές πεδίο συνδέτη με μικρή τιμή ενέργειας διαχωρισμού Δ τα ηλεκτρόνια παραμένουν ασύζευκτα και αυτό οδηγεί σε σύμπλοκο παραμαγνητικό.
διαγράμματα διάταξης ηλεκτρονίων στην d3
Με ισχυρό πεδδίο συνδέτη με μικρή τιμή ενέργειας διαχωρισμού Δ τα ηλεκτρόνια παραμένουν ασύζευκτα και αυτό οδηγεί σε σύμπλοκο παραμαγνητικό.
Η διάταξη των τροχιακών του μετάλλου εξαρτάται και η διαμόρφωση ισχυρού ή ασθενούς πεδίου εξαρτάται και από την ενέργεια του υποκααστάτη που ανάλογα με την ισχύ του επιρρεάζει την διαμόρφωση των τροχιακών.
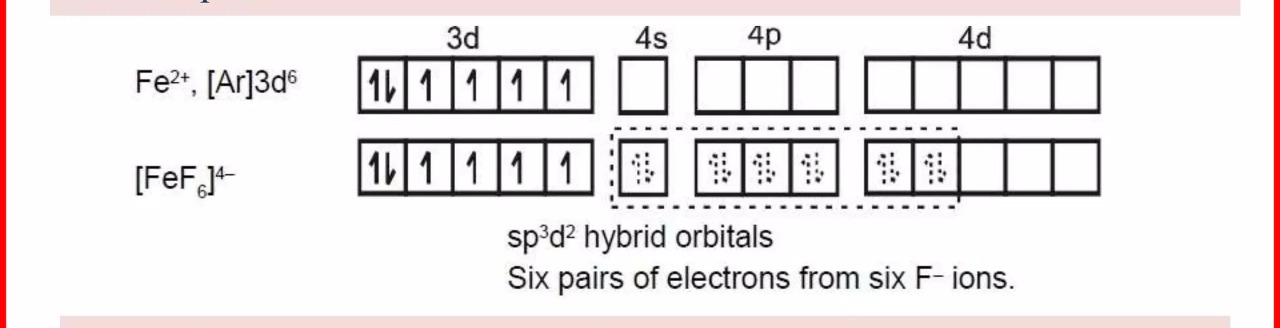
Παράδειγμα το εξαφθοροσίδηρικό ιόν και το εξακυανοσιδηρικό ιόν όπως δείχνει το σχεδιάγραμμα κάτω έχουν διαφορετική διάταξη τροχιακών στο μέταλλο που οφείλεται στην επίδραση του ασθενούς f-
Ισχυροί υποκαταστάτες όπως το κυάνιο δημιουργούν ένα χαμηλό spin στο πεδίο του μετάλλου και είναι διαμαγνητικά, αντίθετα ασθενείς (F-) υψηλό σπιν και είναι παραμαγνητικά
Σημείωση: Εάν κατά την κατασκευή της σύνθετης ένωσης, δημιουργούνται ισχυρά πεδία, τα μεταλλικά ιόντα παραβιάζουν τον νομο του Hund στην τοποθέτηση ηλεκτρονίων στα τροχιακά προκειμένου να κερδίσουν ενέργεια και να ξεπεράσουν την υψηλή ενέργεια πεδίου (από το μέταλλο ή από τους υποκαταστάτες). Έτσι με την δημιουργία ζευγών σε χαμηλής ενέργειας τροχιακά, αφ' ενός κερδίζουν ενέργεια λόγω χαμηλού τροχιακού, αφ' ετ'ερου προστίθεται η επίπλέον ενέργεια σύνδεσης Ρ λόγω των ζευγών ηλεκτρονίων που δημιουργούνται στα τροχιακά. Έτσι,
Ισχυρά πεδία οδηγούν σε μεγάλη διάσπαση και αντίθετα ταα ασθενή. Τα τροχιακά είνουν να καταλαμβάνουν τροχιακά χαμηλής ενέργειας

Ιστορία τους
Οι J. S. Griffith , L. G. Orgel χρησιμοποίησαν τις ηλεκτροστατικές αρχές από τη θεωρία του κρυσταλλικού πεδίου για να εξηγήσουν αλληλεπιδράσεις μετάλλου- υποκαταστάτη που οδηγούν σε σταθεροποίηση του κρυσταλλικού πεδίου.
Αυτή η μέθοδος είναι ικανή για να εξηγήσει την γεωμετρία των συμπλόκων, τις μαγνητικές και φασματοσκοπικές και καταλυτικές τους ιδιότητες.
τα ατομικά τροχιακά είναι δυνατόν να επικαλύπτονται με ατομικά τροχιακά υποκαταστατών με βάση την συμμετρία τους που εξαρτάται από τη γεωμετρία του συμπλόκου
Spectrochemical Series High Spin Low Spin
Η ΕΝΝΟΙΑ ΤΟΥ ΥΒΡΙΔΙΣΜΟΥ ΑΤΟΜΙΚΩΝ ΤΡΟΧΙΑΚΩΝ ΑΠΟ ΔΙΑΦΟΡΕΤΙΚΑ ΑΤΟΜΑ
που προτάθηκε από τον Αμερικανό Χημικό Linus Pauling για να εξηγήσει τα τροχιακά σθένους πολύπλοκων
μορίων στα οποία, αν και η ενέργεια αυτών στο κεντρικό άτομο υπολογίζονταν αρχικά διαφορετική, σχημάτιζαν δεσμούς ισοδύναμους (σε σύνδεση με ίδιους προσδέτες) . Ισχύει για τα d ατομικά τροχιακά!


