Δήμητρα Σπανού, χημικός, συνταξιούχος καθηγήτρια Μέσης Εκπαίδευσης από 30-6-2025
υπό κατασκευή
ΤΕΣΣΕΡΕΣ ΘΕΩΡΙΕΣ ΓΙΑ ΤΗ ΦΥΣΗ ΤΩΝ ΣΥΜΠΛΟΚΩΝ ΕΝΩΣΕΩΝ
Η φύση του χημικού δεσμού (σε απλές όσο και συνθετες ενώσεις) είναι η ίδια και περιγράφεται σε προηγούμενα κεφάλαια.
Στις σύμπλοκες ενώσεις ο βασικός δεσμός είναι αποτέλεσμα της αλληλεπίδρασης ενός κεντρικού ατόμου και άλλων ιόντων ή μορίων που διαθέτουν ένα μη δεσμικό ζεύγος ηλεκτρονίων. Η φύση της αλληλεπίδρασης και του δεσμού εδώ δεν προσδιορίζεται. Βέβαια, ισχύουν οι γενικότερες θεωρίες για τον χημικό δεσμό, όμως αυτές δεν επαρκούν για να ερμηνεύσουν ορισμένες από τις ειδικές ιδιότητες που παρατηρούνται στα σύμπλοκά, όπως, οι μαγνητικές ιδιότητες, το χρώμα τους και ορισμένες θερμοδυναμικές σταθερές τους. Έτσι λοιπόν τροποποιήθηκαν ώστε να είναι πιο αποτελεσματικές στην ερμηνεία της συμπεριφοράς και των ιδιοτήτων των συμπλόκων
Από τις θεωρίες αυτές οι επικρατέστερες είναι:
Η θεωρία του Sidgwick (Werner)ή συντακτική θεωρία που διατυπώθηκει από τον Alfred Werner to 1893
Η θεωρία του δεσμικού σθένους από Linus Pauling το 1930
Η θεωρία του κρυσταλλικού πεδίου από H. Beth κα J. H. Van Vlek 1950
Η θεωρία του πεδίου των υποκαταστατών - Θεωρία των μοριακών τροχιακών J. S. Griffith , L. G. Orgel 1957
συνέχεια από 2Β μέρος
Γ. Η θεωρία του κρυσταλλικού πεδίου H. Beth κα J. H. Van Vlek1950
Με την θεωρία αυτή ερμηνεύεται η δομή των συμπλόκων ενώσεων με όρους ανάλογους με την ερμηνεία της κρυσταλλικής δομής των ενώσεων.
Η θεωρία των κρυστάλλων, όπως επεκτάθηκε και στα σύμπλοκα εφαρμόστηκε με επιτυχία για την ερμηνεία ηλεκτρονικών ιδιοτήτων τους.
Εδώ θεωρείται ότι η δημιουργία συμπλόκων είναι αποτέλεσμα ηλεκτροστατικών δυνάμεων που αναπτύσσονται μεταξύ του κεντρικού ιόντος και των υποκαταστατών κυρίως αρνητικά φορτισμένων. Είναι δυνάμεις ελκτικές αλλά και απωστικές των αρνητικά φορτισμένων ηλεκτρονίων του κεντρικού ατόμου και των υποκαταστατών. Στα σύμπλοκα, οι υποκαταστάτες φορτισμένοι ή ουδέτεροι διευθετούνται γύρω από το κεντρικό ιόν όπως και στους κρυσταλλους
ΕΡΜΗΝΕΙΑ ΤΗΣ ΘΕΩΡΙΑΣ ΚΡΥΣΤΑΛΛΙΚΟΥ ΠΕΔΙΟΥ
Μεγάλη σημασία σ' αυτήν την θεωρία έχει η επίδραση των απώσεων αυτών στα d τροχιακά του κεντρικού ατόμου .
Αυτό ερμηνεύεται ως εξής: Σε όλα τα στοιχεία μεταπτώσεως το άτομο στην αέρια φάση έχει όλα τα d τροχιακά ενεργειακά ισότιμα (εκφυλισμένα).
Η θεωρία λέει πως όταν το άτομο ή ιόν αυτό βρεθεί μέσα σε ένα σφαιρικό ηλεκτρικό πεδίο (που παράγεται λόγω των ομοιόμορφα κατανεμημένων ηλεκτρονίων του υποκαταστάτη) η ενέργειά των d τροχιακών του ανυψώνεται αλλά ο εκφυλισμός τους διατηρείται.
Λόγω του ότι το εξωτερικό πεδίο όμως δεν είναι ακριβώς σφαιρικό και τα σημειακά φορτία των υποκαταστατών βρίσκονται σε συγκεκριμένες θέσεις στον χώρο, τα d τροχιακά του κεντρικού ατόμου- ιόντος υφίστανται διαφορετικά την επίδραση του εξωτερικού πεδίου των υποκαταστατών, άρα παύουν να είναι ενεργειακά ισότιμα, οπότε τα ηλεκτρόνια δεν έχουν πια την ίδια πιθανότητα να βρεθούν σε ένα οποιοδήποτε από αυτά 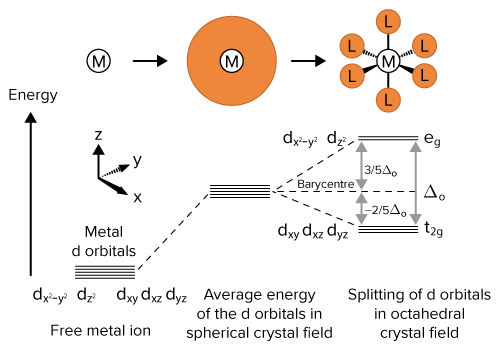
Έτσι κάποια από τα ηλεκτρόνια των d τροχιακών προωθούνται σε θέσεις μικρότερης επίδρασης από το πεδίο και χαμηλότερης ενέργειας t2g ενώ άλλα προωθούνται σε θέσεις με μεγαλύτερη επίδραση από το πεδίο των υποκαταστατών, υψηλότερη ενέργεια τα eg
Η ΕΝΕΡΓΕΙΑ ΔΙΑΧΩΡΙΣΜΟΥ Δο ή Dq
Η διαφορά ενέργειας eg και t2g ονομάζεται Ενέργεια διαχωρισμού κρυσταλλικού πεδίου Συμβολίζεατι με Δο (Ενέργεια σχάσης κρυσταλλικού πεδίου)
Εξαρτάται
- Οξειδωτική κατάσταση μετάλλοιόντος: Υψηλές οξειδωτικές καταστάσεις του μετάλλου οδηγούν σε σύμπλοκα μεγαλύτερης Δο.
- Φύση του μεταλλοιόντος (Γεωμετρία. Ατομικός αριθμός: στην ίδια περίοδο με την αύξηση ΑΑ, έχουμε μείωση του Δ, ενώ στην ίδια ομάδα με αύξηση του ΑΑ έχουμε αύξηση Δ)
- Φύση του υποκαταστάτη. Αύξηση των τιμών του Δ ανάλογα με την φασματοσκοπική σειρά
Η ΙΣΧΥΣ ΤΩΝ ΥΠΟΚΑΤΑΣΤΑΤΩΝ ΦΑΣΜΑΤΟΣΚΟΠΙΚΗ ΣΕΙΡΑ
Οι υποκαταστάτες χωρίζονται σε τρεις κατηγορίες
1. Υποκαταστάτες ασθενούς πεδίου: I-, Br-, S-2, SCN-, F-, Cl-, OH-, Προκαλούν μικρό διαχωρισμό Δ Σχηματίζουν ενώσεις υψηλού σπιν
Όσο μικρότερο είναι το μέγεθος του υποκαταστάτη (μέγεθος: Ι->Br-> Cl-> F-), τόσο ευκολότερα πλησιάζει το μεταλλικό κέντρο με απωστική δύναμη ισχυρότερη.
2. Υποκαταστάτες ενδιάμεσου πεδίου Η2Ο, ΝΗ3, διπυριδίνη,
3. Υποκαταστάτες ισχυρού πεδίου ΝΟ2-, PPh3, CN-, ,CO-2 Προκαλούν μεγάλο διαχωρισμό Δ Σχηματίζουν ενώσεις χαμηλού σπιν. Οι υποκαταστάτες εδώ έχουν αυξανόμενη ικανότητα κα "κόβουν" τα d τροχιακόαπό αριστερά προς τα ξεξιά
ΕΝΕΡΓΕΙΑ ΣΤΑΘΕΡΟΠΟΙΗΣΗΣ ΤΟΥ ΚΡΥΣΤΑΛΛΙΚΟΥ ΠΕΔΙΟΥ
Η Σταθεροποίηση του κρυσταλλικού πεδίου του συμπλόκου εξαρτάται από Ενέργεια Σταθεροποίησης Κρυσταλλικού Πεδίου, που είναι η διαφορά της ενέργειάς του σε σχέση με ένα σφαιρικό πεδίο που υποθέσαμε αρχικά στο οποίο τα ηλεκτρονία του υποκαταστάτη θα ήταν όμοια κατανεμημένα.
Η Ενέργεια Σταθεροποίησης Κρυσταλλικού Πεδίου (ΕΣΚΠ) ορίζεται η απόλυτη τιμή του αθροίσματος των ενεργειών όλων των ηλεκτρονίων που βρίσκονται στα τροχιακά d σε σχέση με το κέντρο βάρους. Τα eg ηλεκτρόνια αποσταθεροποιούν γιατί καθένα έχει αυξημένη ενέργεια κατά 3/5 Δο, ενώ τα t2g σταθεροποιούν έχει μειωμένη ενέργεια κατά -2/5Δο
. ΕΣΚΠ =[- (nt2g . 2/5Δο ) + neg . 3/5Δο)
Κάτι άλλο που παίζει ρόλο είναι η ενέργεια σύζευξης Ρ (ενέργεια που απαιτείται για βρεθούν δύο ηλεκτρόνια με αντιπαράλληλο σπιν στο ίδιο τροχιακό -γέμισμα)
Δ>Ρ
Αν η συνολική ενέργεια Δο όλων των ηλεκτρονίων από την δημιουργία t2g και eg τροχιακών είναι μεγαλύτερη από την ενέργεια σύζευξης Ρ (Δο>Ρ) δημιουργούνται ισχυρά πεδία με γεμάτα τροχιακά λίγα αζύζευκτα ηλεκτρόνια και χαμηλο σπιν π.χ. το σύμπλοκο [Fe(CN)6]3- με ένα ασύζευκτο ηλεκτρόνιο έχει ισχυρό πεδίο υποκαταστατών (CN-) και είναι διαμαγνητικό
Δ<Ρ
Αν η συνολική ενέργεια Δο όλων των ηλεκτρονίων από την δημιουργία t2g και eg τροχιακών είναι μικρότερη από την ενέργεια σύζευξης Ρ (Δο<Ρ) δημιουργούνται ασθενή πεδία με αζύζευκτα ηλεκτρόνια και υψηλό σπιν π.χ. Το σύμπλοκο [Fe(H2O)6]3+ , έχει 5 ασύζευκτα ηλεκτρόνια, με υψηλο σπιν γιατί το πεδίο των υποκαταστατών Η2Ο) είναι ασθενές και είναι παραμαγνητικό
 Οκταεδρικό Σύμολοκο: Αριθμός ένταξης 6
Οκταεδρικό Σύμολοκο: Αριθμός ένταξης 6
 Κεντρικό ιόν συνήθως είναι μέταλλα στην οξειδωτική βαθμίδα +3 όπως κοβάλτιο και χρώμιο και εμφανίζονται σε 2 ισομερείς μορφές cis και trans.
Κεντρικό ιόν συνήθως είναι μέταλλα στην οξειδωτική βαθμίδα +3 όπως κοβάλτιο και χρώμιο και εμφανίζονται σε 2 ισομερείς μορφές cis και trans.
και περιβάλλεται από 6 υποκαταστάτες τοποθετημένους σε καρτεσιανούς άξονες συντεταγμένων με διαφοροποίηση έτσι της ενέργειάς τους.
Έτσι το οκταεδρικό πεδίο των υποκαταστατών επιδρά διαφορετικά στα ηλεκτρόνια d τροχιακών του κεντρικού ατόμου
Από τα 5d τροχιακά έχουμε:
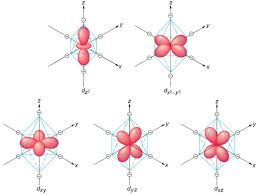
τα eg Είναι 2 πάνω στους άξονες τα dx2y2 καί dz2 .Μεγάλη απώθηση, μεγαλύτερη επίδραση στα ηλεκτρόνια από το πεδίο των υποκαταστατών, υψηλότερη ενέργεια από αυτή του σφαιρικού πεδίου
τα t2g Είναι 3 που στρέφονται ανάμεσα στους άξονες στις διαγώνιές τους και είναι μικρότερης επίδρασης από το πεδίο των υποκαταστατών και χαμηλότερης ενέργειας ναπό αυτήν του σφαιρικού πεδίου
Παραδείγματα δυο 8εδρων κρυσταλλικών πεδίων που έχουν όμως διαφοροποίηση στην κατανομή των ηλεκτρονίων στα τροχιακά λόγω διαφορετικών υποκαταστατών
Διάγραμμα κρυσταλλικού πεδίου με χαμηλό σπιν
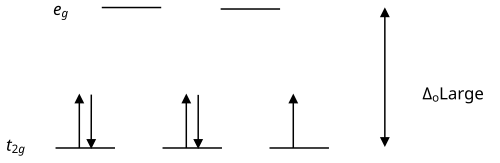
[Fe(NO2 ) 6 ] 3−και οι υποκαταστάτες προκαλούν ισχυρό πεδίο και μεγάλη διάσπαση Δ των d τροχιακών. Έτσι, αφού η τοποθέτηση των υψηλής ενέργειας ΝΟ2 σε υψηλότερα τροχιακά κοστίζει ενεργειακά περισσότερο γίνεται η τοποθέτησή τους στα tg τροχιακά, παρ' όλο που αυτά είναι ήδη κατειλημένα και δημιουργούνται απώσεις ¨εχουμε 1 μόνο αζύζευκτο ηλεκτρόνιο άρα χαμηλό σπιν
![Molecular Orbital (M. O.) diagram for hexaaquatitanium(III) [Ti(H2O)6]3+ | PPTX](https://image.slidesharecdn.com/molecularorbitalsdiagramsoftih2o631-201028041326/75/Molecular-Orbital-M-O-diagram-for-hexaaquatitanium-III-Ti-H2O-6-3-2-2048.jpg)
Διάγραμμα κρυσταλλικού πεδίου με υψηλό σπιν 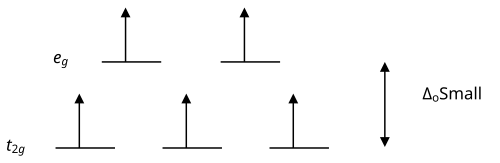
[FeBr6 ]3− , οι υποκαταστάτες προκαλούν μικρή διάσπαση Δ των d τροχιακών
Έτσι, η τοποθέτηση των χαμηλής ενέργειας Br- γίνεται κανονικά με την τοποθέτησή τους σε υψηλότερα τροχιακά εφόσον δεν έχουμε υπερβολικό ενεργειακό κόστος. Τελικά μένουν
και 5 ασύζευκτα ηλεκτρόνια (υψηλό σπιν) Ομοίως στο [Ti(H2O)6]+3
Τετραεδρικό σύμπλοκο αριθμός ένταξης 4
Η τοποθέτηση τωνν υποκαταστατών ως προς το καρτεσιανό σύστημα συντςταγμένων είναι διαφορετική από το οκτάεδρο.
Στο τετραεδρικό οι υποκαταστάτες δεν προσεγγίζουν άμεσα κανένα από τα 5 τροχιακά. Όμως βρίσκονται πιο κοντα στα τροχιακά dxy, dxz, dyz, από ότι στα dx2-y2 και dz2 .
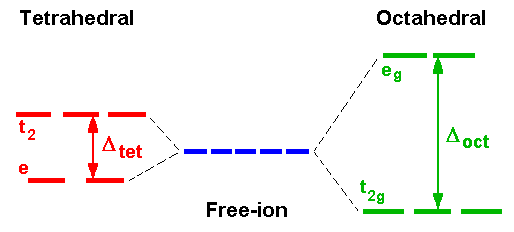 Τα τριπλά εκφυλισμένα τροχιακά dxy, dxz, dzy επιρεάζονται περισσότερο από το τετραεδρικό πεδίο των υποκαταστατών με συνέπεια τώρα τα t2 να είναι ανυψωμένα ενεργειακά. . αντί για τα eg που ήταν στο οκτάεδρο.
Τα τριπλά εκφυλισμένα τροχιακά dxy, dxz, dzy επιρεάζονται περισσότερο από το τετραεδρικό πεδίο των υποκαταστατών με συνέπεια τώρα τα t2 να είναι ανυψωμένα ενεργειακά. . αντί για τα eg που ήταν στο οκτάεδρο.
Αντίθετα τα ηλεκτρόνια των διπλά εκφυλισμένων eg την οποία αποτελούν τα τροχιακά dz2 και dx2-y2 ,δέχονται σε μικρότερο βαθμό την επίδραση των υποκαταστατών.
Συνεπώς η ενέργεια διαχωρισμού στα τετραεδρικά σύμπλοκαδεν δεν είναι αρκετά μεγάλη και έτσι σε ενώσεις ένταξης τετραέδρου, οι καταστάσεις συνήθως ειναι υψηλού σπιιν . Από υπολογισμούς η απόσταση μετάλλου υποαταστάτη για τα ίδια μεταλλοιόνται είναι: Δtetr = 4/9Δοkt (όχι μεγάλη)
Δtetr = 4/3 eσ + 8/4eπ -8/3eπ = 12/9eπ -16/9eπ = 4/9(3eσ -4eπ)
Εάν υπολογίσουμε την ενέργεια διαχωρισμού στο Οκτάεδρο Δokt = 3eσ -4eπ
Παρατηρούμε ότι: Δtetr =4/9 Δoct
ακόμη στο τετράεδρο τα αντιδεσμικά τροχιακά στνδέονται με τα δεμικά με τις σχέσεις : e* =3eσ και t2g* = 4eπ
Εάν στο τετραεδρικό σύμπλοκο δημιουργηθούν τέτοιες συνθήκες ώστε το σύμπλοκο που προκύπτει να χαρακτηρίζεται από ισχυρό πεδίο η τετραεδρκή γεωμετρία απορρίπτεται και ευννοούνται άλλες γεωμετρίες
Επίπεδο τετραγωνικό σύμπλοκο αριθμός ένταξης 4
Το επίπεδο τετραγωνικό σύμπλοκο (αριθμός ένταξης 4 ) προκύπτει από το οκταεδρικό μετά την απομάκρυνση των δύο υποκαταστατών που εντοπίζονται κατά μήκος του άξονα z σε μια οκταεδρική συναρμολόγηση.
Συνήθως παρατηρείται σε d8 σύστημα ισχυρού πεδίου γιατί τέτοια συστήματα καταλήγουν σε σύμπλοκα όπου τα 8d ηλεκτρόνια καταλαμβάνουν χαμηλής ενέργειας τροχιακά dxz, dyz, dz2, dxy, ενώ παραμένουν κενά τα υψηλότερης ενέργειας dx2-y2
Στο επίπεδο τετραγωνικό σύμπλοκο τα τροχιακά που χαρακτηρίζονται από z χαρακτήρα dz2, dzx, dzy, δέχονται μειωμένη άπωση από το πεδίο των υποκαταστατών και επομένως σταθεροποιούνται ενεργειακά.
Τα υπόλοιπα d τροχιακά ανεβαίνουν σε υψηλότερη ενεργειακή στάθμη ενώ το g παραμένει το ίδιο. Αυτό έχει σαν αποτέλεσμα το eg διαχωρίζεται σε δύο επίπεδα, το b1g ψηλότερα σε ενέργεια που αποτελείται από το dx2-y2 και το α1g σε χαμηλότερη ενέργεια που αποτελείται από το dz2 τροχιακό.
Η σταθεροποιητική επίδραση μέσω της δημιουργίας μοριακών τροχιακών που ασκείται από τους υποκαταστάτες (ενώσεις ένταξης) στοχεύει στα τροχιακά υψηλής ενέργειας dx2-y2
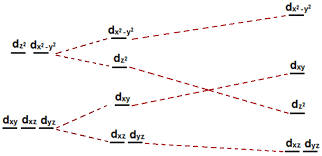
Τα d τροχιακά οκταέδρου, τετραέδρου και επίπεδου τετραγωνικού
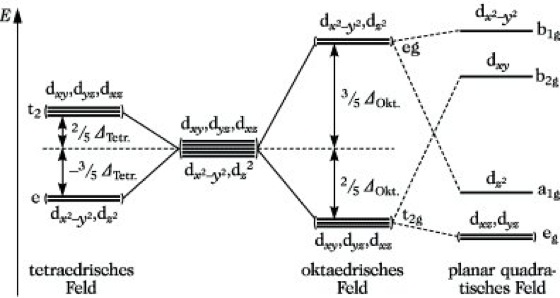
Παράδειγμα της ενέργειας διάχωρισμού πεδίου Δ στοιχείων μεταπτώσεως
- *Η Δ Εξαρτάται από τη Φύση του μεταλλοιόντος (Γεωμετρία. Ατομικός αριθμός: στην ίδια περίοδο με την αύξηση ΑΑ, έχουμε μείωση του Δ, ενώ στην ίδια ομάδα με αύξηση του ΑΑ έχουμε αύξηση Δ)
 1. Tο μεταλλοιόν Αu+2 6ης περιόδου στον περιοδικό πίνακα και 3ης σειρά στα μέταλλα μεταπτώσεως, εμφανίζει ενέργεια διαχωρισμού κρυσταλλικού πεδίου μεγαλύτερη σε σχέση με τον Cu+2 που βρίσκεται στην ίδια περίοδο αλλά στην 1η σειρά των στοιχείων μεταπτώσεως. Έτσι τα 2 από τα τρια ηλεκτρόνια του Αu σταθεροποιούνται και το τρίτο αποσταθεροποιείται και ανεβαίνει σε υψηλότερη ενεργειακή στοιβάδα. Δημιουργούνται εύκολα τετραγωνικά σύμπλοκα του Αu+3 που χαρακτηρίζονται από διαμαγνητικές ιδιότητες
1. Tο μεταλλοιόν Αu+2 6ης περιόδου στον περιοδικό πίνακα και 3ης σειρά στα μέταλλα μεταπτώσεως, εμφανίζει ενέργεια διαχωρισμού κρυσταλλικού πεδίου μεγαλύτερη σε σχέση με τον Cu+2 που βρίσκεται στην ίδια περίοδο αλλά στην 1η σειρά των στοιχείων μεταπτώσεως. Έτσι τα 2 από τα τρια ηλεκτρόνια του Αu σταθεροποιούνται και το τρίτο αποσταθεροποιείται και ανεβαίνει σε υψηλότερη ενεργειακή στοιβάδα. Δημιουργούνται εύκολα τετραγωνικά σύμπλοκα του Αu+3 που χαρακτηρίζονται από διαμαγνητικές ιδιότητες
2. Τα μεταλλοιόντα Pt 2+ και Rb2+ από την 3η και 2η σειρά των στοιχείων μετάπτωσης, προκαλούν μεγάλη διάσταση πεδίου Δ . Τα δυο ασύζευκτα ηλεκτρόνια αποκτούν μεγάλη ενέργεια και δεν μπορούν να σταθεροποιηθούν. Επομένως τα σύμπλοκα των μεταλλοιόντων αυτών, υιοθετούν επίπεδη γεωμετρία ώστε να πραγματοποιηθεί η σταθεροποίησή τους σε τροχιακό χαμηλότερης ενέργειας και εμφανίζουν επομένως διαμαγνητικές ιδιότητες. Αντίθετα τα αντίστοιχα οκταεδρικά σύμπλοκα είναι παραμαγνητικά
Που μειονεκτεί η θεωρία κρυσταλλικού πεδίου
Οι διάφοροι υποκαταστάτες είναι δυνατό να ταξινομηθούν ανάλογα με την τιμή του Δ που παρατηρούνται για ένα ορισμένο μεταλλικό ιόν
α. Αφού θεωρεί καθαρά ηλεκτροστατική την επίδραση μετάλλου- υποκαταστάτου, αποκλείει την ύπαρξη π δεσμού
β. Λαμβάνει υπ' όψη μόνο τα d τροχιακά όχι τα s και τα p
γ. Δεν δίνει σημασία στα τροχιακά των υποκαταστατών
Δ Η θεωρία του πεδίου των υποκαταστατών - Θεωρία των μοριακών τροχιακών J. S. Griffith , L. G. Orgel 1957
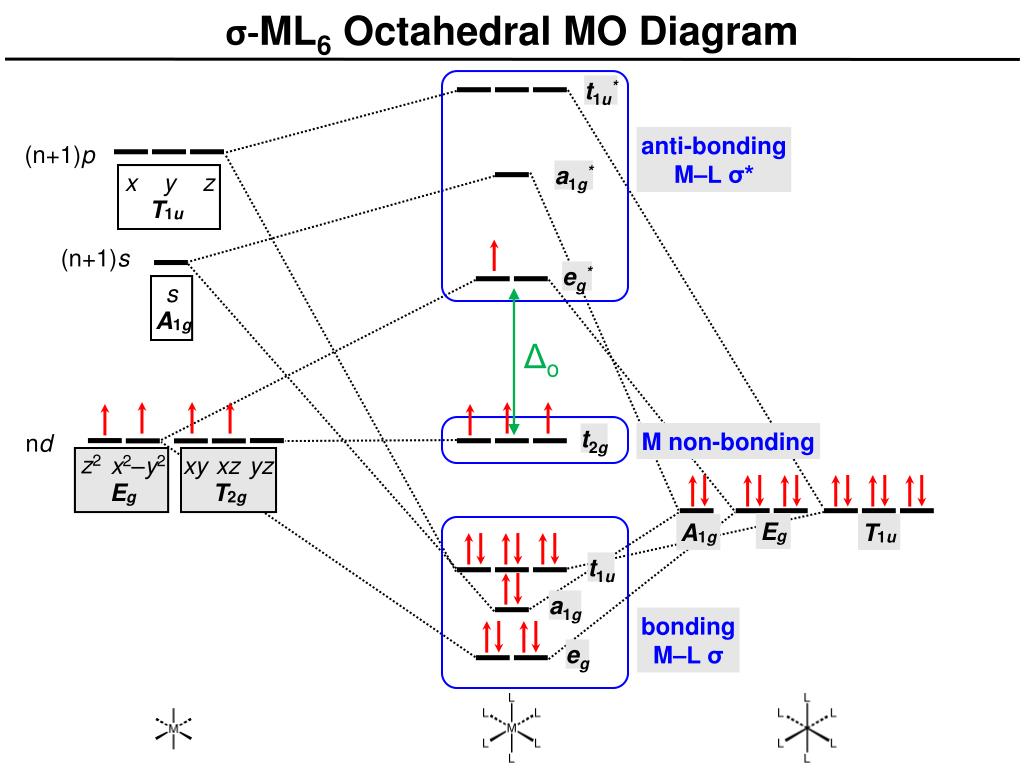
Η θεωρία αυτή δίνει απαντήσει στην δημιουργία συμπλόκων ενώσεων με την θεωρία των μοριακών τροχιακών. Θεωρεί τα μοριακά τροχιακά που σχηματίζονται από τα ατομικά τροχιακά σθένους του μετάλλου και τα τροχιακά σθένους των υποκαταστατών. Αυτή η μέθοδος είναι ικανή για να εξηγήσει την γεωμετρία των συμπλόκων, τις μαγνητικές και φασματοσκοπικές και καταλυτικές τους ιδιότητες.
Τα ατομικά τροχιακά είναι δυνατόν να επικαλύπτονται με βάση την συμμετρία τους.
Για παράδειγμα στο οκταεδρικό σύμπλοκο είναι άλλα τροχιακά που μπορούν να αλληλεπιδρούν με τους υποκαταστάτες και να αλληλοκαλύπτονται κι άλλα όχι: Τα t2g (d-xy, d-xz, d-yz) ενδιαμέσως των αξόνων, 'εχουν λιγότερη επίδραση με υποκαταστάτες ενώ
τα e-g (dz2, dx2-y2 )είναι έντονα επικαλυπτόμενα με τροχιακα υποκαταστατών
κατά μήκος των αξόνων
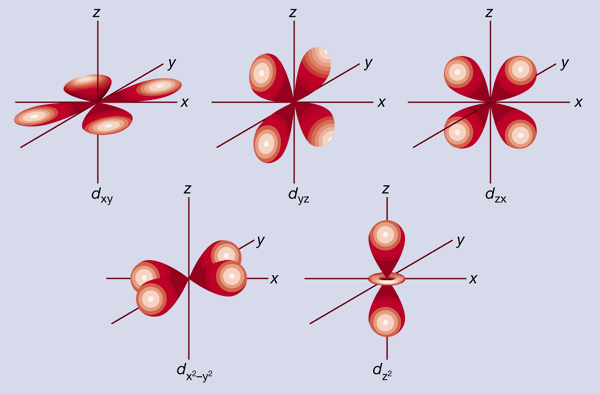
Τα τροχιακά d είναι 5. Τα τρία ανάμεσα στους άξονες και τα δύο πάνω στους άξονες
Τα τροχιακά d-xy, d-xz, d-yz είναι d τροχιακά που βρίσκονται μεταξύ των αξόνων
Τα τροχιακά dz2, dx2-y2 είναι ευθυγραμισμένα κατά μήκος των αξόνων x, y, z.
Τα t2g είναι τα d-xy, d-xz, d-yz, d τροχιακά που έχουν κέντρο συμμετρίας και η ενέργειά τους είναι μειωμένη κα τά 2/5 Δο για κάθε ηλεκτρόνιο επομένως σταθεροποιείται
Τα e-g είναι τα dz2, dx2-y2 d τροχιακά που έχουν έχουν κέντρο συμμετρίας και η ενέργειά τους είναι αυξημένη κατά 3/5 Δο για κάθε ηλεκτρόνιο επομένως αποσταθεροποιείται
ΟΙ ΜΟΡΙΑΚΟΙ ΔΕΣΜΟΙ -ΤΑ ΜΟΡΙΑΚΑ ΤΡΟΧΙΑΚΑ.ΤΙ ΕΙΝΑΙ
Μοριακά τροχιακά Τα μοριακά τροχιακά (σ, π, δ, φ), σχηματίζονται με τον συνδυασμό όλων των ατομικών τροχιακών των ατόμων του μορίου. Εάν με την αλληλοεπικάλυψη δύο ατομικών τροχιακών που ανήκουν σε διαφορετικά άτομα, προκύπτει ένα καινούργιο τροχιακό με ελαχιστοποιημένη την συνολική ενέργειά του τότε μιλάμε για μοριακό τροχιακό και πρόκειται για έναν ομοιοπολικό δεσμο στον οποίο προκύπτει,
Η ΕΝΝΟΙΑ ΤΟΥ ΥΒΡΙΔΙΣΜΟΥ ΑΤΟΜΙΚΩΝ ΤΡΟΧΙΑΚΩΝ ΑΠΟ ΔΙΑΦΟΡΕΤΙΚΑ ΑΤΟΜΑ - ΜΟΡΙΑΚΑ ΤΡΟΧΙΑΚΑ
προτάθηκε από τον Αμερικανό Χημικό Linus Pauling για να εξηγήσει τα τροχιακά σθένους πολύπλοκων
μορίων στα οποία, αν και η ενέργεια αυτών στο κεντρικό άτομο υπολογίζονταν αρχικά διαφορετική, σχημάτιζαν δεσμούς ισοδύναμους (σε σύνδεση με ίδιους προσδέτες)
ΠΟΙΟΙ ΕΙΝΑΙ ΟΙ ΔΕΣΜΟΙ ΠΟΥ ΣΥΝΑΝΤΑΜΕ
ΜΕΤΑΞΥ ΜΕΤΑΛΛΟΙΟΝΤΟΣ ΚΑΙ ΥΠΟΚΑΤΑΣΤΑΤΗ ΣΤΑ ΣΥΜΠΛΟΚΑ
ΟΙ σ ΚΑΙ ΟΙ π ΔΕΣΜΟΙ
Χαρακτηριστικό των κατηγοριών των συμπλόκων είναι οι αλληλεπιδράσεις τους μεταξύ δότη υποκαταστάτη L και δέκτη του μεταλλικού ιόντος M+(μόνο συμμετρία σ), όσο και οι αλληλοεπιδράσεις μεταξύ δέκτη υποκαταστάτη L και δότη μεταλλικού ιόντος που οι τελευταίες μέσω τροχιακών που διαθέτουν συμμετρία π
Οι σ δεσμοί Υποκαταστάτης :σ δότης για οκταεδρικό σύμπλοκο
 Στην σ αλληλεπίδραση L--M σ δεσμοί Δέκτης ηλεκτρονίων είναι το μεταλλικό ιόν
Στην σ αλληλεπίδραση L--M σ δεσμοί Δέκτης ηλεκτρονίων είναι το μεταλλικό ιόν .jpg)
Η δημιουργία ομοιοπολικών σ-δεσμών ένταξης πραγματοποιείται μεσω αλληλεπικάλυψης των κατειλημμένων τροχιακών των υποκαταστατών (Cl-, H2O, PR3, CN-, κ.Α.) με τα κενά τροχιακά μεταλλοιόντος τα οποία προκύπτουν έπειτα από υβριδισμό των s και p και d τροχιακών
Οι π δεσμοί. Υποκαταστάτης π δότης για οκταεδρικό σύμπλοκο
Στην π αλληλεπίδραση L--M π δεσμοί
Δυο p τροχιακά που σχηματίζουν δεσμό π δότης που είναι π δεσμός πλευρικής αλληλοκάλυψης Μετάλλων υψηλής οξειδωτικής βαθμίδας 4ης περιόδου και με υποκαταστάτες μεγάλης ηλεκτρoνιακής πυκνότητας (F-, Cl-, OH-, NH2-)
Εδώ τα δεσμικά t2g του μετάλου βρίσκονται χαμηλότερα από τα αρχικά τα t2g του μετάλου. Τα αντιδεσμικά t2g* του μετάλου όμως, βρίσκονται χαμηλότρα από τα eg*
Έτσι, τα δεσμικά t2g δέχονται ηλεκτρόνια από τους υποκαταστάτες ενώ τα t2g* έχουν πια τα ηλεκτρόνι από το μεταλλοιόν.
π δεσμός Υποκαταστάτης δέκτης με κενό π* τροχιακό
π δεσμός αλληλοκάλυψης Μετάλλων χαμηλής οξειδωτικής κατάστασης με συμπληρωμένα ή
σχεδόν συμπληρωμένα τα d τροχιακά τους με υποκαταστάτες σχετικά χαμηλής ηλεκτραρνητικότητας ( CO, NO2, NO, CN ή 1,10 φαινανθρολινη).
Εδώ τα κενά αντιδεσμικά π* τροχιακά του υποκαταστάτη βρίσκονται υψηλοτερα ενεργειακά από τα τροχιακά t2g του μετάλλου. Έτσι σχηματίζεται σετ t2g μοριακών τροχιακών από δεσμικά t2g χαμηλότερα σε ενέργεια από τα αρχικά t2g και αντιδεσμικά t2g*
Md->Lp αλληλοκάλυψη με την ηλεκτρονιακή πυκνότητα ενός d τροχιακού του μετάλλου και ενός κενού p τροχιακού του υποκαταστάτη.
H σταθεροποίηση επιτυγχάνεται με φαινόμενα συντονισμού
Όμως η θεωρία μοριακών τροχιακών δέχεται ότι η σταθερότητα οφείλεται σε αλληλοκάλυψη του d τροχιακού του μετάλλου και του π αντιδεσμικού τροχιακού του CO.
δεσμός με συνεισφορά των κατειλημένων π τροχιακών
.jpg)
π δοτικός δεσμός Εάν σε σύμπλοκες ενώσεις παρατηρείται απεντοπισμένο ηλεκτρονιακό νέφος δημειουργείται δεσμός με συνεισφορά μεταξύ μεταλλοιόντος και υποκαταστάτη των κατειλημένων π τροχιακών. Τέτοιες σύμπλοκες ενώσεις δημιουργούνται με υποκαταστάτες όπως οι ολεφίνες, τα αλκίνια κ.α.
Δημιουργείται κατ αρχή σ δεσμός μεταξύ του μεταλλοιόντος και του υποκαταστάτη αυτού του τύπου με την συμμετοχή των π τροχιακών του αιθυλενίου.
Παράλληλα το μέταλλο μοιράζεται ηλεκτρόνια με τα κενά π αντιδεσμικά του υποκαταστάτη με αποτέλεσμα την δημιουργία ενός διπλού δεσμού
π δεκτικός δεσμός: Κενά π τροχιακά χαμηλής ενέργειας των υποκαταστατών δέχονται ηλεκτρόνια από κατειλημένα d τροχιακά του μετάλλου για δημιουργία π ή σ δεσμών με το κεντρικό μεταλλοιόν ( η αποδοχή ηλεκτρονίων ονομάστηκε και π οξύτητα των υποκαταστατών)
π δεσμός αλληλοκάλυψης d τροχιακού του μετάλλου τροχιακού του υποκαταστάτη
Md-->Lp αλληλοκάλυψη ενός d τροχιακού του μετάλλου και ενός κενού p τροχιακού του υποκαταστάτη.
- π δεσμός επαναφοράς Η αλληλοκάλυψη γίνεται στο ίδιο επίπεδο με συμμετοχή των δύο λοβών
- δ δεσμός επαναφοράς Η αλληλοκάλυψη συμπεριλαμβανει και τους τέσσερις λοβούς Μεταξύ μετάλλων υψηλής οξειδωτικής βαθμίδας 5ης και 6ης περιόδου και υποκαταστατών PF3,PR3, AsR3, κ.α.
PPT - Coordination Chemistry II: Ligand Field Theory PowerPoint ...
ΠΗΓΕΣ
Βασικές Αρχές Ανόργανης Χημείας . Γ. ΠΝΕΥΜΑΤΙΚΑΚΗΣ -Χ. ΜΗΤΣΟΠΟΥΛΟΥ -Κ. ΜΕΘΕΝΙΤΗΣ
https://en.wikipedia.org/wiki/Tetrachloronickelate#:~:text=Near%20room%20temperature%2C%20these%20salts,consisting%20of%20octahedral%20Ni%20centers.
Θεωρία Πεδίου Υποκαταστατών.pptx
https://ruby.chemie.uni-freiburg.de/Vorlesung/metalle_8_3.html
https://klouras.chem.upatras.gr/attachments/article/30/10.%20CRYSTAL%20FIELD%20THEORY%28PPP%29.pdf
https://en.wikipedia.org/wiki/Crystal_field_theory#:~:text=The%20most%20common%20type%20of%20complex%20is,the%20latter%20and%20therefore%20experiences%20less%20repulsion.
https://courses.lumenlearning.com/suny-mcc-chemistryformajors-1/chapter/hybrid-atomic-orbitals/
file:///C:/Users/user/Downloads/100576_ΑΣΗΜΑΚΟΠΟΥΛΟΣ_
The Meaning of d-Orbital Labels
Χαρκοπλιάς Κώστας Χημικός: Γ΄Λυκείου: Τροχιακά s, p, d, f ... και η κυματοσυνάρτηση Ψ
Πηγή: https://wwwchem.uwimona.edu.jm/courses/Tanabe-Sugano/tetoct.gif
Η ΧΗΜΕΙΑ ΠΕΡΙΓΡΑΦΕΙ ΤΗΝ ΥΛΗ ΜΕ ΤΟΝ ΗΛΕΚΤΡΙΣΜΟ ΚΑΙ ΤΟΝ ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΣΜΟ: 6ο μέρος. Υλικά σιδηρομαγνητικά, διαμαγνητικά, παράμαγνητικά και οι ατομικές μαγνητικές ροπές τους
https://flexbooks.ck12.org/cbook/ck-12-cbse-chemistry-class-12/section/5.6/primary/lesson/crystal-field-theory/
ακατεργαστο
Σχήμα 29 α) Σύμπλοκο [NiCN4]2- με επίπεδη τετραγωνική γεωμετρία, β) σύμπλοκο FeCΟ5 με γεωμετρία τριγωνικής διπυραμίδας και γ) σύμπλοκο [FeCN6]3- με οκταεδρική γεωμετρία
|
|
Το λήμμα δεν περιέχει πηγές ή αυτές που περιέχει δεν επαρκούν. |
PPT - Molecular Orbitals PowerPoint Presentation, free download - ID .
Ligandenfeldtheorie - Lexikon der Chemie
