Δήμητρα Σπανού, χημικός, συνταξιούχος καθηγήτρια Μέσης Εκπαίδευσης από 30-6-2025
υπό κατασκευή
ΕΠΕΞΗΓΗΣΕΙΣ ΥΒΡΙΔΟΠΟΙΗΣΗ ΚΑΙ ΜΟΡΙΑΚΑ ΤΡΟΧΙΑΚΑ

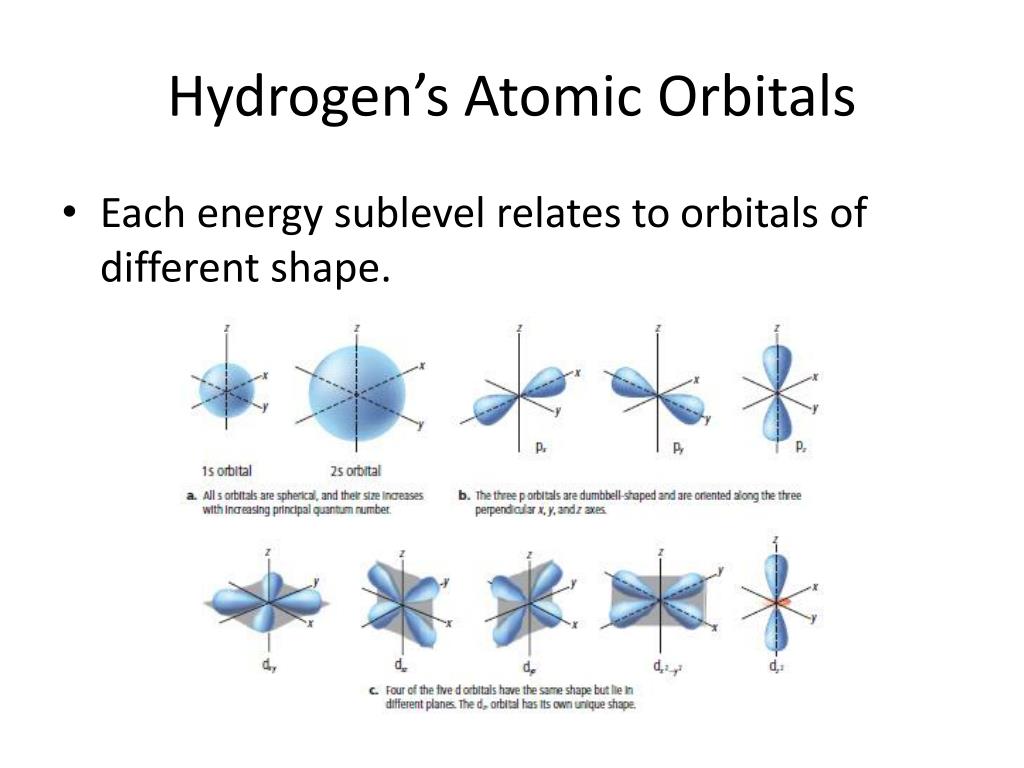
Τα ατομικά τροχιακά που είναι περιοχές του χώρου που περιβάλλουν τον πυρήνα ενός ατόμου στις οποίες είναι μεγαλύτερη η πιθανότητα για την εύρεση ενός ηλεκτρονίου. Αποτελούν δε επίλυση των εξισώσεων Schrondinger για κάθε ένα από τα ηλεκτρόνια αυτά. Οι τύποι των ατομικών τροχιακών που υπάρχουν είναι οι εξής: s, p, d, f, με διαφορετικό σχήμα προσανατολισμό και ενέργεια.
* Τα υβριδοποιημένα ατομικά και μοριακά τροχιακά
Αυτή η περιγραφή των απλών τροχιακών δεν είναι ικανοποιητική για πολύπλοκες ενώσεις και έτσι εισάγεται από τον Pauling to 1931 η έννοια του υβριδισμού των τροχιακών.
Υβριδοποιημένα ατομικά τροχιακά 
Συμφωνα με αυτήν ατομικά τροχιακά στο κέλυφος, σε ίδια ενεργειακή στοιβάδα ή σε συνεχόμενες, μπορούν να συνδυαστούν και να 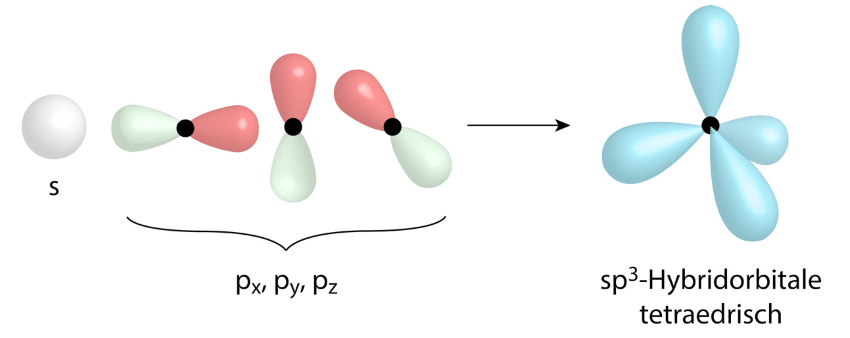 σχηματίσουν ίσα νέα ισοδύναμα ενεργειακά τροχιακά, αφού πρώτα επιλεγούν τα κατάλληλα ηλεκτρόνια. Τα τροχιακά που μπορούν να υβρυδοποιηθούν είναι τα s, p, d.
σχηματίσουν ίσα νέα ισοδύναμα ενεργειακά τροχιακά, αφού πρώτα επιλεγούν τα κατάλληλα ηλεκτρόνια. Τα τροχιακά που μπορούν να υβρυδοποιηθούν είναι τα s, p, d.
Παράδειγμα υβρυδισμού : αν συνδυαστούν από τα τροχιακά σθένους 1s και 3p τροχιακά μπορούν να σχηματίσουν τέσσερα sp3 υβριδοποιημένα ατομικά τροχιακά.7. Φυσικά υπάρχουν κι άλλα είδη υβριδισμού:

Όμοια τα τρία sp2 κ.λ.π. Σε σύμπλοκες ενώσεις είναι συχνός η υβριδοποίηση ταυτόχρονα s, p και d (dsp2, dsp3, d2sp3 )
Αν έχουμε τροχιακά με ίδια φορά στρέψης ++ή - - αυτά αλληλοενισχύονται και αντίθετα αν έχουν αντίθετη φορά στρέψης +- μειώνονται
Στην περίπτωση που ένα από τα υβριδοποιημένα αυτά τροχιακά sp3 είναι ημικατελειμμένα ( έχει ένα μόνο ηλεκτρόνιο) αυτό συνεισφέρεται για
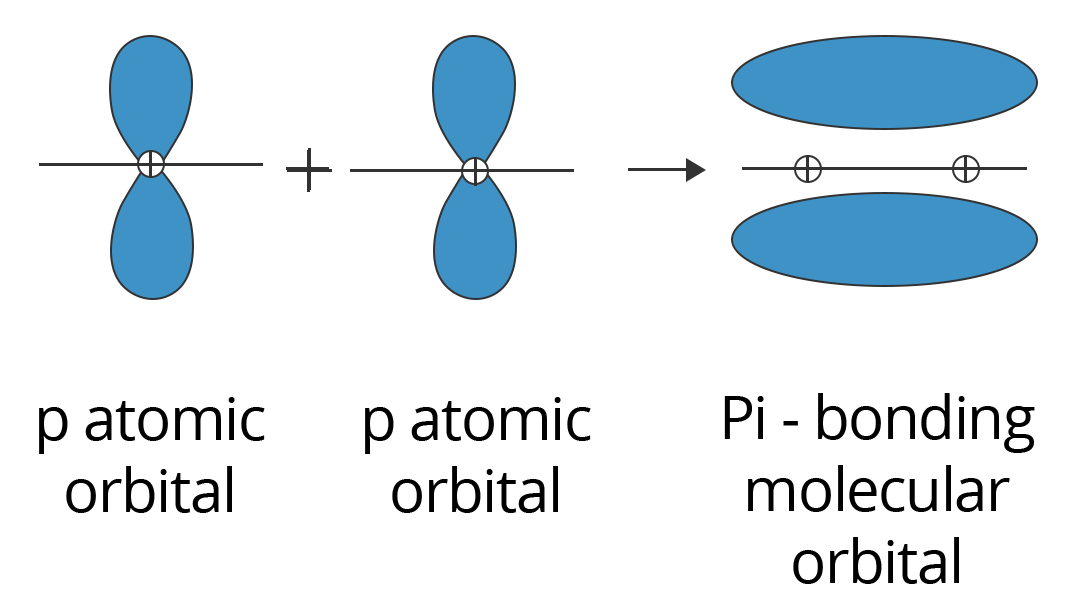
την δημιουργία ομοιπολικού σ- δεσμού μέσω γραμμικής αλληλοκάλυψης.
Πλευρική αλληλοκάλυψη p τροχιακού με κάποιο άλλο τροχιακό οδηγεί σε π-δεσμό
Μοριακά τροχιακά 
Τα μοριακά τροχιακά προκύπτουν από αλληλεπιδράσεις μεταξύ ατομικών τροχιακών ή υβριδιποιημένων ατομικών τροχιακών, οι οποίες επιτρέπονται αν οι συμμετρίες των ατομικών τροχιακών είναι συμβατές μεταξύ τους
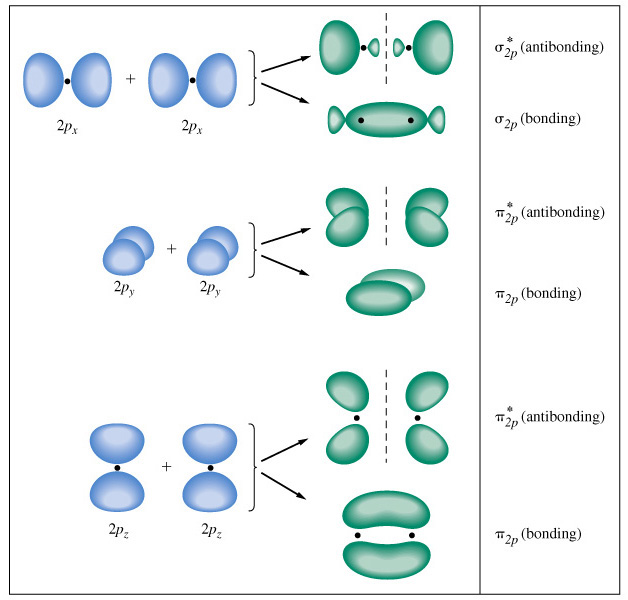 Γι αυτόν τον λόγο υπάρχουν τρεις κατηγορίες μοριακών τροχιακών:
Γι αυτόν τον λόγο υπάρχουν τρεις κατηγορίες μοριακών τροχιακών:
*****Τα δεσμικά μοριακά τροχιακά τα οποία έχουν χαμηλότερη ενέργεια από αυτήν των αντίστοιχων ατομικών τροχιακών
Τα αντιδεσμικά μοριακά τροχιακά τα οποία έχουν υψηλότερη ενέργεια από αυτήν των αντίστοιχων ατομικών τροχιακών
Τα μη δεσμικά μοριακά τροχιακά τα οποία έχουν ιση ενέργεια από αυτήν των αντίστοιχων ατομικών τροχιακών
ΥΒΡΙΔΟΠΟΙΗΣΗ ΣΤΙΣ ΣΥΜΠΛΟΚΕΣ ΕΝΩΣΕΙΣ
**Υβριδοποιημενα τροχιακά στις σύμπλοκες ενώσεις (ενώσεις ένταξης)
Πως δημιουργείται η σύμπλοκος ένωση
Η πλήρωση των κενών υβριδικών τροχιακών του μεταλλοϊόντος που ο αριθμός τους είναι ίσος με τον αριθμό των ατομικών του τροχιακών που λαμβάνουν μέρος στον υβριδισμό, επιτυγχάνεται μέσω του σχηματισμού δοτικών ομοιοπολικών δεσμών μεταξύ υποκαταστατών και κεντρικού ιόντος αφού ο κάθε υποκαταστάτης προσφέρει ένα ζεύγος ηλεκτρονίων στο μεταλλοιόν.
ΠΗΓΕΣ
https://dlefkad.blogspot.com/2017/02/blog-post.html
ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ - ΟΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ ΚΑΙ ΤΑ ΤΡΟΧΙΑΚΑ | PDF
