Δήμητρα Σπανού συνταξιούχος χημικός καθηγήτρια Βθμιας Εκπαίδευσης
ΕΙΙΣΑΓΩΓΙΚΟ
Η ΧΗΜΕΙΑ ΠΕΡΙΓΡΑΦΕΙ ΤΗΝ ΥΛΗ. ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ. ΣΥΜΠΕΡΙΦΟΡΑ ΧΗΜΙΚΩΝ ΣΤΟΙΧΕΙΩΝ κ.λ.π.
Ο τομέας αυτός αποτελεί συνέχεια από τον προηγούμενο: Η ΧΗΜΕΙΑ ΠΕΡΙΓΡΑΦΕΙ ΤΗΝ ΥΛΗ. ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ. ΕΣΩΤΕΡΙΚΗ ΔΟΜΗ ΥΛΙΚΩΝ ΣΩΜΑΤΩΝ.
Πολλές φορές στα κεφάλαια για την εσωτερική δομή των υλικών σωμάτων, αναφέρονται και οι ιδιότητές τους, που πάντα σχετίζονται με την εσωτερική τους δομή. Όμως επειδή συνήθως πρόκειται γαι θέματα πιο εκτεταμένα και δυσκολονόητα, τα δίνω εδώ κάπως ξεχωριστά, ώστε να μην αποσπούν την προσοχή από το κυρίως θέμα που είναι η εσωτερική δομή των υλικών σωμάτων
ΠΩΣ ΠΕΡΝΑ Η ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ ΜΕΣΑ ΑΠΟ ΤΗΝ ΥΛΗ
ΗΛΕΚΤΡΙΚΗ ΑΝΤΙΣΤΑΣΗ ΚΑΙ ΗΛΕΚΤΡΙΚΗ ΑΓΩΓΙΜΟΤΗΤΑ
Ηλεκτρική αγωγιμότητα είναι η ιδιότητα των υλικών να επιτρέπουν την διέλευση ηλεκτρικού ρεύματος διά μέσου αυτών υπό την επίδραση ηλεκτρικού πεδίου.
Η ηλεκτρική αγωγιμότητα ενός μέσου σχετίζεται με την ικανότητα των φορέων του ηλεκτρικής ενέργειας (συνήθως ηλεκτρόνια, οπές ή ιόντα) να διέρχονται και να κινούνται ελεύθερα μέσα σ΄αυτό.
Αυτό εξαρτάται α. από την φύση (δομή) της ουσίας β. τη χημική της σύσταση γ. την κατάσταση συσσωμάτωσης δ. από τις φυσικές συνθήκες (κυρίως θερμοκρασία)
Ταυτόχρονα όμως, τα υλικά εμποδίζουν την διέλευση του ηλεκτρικύ ρεύματος άλλα περισσότερο κι άλλα λιγότερο. Το μέτρο της δυσκολίας στην διέλευση του ηλεκτρικού ρεύματος δίνει η ηλεκτρική αντίσταση ενος υλικού στη διέλευση του ρεύματος.
Σσυνηθίζεται να αναφέρεται για διέλευση συνεχούς ρεύματος και όχι εναλλασσόμενου όπως συμβαίνει με τα διηλεκτρικά.
Στην διέλευσή του το ηλεκτρικό ρεύμα συναντά δυσκολίες. Αυτή οφείλεται κυρίως στις συγκρούσεις των φορέων του ηλεκτρισμού με τα άτομα και τα μόρια του υλικού
Όσο μικρότερη είναι η αντίσταση ενός αγωγού στην διέλευση του ρεύματος, τόσο μεγαλύτερη είναι η ηλεκτρική αγωγιμότητα αυτού. Η αντίσταση εξαρτάται από τα φυσικά χαρακτηριστικά του υλικού και τις συνθήκες περιβάλλοντος κυρίως τη θερμοκρασία.
ΘΕΩΡΙΑ ΤΩΝ ΗΛΕΚΤΡΙΚΩΝ ΖΩΝΩΝ ΓΙΑ ΤΟΝ ΗΛΕΚΤΡΙΣΜΟ ή
Ποια ηλεκτρόνια μπορούν να μεταφέρουν το ηλεκτρικό φορτίο
Είναι μια θεωρία που αναφέρεται σε κίνηση ηλεκτρονίων σε στερεά
Σύμφωνα με την θεωρία του Bohr τα ηλεκτρόνια των ατόμων είναι κβαντισμένα ως προς την ενέργεια και κατατάσσονται σε ανόλογες ηλεκτρονιακές στοιβάδες (ενεργειακές ζώνες) με διακριτές επιτερεπόμενες ενεργειακές τιμές που λέγονται ατομικά τροχιακά. Με αυτές τις ενεργειακές ζώνες δημιουργούνται επιτρεπτές ενεργειακές τιμές για τα ηλεκτρόνια του ατόμου (ζώνες) , που χωρίζονται από κβαντικά απαγορευμένες ενεργειακές περιοχές (ζώνες).
Δηλαδή τα ηλεκτρόνια των ατόμων δηλαδή βρίσκονται σε καθορισμένα ατομικά τροχιακά (που, στην γλώσσα των μαθηματικών σύμφωνα με τηνθεωρία του Bohr και Schrodinger περιστάνονται από μια κυματοσυνάρτηση του ηλεκτρονίου)
Επίσης τα ηλεκτρόνια των χημικών δεσμών , μεταξύ ατόμων έχουν άλλες επιτρεπτές ενεργειακές τιμές που υπολογίζονται από τις ξεχωριστές κβαντικές καταστάσεις κάθε ατόμου που συμμετέχει και βρίσκονται σε τροχιακά που είναι τα μοριακά τροχιακά

(Βέβαια εάν τα ηλεκτρόνια σθένους των ατόμων συνδέονται σχηματίζοντας ένας ομοιοπολικό δεσμό τα ατομικά τους τροχιακά συμπλέκονται για την δημιουργία μοριακού τροχιακού με ταυτόχρονη μεταβολή της επιτρεπτής ενεργειακής τους ζώνης, του χώρου που αναπτύσσονται και της μαθηματικής τους συνάρτησης)
Από τις κβαντισμένες περιοχές αυτή που ενδιαφέρει κυρίως εδώ είναι η ζώνη σθένους που είναι η ενεργειακή περιοχή ή αλλιώς τα τροχιακά , των ηλεκτρονίων της εξωτερικής στοιβάδας του ατόμου που συνήθως αποτελεί και την στοιβάδα σθένους και βρίσκεται στο ανώτερο επιπεδο της κατανομής των ενεργεικών ζωνών (τροχιακών) των ηλεκτρονίων του ατόμου.
Κι αυτό γιατί, οι πλήρως κατελημένες ζώνες πιο κάτω, με την χαμηλότερη ενέργεια, δεν μπορούν να συμβάλουν στην ηλεκτρική αγωγιμότητα γιατί ακόμα κι αν τα ηλεκτρονια αυτά απορροφούν ενέργεια από το ηλεκτρικό πεδίο, την χρησιμοποιούν για την ενεργειακή ανύψωση της ζώνης τους.
Έτσι, η
![]() Ζώνη σθένους που :
Ζώνη σθένους που :
είναι η υψηλότερη πλήρως κατελημένη ζώνη ενέργειας ενεργειακά κβαντισμένων ηλεκτρονίων στο απόλυτο μηδέν και είναι οι ζώνες ηλεκτρονίων στις οποίες τα ηλεκτρόνια συμβάλουν στον χημικό δεσμό
Από τη ζώνη αυτή συγκεντρώνουμε την προσοχή μας στο πάνω μέρος της που λέγεται οροφή της ζώνης σθένους
Κυρίως εξετάζουμε όχι την ενέργειά της, αλλά την διαφορά ενέργειας που έχει με τα άλλα επίπεδα ζωνών από τη ζώνη αγωγιμότητας που θα δούμε στη συνέχεια.
Ζώνη αγωγιμότητας
Εκτός όμως από τα ηλεκτρόνια που είναι δεσμευμένα σε ατομικά ή μοριακά τροχιακά, έχουμε τα ελεύθερα ηλεκτρόνια δεν είναι κβαντισμένα και μπορούν να πάρουν οποιανδήποτε τιμή στην ενέργειά τους και το ενεργειακό τους φάσμα είναι συνεχές και .
Για να κινηθουν ηλεκτρόνια μέσα στο στερεό είναι απαραίτητες οι καταστάσεις ελεύθερης ενέργειας.
Ο όρος χρησιμοποιείται για να εξηγησει την ηλεκτρική αγωγιμότητα (ιδιαίτερα των ημιαγωγών που θα δούμε παρακάτω).
Η Ζώνη αγωγιμότητας είναι μοντέλο ζώνης που χρησιμοποιείται για να εξηγήσει την ηλεκτρική αγωγιμότητα των υλικών. Αναφέρεται για την ενεργειακή ζώνη που βρίσκεται ενεργειακά πάνω από τη ζώνη σθένους των ηλεκτρονίων
Ηλεκτρόνια που βρίσκονται στην ζώνη αγωγιμότητας μπορούν εύκολα να απορροφήσουν ενέργεια από ένα ηλεκτρικό πεδίο λόγω καταστάσεων ελεύθερης ενέργειας στη ζώνη αγωγιμότητας. Σύμφωνα με το θεώρημα Bloch τα ηλεκτρόνια τότε θεωρούνται σαν ελεύθερα σωματίδια και εφαρμόζεται σε αυτά η εξίσωση Stondinger. Επομένως το υλικό της ζώνης αγωγιμότητας είναι ηλεκτρικά αγώγιμο.
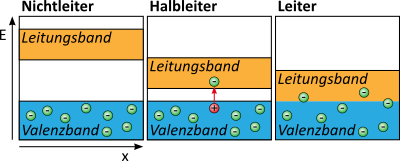
ΣΥΜΠΕΡΙΦΟΡΑ ΤΩΝ ΧΗΜΙΚΩΝ ΣΤΟΙΧΕΙΩΝ ΩΣ ΠΡΟΣ ΤΟΝ ΗΛΕΚΤΡΙΣΜΟ: ΑΓΩΓΟΙ, ΗΜΙΑΓΩΓΟΙ, ΜΟΝΩΤΕΣ
Οι αγωγοί του ηλεκτρισμού διακρίνονται σε αγωγούς πρώτου είδους που είναι τα μέταλλα και οι φορείς είναι τα ηλεκτρόνια και αγωγούς δεύτερου είδους που περιλαμβάνουν αέρια και μερικές στερεές ουσίες (ιοντικούς κρυστάλλους και γυαλιά, τετηγμένα άλατα και διαλύματα ουσιών σε νερό , μη υδατικούς διαλύτες και τήγματα) οι φορείς του ηλεκτρικού ρεύματος είναι ιόντα.
Συνοπτικά,
Στην περίπτωση των αγωγών αυτή η ζώνη σθένους είτε είναι πανομοιότυπη με την ζώνη αγωγιμότητας (όπως στην περίπτωση του Νατρίου) ή να μπορεί να επικαλύπτεται από την επόμενη ενεργειακά υψηλότερη ζώνη
Στην περίπτωση των ημιαγωγών και των μονωτών αυτή η ζώνη σθένους καταλαμβάνεται πλήρως και διαχωρίζεται από την ζώνη αγωγιμότητας από διάκενο ζώνης. Μπορούν να ξεπεράσουν μόνο με παροχή ενέργειας (θερμική, κινητική, φωτονική)
Όπως γραφτηκε πιο πάνω, οι πλήρως κατελημένες ζώνες δεν μπορούν να συμβάλουν στην ηλεκτρική αγωγιμότητά τους.
Οι αγωγοί του ηλεκτρισμου
Οι αγωγοί του ηλεκτρισμου είναι ουσίες, μέσα ή υλικά τα οποία εάν τοποθετηθούν σε μια περιοχή με διαφορά ηλεκτρικού Δυναμικού, οι φορείς του ρεύματος (ηλεκτρόνια, ιόντα, οπές) κινούνται προς την περιοχή χαμηλού δυναμικού μεταφέροντας έτσι ηλεκτρικό ρεύμα. Παράδειγμα στα μέταλλα τα ηλεκτρόνια είναι χαλαρά συνδεδεμένα με τα άτομα.
Οι αγωγοί έχουν ποιοτικά χαρακτηριστικά (που χαρακτιρίζουν την ικανότητά του και τον τρόπο του να μεταφέρει ηλεκτρικό ρεύμα)
και ποσοτικά χαρακτηριστικά (που υποδεικνύουν την ποσότητα του ηλεκτρικού ρεύματος που μπορεί να περάσει για πολύ καιρό υπό κανονικές συνθήκες)
Διακρίνονται σε αγωγούς πρώτου είδους που έχουν ηλεκτρική αγωγιμότητα
Αγωγούς δευτέρου είδους στους οποίους η μεταφορά του ηλεκτρικού ρεύματος γίνεται με ιόντα (ηλεκτρολύτες)
Οι αγωγοί υπό κανονικές συνθήκες, μπορούν να είναι στερεά σώματα (μέταλλα, ημιμέταλλα και ο άνθρακας υπό μορφή γραφίτη)
υγρά (ο υδράργυρος, οι ηλεκτρολύτες, λυωμένα μέταλλα)
αέρια (πλάσμα)
Σύμφωνα τώρα με την θεωρία των ζωνών αγωγιμότητας σε έναν αγωγό
η ανώτερη ζώνη δεν είναι πλήρως γεμάτη με ηλεκτρόνια
ή
οι ζώνες γειτονικών επιπέδων αλληλοεπικαλύπτονται.
Κάτω υπάρχει ένα γράφημα που δείχνει τις ενεργειακές ζώνες στα ηλεκτρόνια του Λιθίου. Βλεπουμε το εύρος των ζωνών, την απόσταση από τον πυρήνα και την αλληλοεπικάλυψη s και p ηλεκτρονίων

Εικόνα 2. Γράφημα των ενεργειακών επιπέδων που διασπώνται ως συνάρτηση της απόστασης μεταξύ των ατόμων Μεταφορά από Θεωρία αγωγιμότητας με βάση τη ζώνη

Μεταφορά από Θεωρία αγωγιμότητας με βάση τη ζώνη
Οι ημιαγωγοί του ηλεκτρισμου
Οι ημιαγωγοί εμφανίζουν ιδιότητες μονωτών αλλά και αγωγών όταν τους δωθεί η ανάλογη ενέργεια ,
Στους ημιαγωγούς υπάρχει διάκενο ζώνης ανάμεσα στη ζώνη σθένους και την ζώνη αγωγημότητας. Η ειδική αγωγιμότητα είναι από 105 έως 1010 Ohms/cm
 Το διάκενο μεταξύ της ζώνη αγωγιμότητας και της ζώνης σθένους δεν είναι μεγάλου εύρους δηλαδή μικρότερο των 2 eV. Έτσι εύκολα με σχετικά μικρή ενέργεια ηλεκτρόνια από την ζώνη σθένους μπορούν να μεταβούν στην ζώνη αγωγιμότητας και οι ημιαγωγοί από μονωτές να μετατραπούν σε αγωγούς.
Το διάκενο μεταξύ της ζώνη αγωγιμότητας και της ζώνης σθένους δεν είναι μεγάλου εύρους δηλαδή μικρότερο των 2 eV. Έτσι εύκολα με σχετικά μικρή ενέργεια ηλεκτρόνια από την ζώνη σθένους μπορούν να μεταβούν στην ζώνη αγωγιμότητας και οι ημιαγωγοί από μονωτές να μετατραπούν σε αγωγούς.
Για αυτόν τον λόγω η θέρμανση αυξάνει τις αγώγιμες ιδιότητες των ημιαγωγών (αντίθετα με τους αγωγούς που τις μειώνει λόγω αύξησης της αντίστασης του αγωγού)
Ημιαγωγοί από τα χημικά στοιχεία είναι το πυρίτιο το Γερμάνιο, το σελήνιο, το Τελλούριο, το Αρσενικό κ.α. Συναντώνται σε κρυσταλλική μορφή σε κρυστάλλους που δημιουργούν ομοιοπολικούς δεσμούς
Να σημειώσουμε ότι ιδιότητες ημιαγωγών έχουν πολλά κράματα και πολλές χημικές ενώσεις (αλλά και χημικά στοιχεία με προσμίξεις)
Ένα παράδειγμα ημιαγωγού είναι το πυρίτιο. Στην κρυσταλλική μορφή του είναι μονωτής. Όταν στο πυρίτιο υπάρχουν προσμίξεις από ομάδα ΙΙΙ, αργιλίου, Γάλλιο, Βόριο Ίνδιο γίνεται ημιαγωγός οπών. Αν περιέχει προσμίξεις από την ομάδα ΙV όπως φωσφόρος, Αρσενικό, Αντιμόνιο γίνεται ημιαγωγός ηλεκτρονίων
Οι μονωτές του ηλεκτρισμου
Οι μονωτές του ηλεκτρισμου είναι ουσίες, μέσα ή υλικά δεν μπορούν να μεταφέρουν ηλεκτρικό ρεύμα, ακόμα κι αν εφαρμοστεί μια διαφορά Δυναμικού κυρίως γιατί οι φορείς του ρεύματος (ηλεκτρόνια) δεν γεν έχουν χώρο ώστε μπορούν να κινηθούν ελεύθερα μέσα στο υλικό και γιατί είναι στενά συνδεδεμένα μετα άτομα. 
Εικόνα 8. Γράφημα ενεργειακών ζωνών στα διηλεκτρικά
Στους μονωτές ή διηλεκτρικά υπάρχει διάκενο ζώνης ανάμεσα στη ζώνη σθένους και την ζώνη αγωγημότητας.
Η ζώνη αγωγιμότητας και η ζώνη σθένους χωρίζονται με διάκενο μεγάλου εύρους δηλαδή μεγαλύτερο των 5 eV. Η μετάβαση των ηλεκτρονίων των μονωτών στη ζώνη αγωγιμότητας μπορεί να γίνει μόνο με ιονίζουσα ακτινοβολία
Η ειδική αγωγιμότητα είναι από 1010 έως 1015 Ohms/cm
ΥΠΕΡΑΓΩΓΟΙ
Σε πολύ χαμηλή θερμοκρασία, κοντά στο απόλυτο μηδέν κάποια υλικά μεταξύ των οποίων και μέταλλα εμφανίζουν μηδενική αντίσταση στην ροή του ηλεκτρικού ρεύματος και απειρή αγωγιμότητα. Ένα υλικό που χρησιμοποιείται σε υπεραγωγούς είναι το κράμα Γερμάνιο με Γάλλιο
.jpg)
Δήμητρα Σπανού
ΠΗΓΕΣ
Ηλεκτρικοί Αγωγοί & Μονωτές | Ηλεκτρισμός & Μαγνητισμός | Έβδομη Τάξη | ΦυσικήΡοή
Θεωρία αγωγιμότητας με βάση τη ζώνη
ΘΕΩΡΙΑ ΤΩΝ ΗΛΕΚΤΡΙΚΩΝ ΖΩΝΩΝ
Ποια ηλεκτρόνια μπορούν να μεταφέρουν το ηλεκτρικό φορτίο
Είναι μια θεωρία που αναφέρεται σε κίνηση ηλεκτρονίων σε στερεά
Τα ηλεκτρόνια των ατόμων είναι κβαντισμένα ως προς την ενέργεια και κατατάσσονται σε ανόλογες ηλεκτρονιακές στοιβάδες (ενεργειακές ζώνες) με διακριτές επιτερεπόμενες ενεργειακές τιμές. Αυτές οι ενεργειακές ζώνες χωρίζονται από κβαντικά απαγορευμένες ενεργειακές περιοχές (ζώνες).
Τα ηλεκτρόνια των ατόμων δηλαδή βρίσκονται σε καθορισμένα ατομικά τροχιακά (θεωρία Bohr)
Αντίθετα, τα ελεύθερα ηλεκτρόνια δεν είναι κβαντισμένα και μπορούν να πάρουν οποιανδήποτε τιμή στην ενέργειά τους και το ενεργειακό τους φάσμα είναι συνεχές.
Επίσης τα ηλεκτρόνια των χημικών δεσμών , μεταξύ ατόμων έχουν άλλες επιτρεπτές ενεργειακές τιμές που υπολογίζονται από τις ξεχωριστές κβαντικές καταστάσεις κάθε ατόμου που συμμετέχει και βρίσκονται σε τροχιακά που είναι τα μοριακά τροχιακά
Ζώνη σθένους: Ο όρος χρησιμοποιείται για να εξηγησει την ηλεκτρική αγωγιμότητα ιδιαίτερα των ημιαγωγών.
Είναι η υψηλότερη πλήρως κατελημένη ζώνη ενέργειας ενεργειακά κβαντισμένων ηλεκτρονίων στο απόλυτο μηδέν ή είναι οι ζώνες ηλεκτρονίων στις οποίες τα ηλεκτρόνια συμβάλουν στον χημικό δεσμό . Οι πλήρως κατελημένες ζώνες δεν μπορούν να συμβάλουν στην ηλεκτρική αγωγιμότητα γιατί ακόμα κι αν τα ηλεκτρονια αυτά απορροφούν ενέργεια από το ηλεκτρικό πεδίο, την χρησιμοποιούν για την ενεργειακή ανύψωση της ζώνης τους.
Για να κινηθουν ηλεκτρόνια μέσα στο στερεό είναι απαραίτητες οι καταστάσεις ελεύθερης ενέργειας.
Ζώνη αγωγιμότητας: Είναι είναι μοντέλο ζώνης που χρησιμοποιείται για να εξηγήσει την ηλεκτρική αγωγιμότητα των υλικών. Αναφέρεται για την ενεργειακή ζώνη που βρίσκεται ενεργειακά πάνω από τη ζώνη σθένους των ηλεκτρονίων
Ηλεκτρόνια που βρίσκονται στην ζώνη αγωγιμότητας μπορούν εύκολα να απορροφήσουν ενέργεια από ένα ηλεκτρικό πεδίο λόγω καταστάσεων ελεύθερης ενέργειας στη ζώνη αγωγιμότητας. Σύμφωνα με το θεώρημα Bloch τα ηλεκτρόνια τότε θεωρούνται σαν ελεύθερα σωματίδια και εφαρμόζεται σε αυτά η εξίσωση Stondinger. Επομένως το υλικό είναι ηλεκτρικά αγώγιμο.
ΣΥΜΠΕΡΙΦΟΡΑ ΤΩΝ ΜΕΤΑΛΛΩΝ ΩΣ ΠΡΟΣ ΤΟΝ ΗΛΕΚΤΡΙΣΜΟ
Ζώνη σθένους: Ο όρος χρησιμοποιείται για να εξηγησει την ηλεκτρική αγωγιμότητα ιδιαίτερα των ημιαγωγών. Είναι η υψηλότερη πλήρως κατελημένη ζώνη ενέργειας ηλεκτρονίων στο απόλυτο μηδέν ή είναι οι ζώνες ηλεκτρονίων στις οποίες τα ηλεκτρόνια συμβάλουν στον χημικό δεσμό.
Στην περίπτωση των αγωγών αυτή η ζώνη σθένους είτε είναι πανομοιότυπη με την ζώνη αγωγιμότητας (όπως στην περίπτωση του Νατρίου) ή να μπορεί να επικαλύπτεται από την επόμενη ενεργειακά υψηλότερη ζώνη
Η ζώνη σθένους ενός μονοσθενούς μετάλλου όπως του Νατρίου που είναι η 3s1 και είναι μερικώς κατελημένη με 1 ηλεκτρόνιο. Στο κρυσταλλικό πλέγμα του κατασκευάζεται, κάθε άτομο συνεισφέρει ένα ηλεκτρόνιο σθένους στον χημικό ιοντικό δεσμό.
Έτσι, η ζώνη σθένους γίνεται ενεργειακά πανομοιότυπη με την ζώνη αγωγιμότητας και το μονοσθενές μέταλλο που δημιουργεί κρυστάλλους γίνεται ηλεκτρικά αγώγιμο
Αντί για το ατομικό τροχιακό του ηλεκτρονίου του ατόμου του νατρίου, αυτό επεκτείνεται σε μοριακά τροχιακά που δημιουργείται συγκεκριμένα στην νέα κατάσταση ύπαρξης του ηλεκτρονίου, αυτήν του κρυσταλλικού πλέγματος, που περιγράφεται επίσης από μια νέα μορφή της εξίσωσης Strondinger.
Κάθε μοριακό τροχιακό έχει μια ορισμένη ενέργεια που είναι πολύ κοντά στην ενέργεια ιοντισμού
( Κάθε μοριακό τροχιακό έχει μια ορισμένη ενέργεια, που χαρακτηρίζεται περίπου από ένα αντίστοιχο δυναμικό ιονισμού.)
Σε αντίθεση με τα μονοκεντρικά ατομικά τροχιακά τα τροχιακά του χημικού δεσμού (κρυσταλλικό πλέγμα στην προκειμένη περίπτωση, είναι πολυκεντρικά και σε αντιστοιχία με τα s, p, d, f, ορίζονται σαν σ, π, δ, φ.
Στα δισθενή μέταλλα όμως, η στοιβάδα σθένους είναι με δύο ηλεκτρόνια και το ατομικό τροχιακό είναι κατειλημένο και θα έπρεπε να μην διαθέτει ηλεκτρική αγωγιμότητα