Δήμητρα Σπανού καθηγήτρια χημικός, συνταξιούχος Δευτερο/ιας Εκπ/σης από 30-6-2025
ΕΙΣΑΓΩΓΗ
Οι εξωτερικά μακροσκοπικές μεταβολές στην μάζα των σωμάτων βρίσκουν την ερμηνεία τους στον μικρόκοσμο των σωματιδίων της ύλης. Εκεί η μελέτη της συμπεριφοράς των σωματιδίων των κινήσεων και των αλληλεπιδράσεων θα δώσει τα στοιχεία για τον προσδιορισμό των εξωτερικών παραμέτρων.
Αυτά είναι θέματα που αφορούν την Επιστήμη της Στατιστικής που ασχολείται με την συλλογή και ανάλυση δεδομένων που διευκολύνουν την μελέτη και επεξεργασία προβλημάτων διαφόρων κλάδων της επιστήμης . Πιο συγκεκριμένα εδώ η Στατιστική Φυσική συστημάτων σωματιδίων χρησιμοποιεί κατά πολύ τις εξισώσεις, τα στατιστικά στοιχεία και κατανομές στην μελέτη τους.
Η γνώση της κατανομής των σωματιδίων σε ένα σύστημα καθιστά δυνατή την εύρεση των μέσων τιμών διαφόρων χαρακτηριστικών ενός θερμοδυναμικού συστήματος με την βοήθεια της Μαθηματικής Φυσικής
Έτσι δίνεται η δυνατότητα να γιίνει καλύτερα κατανοητή η χημική τους δραστηριότητα. Δ.Σ
Η ΚΑΝΟΝΙΚΗ ΚΑΤΑΝΟΜΗ
Στη Στατιστική Μηχανική η κανονική κατανομή χρησιμοποιείται συχνά για να περιγράψει συστήματα σε θερμοδυναμική ισορροπία, σε σταθερή θερμοκρασία, όγκο με σταθερό αριθμό σωματιδίων που ανταλλάσει ενέργεια με το περιβάλλον. Αυτή η κατανομή παίζει σημαντικό ρόλο στη θεωρία των στατιστικών συνόλων και αποτελεί βάση για την περιγραφή πολλών φυσικών διεργασιών όπως η θερμική αγωγιμότητα, η διάχυση και οι αντιδράσεις χημικής ισορροπίας
Η κανονική κατανομή συστήματος με ενέργεια Ει καθορίζεται από τον τύπο: P(Ei) = 1/Z exp(-βEi) όπου β=1/kbT με kb σταθερά Boltzman και Ζ είναι κι αυτή συνάρτηση κατανομής που ονομάζεται στατιστικό άθροισμα το οποίο κανονικοποιεί την κατανομή ώστε το άθροισμα όλων των περιοχών των πιθανών καταστάσεων να είναι ίσο με 1 Ζ = ∑ie−βΕi
Η συνάρτηση κατανομής Ζ είναι σημαντική γιατί από αυτό το σύνολο εξαρτώνται θερμοδυναμικά μεγέθη του συστήματος όπως η πίεση, η ελεύθερη ενέργεια , η εντροπία και η πίεση
Θερμοδυναμικοί παράμετροι που μπορούν να εκφραστούν μέσω της κανονικής κατανομής
και δίνουν τη σχέση μεταξύ μικροσκοπικών ιδιοτήτων και μακροσκοπικών θερμοδυναμικών παραμέτρων
- Η μέση ενέργεια του συστήματος ως σταθμισμένος μέσος όρος όλων των δυνατών ενεργειών: ⟨E⟩=ΣP(Ei)Ei=1/ZΣEiexp(-βΕi)
- Η ελεύθερη ενέργεια F του συστήματος ως F= -kβΤλνΖ H ελεύθερη ενέργεια καθορίζει το έργο που μπορεί να επιτελέσει το σύστημα υπό σταθερή θερμοκρασία
- Η Εντροπία S ενός συστήματος σε κανονικό σύνολο μπορεί να εκφραστεί με την ελεύθερη ενέργεια f και την μέση ενέργεια ⟨E⟩
Η κατανομή του Bolzman
Είναι μια κατανομή πιθανοτήτων διαφορετικών ενεργειακών καταστάσεων των σωματιδίων ενός ιδανικού θερμικού συστήματος όπως ένα ιδανικό αέριο αερίου, υπό συνθήκες θερμοδυναμικής ισορροπίας.
Η κατανομή Boltzman ισχύει μόνο για ιδανικά αέρια αφού στα πραγματικά υπάρχουν αλληλεπιδράσεις όπως δυνάμεις van der waals, κβαντικές ή αλληλεπιδράσεις ανταλλαγής.
Όμως η κατανομή που επικρατεί δεν είναι αυτή που αναφέρεται αρχικά σαν κατανομής πιθανοτήτων  ,
,
η οποία συνάρτηση f(x,y,z) περιγράφει την πιθανότητα εύρεσης ενός μικροσωματιδίου σε ένα συγκεκριμένο σημείο του χώρου,
αλλά η κατανομή που εξετάζει άμεσα τον αριθμό σωματιδίων  , που βρίσκονται στον χώρο ( όγκος V) δηλαδή την συγκέντρωση των μικροσωματιδίων (και όχι την συνάρτηση κατανομής τους δηλαδή την πιθανότητα εύρεσης ενός σωματιδίου σε ένα σημείο του χώρου)
, που βρίσκονται στον χώρο ( όγκος V) δηλαδή την συγκέντρωση των μικροσωματιδίων (και όχι την συνάρτηση κατανομής τους δηλαδή την πιθανότητα εύρεσης ενός σωματιδίου σε ένα σημείο του χώρου)
Αν το σύστημα δεν επιρεάζεται από εξωτερικές δυνάμεις και βρίσκεται σε κατάσταση θερμοδυναμικής ισορροπίας τότε η συγκέντρωση των μικροσωματιδίων είναι ιδια σε όλα τα σημεία του συστήματος.
Στην περίπτωση όμως που επιρρεάζονται από ένα εξωτερικό πεδίο η συγκέντρωσή τους είναι διαφορετική σε διαφορετικά σημεία του χώρου αλλά με ταυτόχρονη διατήρηση της θερμοδυναμικής ισορροπίας. (Τ σταθερό) 
Σύμφωνα με αυτήν, ο αριθμός σωματιδίων ni με συνολική ενέργεια Εi ισούται με ni =A•ωi •eEi /Kt (1) (ω είναι το στατιστικό βάρος, και Α προέρχεται από το άθροισμα ni για όλα τα σωματίδια (είναι σταθερά) που δεν εξαρτάται από τα qi, pi αλλά καθορίζεται από την συνθήκη κανονικοποίησης, ώστε η συνολική πιθανότητα να είναι ένα, η Τ είναι η απόλυτη θερμοκρασία, η k είναι η σταθερά του Boltzman
( n(x,y,z) η συγκέντρωση σωματιδίων στη στατιστική περιγραφή της κατανομής του).
Μπορούμε να μελετήσουμε την κατανομή Boltzman σε βαρυτικό πεδίο και να εξάγουμε από εκεί την εξίσωση κατανομής σωματιδίων υπό την επίδραση εξωτερικού δυναμικού πεδίου
Κατανομή Boltzman στο βαρυτικό πεδίο
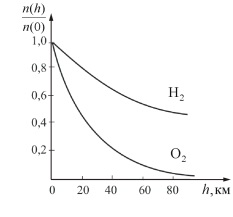 Παράδειγμα της κατανομής Boltzman είναι η κατανομή σωματιδίων στο βαρυτικό πεδίο, που είναι ένα εξωτερικό πεδίο που επιφέρει πάνω στα σωματίδια δυναμική ενέργεια U(x,y,z) στις θέσεις που βρίσκονται. Θα υποθέσουμε ότι το βαρυτικό πεδίο είναι ομοιόμορφο και ο άξονας κίνησης κατευθύνεται κάθετα προς τα πάνω.
Παράδειγμα της κατανομής Boltzman είναι η κατανομή σωματιδίων στο βαρυτικό πεδίο, που είναι ένα εξωτερικό πεδίο που επιφέρει πάνω στα σωματίδια δυναμική ενέργεια U(x,y,z) στις θέσεις που βρίσκονται. Θα υποθέσουμε ότι το βαρυτικό πεδίο είναι ομοιόμορφο και ο άξονας κίνησης κατευθύνεται κάθετα προς τα πάνω.
Η δυναμική ενέργεια μεταβάλλεται με το ύψος, επειδή η δυναμικύ ενέργεια λόγω εξωτερικού πεδίου (βαρυτικό) μειώνεται οπότε μειώνεται και η πίεση και ο αριθμός των μορίων ανά μονάδα όγκου. Σύμφωνα με την βασική εξίσωση κινητικής θεωρίας μπορούμε να έχουμε αντικατάσταση του P από το n.
n= no exp(-mgh/kT) Αυτή είναι η κατανομή Boltzman στο βαρυτικό πεδίο
- Ο αριθμός των μορίων ανά μονάδα όγκου n μειώνεται με την μείωση τηςη θερμοκρασίας και την αύξηση του h.
- Εάν Τ=0 δεν παρατηρείται θερμική κίνηση. Εάν η θερμοκρασία τείνει στο απόλυτο μηδέν, τα μόρια αρχίζουν να συσσωρεύονται σε ένα μέρος όπου η δυναμική ενέργεια παίρνει την χαμηλώτερη τιμή
- To αρνητικό πρόσημο έχει νόημα εφόσον η δυναμική ενέργεια που εισάγεται στο σύστημα είναι αρνητική για το περιβάλλον ενώ εάν εξάγεται δυναμική ενέργεια από το σύστημα προς τα έξω είναι αντίθετα
Με βάση την εξίσωση της δυναμικής Ενέργειας U=mgh γίνεται n= no exp(-U/kT)
Αυτή η εξίσωση είναι και ο Νόμος της κατανομής των σωματιδίων σύμφωνα με τις δυναμικές ενέργειες ή αλλοιώς η κατανομή Boltzman
Παραλλαγές και επεκτάσεις της κατανομής Boltzman
Aπό την εξίσωση n= no exp(-mgh/kT)
μπορούμε να αντικαταστήσουμε την σταθερά Boltzman k εφόσον k=m/μ .R
Ακόμα η πυκνότητα του αερίου δίνεται από τον τύπο  ,
,
και η εξάρτηση της πίεσης από το υψόμετρο είναι (z=h)  λέγεται βαρομετρικός τύπος
λέγεται βαρομετρικός τύπος
και αν h=z=0 ο αριθμός των σωματιδίων είναι ο Ν0
ακόμη αν θεωρήσουμε την καταστατική εξίσωση των αερίων με την μορφή  ,
,
αντικαθιστώντας στην πίεση φτάνουμε στην  .
.
εισάγωντας την Μοριακή Μάζα του αερίου (μοριακό Βάρος) γιατί έχουμε την σχέση  ,
,
αντίστοιχα αν δουλεύουμε με τις συγκεντρώσεις μπορούμε να χρησιμοποιούμε τον τύπο  ,
,
Από την κατανομή αυτή φαίνεται πως όσο ανεβαίνει το υψόμετρο η συγκέντρωση n(z) μειώνεται εκθετικά
Εργασίες πάνω σε αυτό έγιναν το 1908-1911 από τον Γάλλο φυσικό Jean-Baptiste Perrin για κατανομή μικροσκοπικών σωματιδίων στο εξωτερικό βαρυτικό πεδίο, οι οποίες έκαναν δυνατή την εφαρμογή του τύπου Boltzman για περιγραφή όχι μόνο μορίων αερίου αλλά και οποιωνδήποτε άλλων μικροσωματιδίων
Αν υποθέσουμε ότι έχουμε ένα ομογενές βαρυτικό πεδίο η παράσταση mgz είναι η δυναμική του ενέργεια, δηλαδή  .
.
αλλά κι αν επεκτείνουμε για κάθε σημείο.του χώρου, η δυναμική ενέργεια του βαρυτικού πεδίου γίνεται Επ (x,y,z)
και η κατανομή  , (Boltzman 1866)
, (Boltzman 1866)
υπό την προυπόθεση ότι  .
.
Αν pi είναι η πιθανότητα να βρεθούν ni σωματίδια στη ενεργειακή κατάσταση Ei τότε pi = nι/nο
Εφόσον πρόκειται για ιδανικό αέριο και η ενέργεια αλληλεπίδρασης είναι μηδαμινή ώστε μπορεί να αγνοηθεί και η κανονική κατανομή του Gibbs μετατρέπεται στην κατανομή του Boltzman.
Δ'ημητρα Σπανού
e−μgh
e−μgh
RT
n0e−μgh
RT
n=n0e−μghRT
ΠΗΓΕΣ
Κατανομή Boltzmann: Βαρομετρικός τύπος, Γραφική παράσταση, Συμπέρασμα
Διανομή Maxwell-Boltzmann | Επιστήμη | Φανατισμός
5.2. Распределение Больцмана | Физическая термодинамика | МГТУ им. Н.Э. Баумана. Кафедра физики
Ο Νόμος της Κατανομής Μοριακών Ταχυτήτων: Αρχές και Πρακτικές Εφαρμογές


