Δήμητρα Σπανού καθηγήτρια χημικός, συνταξιούχος Δευτερο/ιας Εκπ/σης από 30-6-2025
υπό κατασκευή
ΕΙΣΑΓΩΓΗ
Οι εξωτερικά μακροσκοπικές μεταβολές στην μάζα των σωμάτων βρίσκουν την ερμηνεία τους στον μικρόκοσμο των σωματιδίων της ύλης. Εκεί η μελέτη της συμπεριφοράς των σωματιδίων των κινήσεων και των αλληλεπιδράσεων θα δώσει τα στοιχεία για τον προσδιορισμό των εξωτερικών παραμέτρων.
Αυτά είναι θέματα που αφορούν την Επιστήμη της Στατιστικής που ασχολείται με την συλλογή και ανάλυση δεδομένων που διευκολύνουν την μελέτη και επεξεργασία προβλημάτων διαφόρων κλάδων της επιστήμης . Πιο συγκεκριμένα εδώ η Στατιστική Φυσική συστημάτων σωματιδίων χρησιμοποιεί κατά πολύ τις εξισώσεις, τα στατιστικά στοιχεία και κατανομές στην μελέτη τους.
Η γνώση της κατανομής των σωματιδίων σε ένα σύστημα καθιστά δυνατή την εύρεση των μέσων τιμών διαφόρων χαρακτηριστικών ενός θερμοδυναμικού συστήματος με την βοήθεια της Μαθηματικής Φυσικής
Έτσι δίνεται η δυνατότητα να γιίνει καλύτερα κατανοητή η χημική τους δραστηριότητα. Δ.Σ
Συνέχεια από την κανονική κατανομή Gibbs ...
Οι κατανομές Μaxwell και Boltzman έχουν προέλευση από την κατανομή Gibbs που σύμφωνα με τον γενικό τύπο P(x) =(1/Z)*exp(-E(x)/kT
η κατανομή Gibbs είναι F(qi, pi) =Aexp(-H(qi, pi)/kT )
Η H (qi, pi) είναι η Χαμιλτονιανή συνάρτηση
και Α είναι η κινητική και η δυναμική ενέργειά του
Αν θεωρήσουμε ιδανικό αέριο σε ένα ομογενές πεδίο κάθε μόριο έχει Κινητική λόγω της μεταφορικής κίνησης Εκιν και δυναμική ενέργεια U που εξαρτάται από τη θέση του τότε η ολική του ενέργεια είναι το άθροισμα των δύο
Εολ = Εκιν + Εδυν και Εδυν = U(x, y, z)
Αν θεωρήσουμε ότι στο σώμα υπάρχουν αλληλεπίδρασεις μεταξύ των σωματιδίων , ανάλογα με τους βαθμούς ελευθερίας κάθε μικροσωματιδίου, η παραπάνω σχέση γίνεται
Εολ =Εκιν + Εδυνεξ + Εδυν σωμ ,
Η ΚΑΝΟΝΙΚΗ ΚΑΤΑΝΟΜΗ
Στη Στατιστική Μηχανική η κανονική κατανομή χρησιμοποιείται συχνά για να περιγράψει συστήματα σε θερμοδυναμική ισορροπία, σε σταθερή θερμοκρασία, όγκο με σταθερό αριθμό σωματιδίων που ανταλλάσει ενέργεια με το περιβάλλον. Αυτή η κατανομή παίζει σημαντικό ρόλο στη θεωρία των στατιστικών συνόλων και αποτελεί βάση για την περιγραφή πολλών φυσικών διεργασιών όπως η θερμική αγωγιμότητα, η διάχυση και οι αντιδράσεις χημικής ισορροπίας
Η κανονική κατανομή συστήματος με ενέργεια Ει καθορίζεται από τον τύπο: P(Ei) = 1/Z exp(-βEi) όπου β=1/kbT με kb σταθερά Boltzman και Ζ είναι κι αυτή συνάρτηση κατανομής που ονομάζεται στατιστικό άθροισμα το οποίο κανονικοποιεί την κατανομή ώστε το άθροισμα όλων των περιοχών των πιθανών καταστάσεων να είναι ίσο με 1 Ζ = ∑ie−βΕi
Η συνάρτηση κατανομής Ζ είναι σημαντική γιατί από αυτό το σύνολο εξαρτώνται θερμοδυναμικά μεγέθη του συστήματος όπως η πίεση, η ελεύθερη ενέργεια , η εντροπία και η πίεση
- ΘΕΡΜΟΔΥΝΑΜΙΚΟΙ ΠΑΡΑΜΕΤΡΟΙ ΠΟΥ ΜΠΟΡΟΥΝ ΝΑ ΕΚΦΡΑΣΤΟΥΝ ΜΕΣΩ ΤΗΣ ΚΑΝΟΝΙΚΗΣ ΚΑΤΑΝΟΜΗΣ ΚΑΙ ΔΙΝΟΥΝ ΤΗ ΣΧΕΣΗ ΜΕΤΑΞΥ ΜΙΚΡΟΣΚΟΠΙΚΩΝ ΙΔΙΟΤΗΤΩΝ ΚΑΙ ΜΑΚΡΟΣΚΟΠΙΚΩΝ ΘΕΡΜΟΔΥΝΑΜΙΚΩΝ ΠΑΡΑΜΕΤΡΩΝ
- Η μέση ενέργεια του συστήματος ως σταθμισμένος μέσος όρος όλων των δυνατών ενεργειών: ⟨E⟩=ΣP(Ei)Ei=1/ZΣEiexp(-βΕi)
- Η ελεύθερη ενέργεια F του συστήματος ως F= -kβΤλνΖ H ελεύθερη ενέργεια καθορίζει το έργο που μπορεί να επιτελέσει το σύστημα υπό σταθερή θερμοκρασία
- Η Εντροπία S ενός συστήματος σε κανονικό σύνολο μπορεί να εκφραστεί με την ελεύθερη ενέργεια f και την μέση ενέργεια ⟨E⟩
O NOMOΣ ΤΗΣ ΚΑΤΑΝΟΜΗΣ ΜΟΡΙΑΚΩΝ ΤΑΧΥΤΗΤΩΝ ΣΥΜΦΩΝΑ ΜΕ ΤΟΥΣ MAXWELL- BOLTZMAN
Είναι η στατιστική κατανομή για την περιγραφή φυσικών συστημάτων με μεγάλο αριθμό μη αλληλεπιδρώντων σωματιδίων που κινούνται σύμφωνα με τους νόμους της κλασσικής μηχανικής, (όπως κατανομή μορίων ιδανικού αερίου) και βρίσκονται σε καταστάσεις θερμοδυναμικής ισορροπίας.
Βασική ιδέα του νόμου είναι ότι τα μόρια ενός αερίου κινούνται με διάφορες ταχύτητες όμως οι ταχύτητες αυτές κατανέμονται σύμφωνα με τον νόμο της κατανομής των ταχυτήτων.
Η κατανομή Maxwell- Boltzman ισχύει μόνο για ιδανικά αέρια αφού σε πραγματικά υπάρχουν αλληλεπιδράσεις όπως δυνάμεις van der waals, κβαντικές ή αλληλεπιδράσεις ανταλλαγής.
Η κατανομή είναι ως προς τις συντεταγμένες και την ταχύτητα σε συνθήκες θερμικής ισορροπίας σε αυθαίρετο εξωτερικό πεδίο δύναμης.
Κάθε μόριο του αερίου αυτού έχει την κινητική του ενέργεια και επιπλέον μια δυναμική U(x,y,z) λόγω της επίδρασης που ασκεί το εξωτερικό δυναμικό πεδίο στην θέση του
Ο νόμος δείχνει ότι ο αριθμός σωματιδίων σε υψηλή ενέργεια μειώνεται εκθετικά και η κατανομή εξαρτάτα από τη θερμοκρασία την μάζα των σωματιδίων και την δυναμική ενέργεια
Συνδυάζει την κατανομή Maxwell σωματιδίων που έχουν μόνο την κινητική ενέργεια και την κατανομή Boltzan σωματιδίων υπό την επίδραση εξωτερικού πεδίου και με μηδενική κινητική ενέργεια.
Σωματίδια κινούνται μέσα σε ένα κλειστό ακίνητο δοχείο χωρίς να αλληλοεπιδρούν μεταξύ τους εκτός από στιγμιαίες συγκρούσεις κατά τις οποίες ανταλλάσουν μεταξύ τους ή με το περιβάλλον ορμή και ενέργεια έχοντας φτάσει σε θερμοδυναμική ισορροπία
Η ΣΥΝΑΡΤΗΣΗ ΤΗΣ ΚΑΤΑΝΟΜΗΣ ΠΙΘΑΝΟΤΗΤΑΣ ΤΑΧΥΤΗΤΩΝ ΣΩΜΑΤΙΔΙΩΝ
Εδώ παίρνουμε την κατανομή Maxwell- Boltzman για μια κατανομή πιθανότητας ταχυτήτων των σωματιδίων του συστήματος
Η συνάρτηση κατανομής πιθανότητας ταχυτήτων στις τρεις διαστάσεις 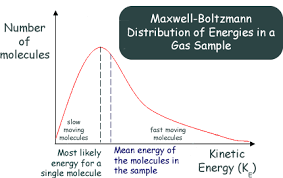
(Μπορεί να προκύψει από την κατανομή Gibbs στην οποία κάθε μόριο έχει συνολική ενέργεια )
Η κατανομή ταχυτήτων εξαρτάται από την θερμοκρασία ακαι από την μάζα των μορίων των αερίων. Ελαφρύτρα μόρια έχουν συνήθως υψηλότερες ταχύτητες ενώ βαρύτερα χαμηλώτερες.
Γνωρίζοντας ότι η ενεργειακές καταστάσεις του συστήματος εξαρτώνται από την θερμοκρασία Τ
παρατηρούμε ότι Σε διαφορετικές θερμοκρασίες οι καμπύλες διαφέρουν
Η ΣΤΑΤΙΣΤΙΚΗ ΤΩΝ MAXWELL- BOLTZMAN ΓΙΑ ΤΟΝ ΜΕΣΟ ΑΡΙΘΜΟ ΣΩΜΑΤΙΔΙΩΝ ΠΟΥ ΒΡΙΣΚΟΝΤΑΙ ΣΕ ΔΟΣΜΕΝΗ ΜΙΚΡΟΚΑΤΑΣΤΑΣΗ
Εδώ εξετάζεται το ποσοστό των σωματιδίων ως προς τον συνολικό αριθμό τους, τα οποία βρίσκονται σε μια συγκεκριμένη μικροκατάσταση. (υπό ορισμένες προυποθέσεις ). Ισχύει ότι:
Τα σωματίδια α. δεν αλληλεπιδρούν β. Θεωρείται ότι μετά την πάροδο χρόνου οι μοριακές κρούσεις τείνουν προς ισορροπία.
Η σχέση αυτή μπορεί να γραφεί και ως εξίσωση
(Ni o αναμενόμενος αριθμός σωματιδίων στη μικροκατάσταση i. Ν ο συνολικός αριθμός σωματιδίων στο σύστημα, Εi η ενέργεια της μικροκατάστασης i, Τ η θερμοκρασία ισορροπίας του συστήματος, k η σταθερά του Boltzman
Στο διάγραμμα κάτω, βλέπουμε στην Maxwell-Boltzman κατανομή, τον αριθμό των σωματιίων στις διάφορες ταχύτητες της κίνησής τους
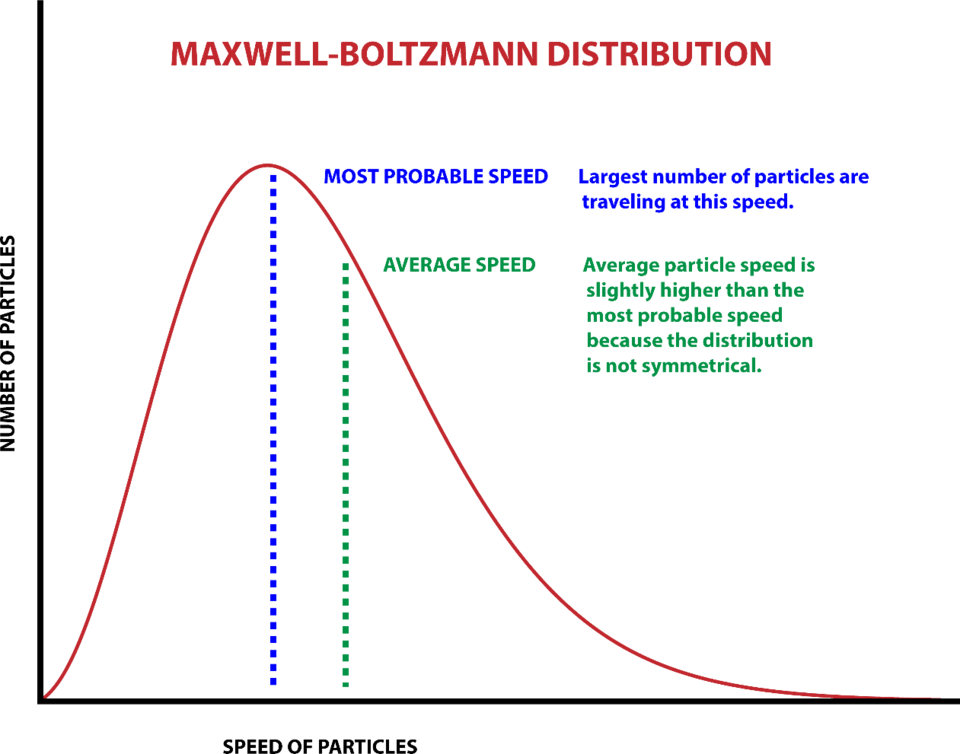
Σε ένα απειροστό διάστημα του τρισδιάστατου χώρου των ταχυτήτων (υx, υy, υz) με κέντρο ένα διάνυσμα μέτρου υ, το κλάσμα των σωματιδίων που βρίσκονται είναι f(υ)d3υ όπου dυ3= dυx, .d υy .dυz και ισχύει
και εφόσον ισχύει η συμμετρία προς όλες τις διευθύνσεις και έχοντας ορίσει την θερμοκρασία σαν Τ, ισχύει
Η ΣΥΝΑΡΤΗΣΗ ΠΥΚΝΟΤΗΤΑΣ ΠΙΘΑΝΟΤΗΤΑΣ
Με τον πολλαπλασιασμό της πυκνότητας πιθανότητας με την πυκνότητα των σωματιδίων φτάνουμε σε μια επόμενη σχέση στην οποία δίνεται η κατανομή πιθανότητας των ταχυτήτων σαν την συνάρτηση πυκνότητας πιθανότητας που δίνει την πιθανότητα ανά μονάδα ταχύτητας να βρούμε ένα σωματίδιο με ταχύτητα κοντά στη υ
Η συνάρτηση πυκνότητας πιθανότητας προκύπτει αν η κατανομή πιθανότητας πολλαπλασιαστεί με την πυκνότητα των σωματιδίων (αριθμητική πυκνότητα) ορίζεται ως η παράγωγος της αθροιστής συνάρτησης κατανομής
.jpg)
Δήμητρα Σπανού
ΠΗΓΕΣ
Κανονική και Κύρια Κανονική Διανομή | Κβαντομηχανική. Σχολικό βιβλίο
https://el.wikipedia.org/wiki/%CE%9A%CE%B1%CF%84%CE%B1%CE%BD%CE%BF%CE%BC%CE%AE_%CE%9C%CE%AC%CE%BE%CE%B3%CE%BF%CF%85%CE%B5%CE%BB-%CE%9C%CF%80%CF%8C%CE%BB%CF%84%CF%83%CE%BC%CE%B1%CE%BD
Κατανομή Boltzmann: Βαρομετρικός τύπος, Γραφική παράσταση, Συμπέρασμα
Διανομή Maxwell-Boltzmann | Επιστήμη | Φανατισμός
Ο Νόμος της Κατανομής Μοριακών Ταχυτήτων: Αρχές και Πρακτικές Εφαρμογές

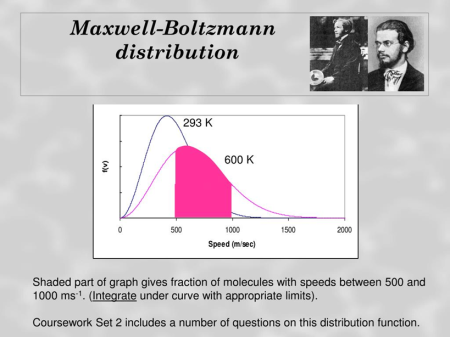



 (Ni o αναμενόμενος αριθμός σωματιδίων στη μικροκατάσταση i. Ν ο συνολικός αριθμός σωματιδίων στο σύστημα, Εi η ενέργεια της μικροκατάστασης i, Τ η θερμοκρασία ισορροπίας του συστήματος, k η σταθερά του Boltzman
(Ni o αναμενόμενος αριθμός σωματιδίων στη μικροκατάσταση i. Ν ο συνολικός αριθμός σωματιδίων στο σύστημα, Εi η ενέργεια της μικροκατάστασης i, Τ η θερμοκρασία ισορροπίας του συστήματος, k η σταθερά του Boltzman
