Δήμητρα Σπανού χημικός, καθηγήτρια Δ/θμιας Εκπ/σης με οργανική θέση στο 1ο Γυμνάσιο Δάφνης
συνταξιούχος από 30-6-2025
ΕΙΣΑΓΩΓΗ
ΕΝΥΔΡΕΣ ΟΥΣΙΕΣ ΣΤΗΝ ΧΗΜΕΙΑ
Στην Χημεια, ενυδρες ουσίες είναι εκείνες που περιέχουν νερό, τα μόρια του νερού συνδέονται με άλλα μόρια ή ιόντα
- σε αντίθεση με τις ανυδρες-
ΤΥΠΟΙ ΕΝΥΔΡΩΝ ΟΥΣΙΩΝ
Υπάρχουν ανόργανες ένυδρες ενώσεις και οργανικές ένυδρες ενώσεις
Στις ανόργανες ένυδρες το νερό συνδέεται με ανόργανα μόρια ή ιόντα (Ιοντικά ένυδρα)
Στις οργανικές ένυδρες το νερό συνδέεται με οργανικά μόρια
Τα ένυδρα αέρια (κλαθρικά) που σχηματίζονται όταν αέρια εγκλωβίζονται σε υδατικά κρυσταλλικά πλέγματα
Ένυδρα μπορεί να είναι στερεά διαλύματα που περιεχουν μοριακό κρυσταλλικό νερό όπως ανόργανα ένυδρα κρυσταλλικά άλατα.
Ένυδρα επίσης είναι σύμπλοκα που διαθέτουν συνδέτες νερού, κεντρική, γεφυρωμένη ή χηλική σύνδεση
ΣΥΝΔΕΣΙΜΟΤΗΤΑ ΤΩΝ ΜΟΡΙΩΝ ΤΟΥ ΝΕΡΟΥ ΣΤΟΥΣ ΚΡΥΣΤΑΛΛΟΥΣ
ΤΡΟΠΟΣ ΣΥΝΔΕΣΗΣ ΤΟΥ ΝΕΡΟΥ
Στα ένυδρα, το νερό μπορεί να είναι συνδεδεμένο με δεσμούς υδρογόνου ή διαμοριακές δυνάμεις ή να τοποθετείται εσωτερικά (ενσωμέτωση) εάν αυτό σταθεροποιεί το κρυσταλλικό πλέγμα.
Η ΕΝΥΔΑΤΩΣΗ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ
Α. Άμεση ένωση νερού με χημικές μέσω χημικών αντιδράσεων
Β. Ένωση της ουσίας με το νερό με την συμμετοχή άλλων χημικών ουσιών (ενυδατικές ουσίες)
Γ. Καταστροφή των μορίων του νερού. Απορρόφησή τους στα προϊόντα της αντίδρασης. Υδρόλυση και αποσύνθεση
Η ενυδάτωση που μπορεί να επιρρεάσει την δραστικότητα χημικών ουσιών, αλλά και τις φυσικές τους ιδιότητες και είναι πολύ σημαντική στα βιολογικά συστήματα μπορεί να πραγματοποιηθεί:
ΕΝΥΔΑΤΩΣΗ ΟΥΣΙΩΝ ΜΕ ΧΗΜΙΚΕΣ ΔΙΑΔΙΚΑΣΙΕΣ

Α Προσθήκη νερού σε μόρια οργανικών ουσιών
α.Ενυδάτωση πρωτεϊνών. (σχήμα αριστερά)Οι πρωτεϊνες δεσμεύουν εύκολα το νερό. Οι Η απορρόφηση νερού από τις πρωτεϊνες συνδέεται με την διόγκωση την διαλυτότητα, την καθίζηση και την μετουσίωση. Το νερό συγκρατείται από την πρωτεϊνη λόγω σχηματισμού δεσμών υδρογόνου

β. Ενυδάτωση ακόρεστων οργανικών ουσιών (σχήμα δεξιά)
Προσθήκη νερού σε οργανικές ακόρεστες ενώσεις όπως αλκένια
Προσθήκη νερού σε ακόρεστες μονουδρικές αλκοόλες προς γλυκόλες
CH2=CH(OH) +H2O -H+--> CH2(OH)CH2(OH)
Β. Χημικές Αντιδράσεις ενυδάτωσης που πραγματοποιούνται με συμμετοχή άλλων ουσιών (ενυδατικές ουσίες)
 ΟΞΙΝΕΣ ΚΑΙ ΒΑΣΙΚΣΕ ΟΥΣΙΕΣ
ΟΞΙΝΕΣ ΚΑΙ ΒΑΣΙΚΣΕ ΟΥΣΙΕΣ
Συνήθως η ενυδάτωση ενισχύεται σε όξινο ή βασικό περιβάλλον γιατί τα Η+ ή τα ΟΗ- προσκολλώνται σε πρωτονιόφιλες ή ηλεκτρονιόφιλες ομάδες της ουσίας με συνέπεια να χαλαρώνουν υπάρχοντες χημικούς δεσμούς και να ενισχύουν την προσκόληση μορίων νερού.
Οι ενυδατικές ουσίες συμμετέχουν στην αντίδραση αλλά παραμένουν αμετάβλητες στο τέλος .
Έτσι κατά την αντίδραση προσθήκης νερού στην αιθυλική αλκοόλη, η ενυδατική ουσία είναι το θειϊκό οξύ που αντιδρά στις ακόλουθες εξισώσεις.
CH3CH2ΟΗ+ H(HSO4) -> CH2(HSO4) -CH2-ΟΗ
Στη συνέχεια των αντιδράσεων αυτών μπορεί να περιλαμβάνεται την περίπτωση Γ.
ΨCH2(HSO4) -CCH2-ΟΗCH3-CH2(HSO4) + H2O -> CH3-CH2(OH) + H(HSO4)
Το θειϊκο οξύ δρα σαν καταλύτης επιτρίποντας την ταχύτερη αντίδραση ενυδάτωσης

Γ. Ενυδάτωση με ταυτόχρονη καταστροφή μορίων νερού . Απορρόφησή τους στα προϊόντα της αντίδρασης . Υδρόλυση
οι όξινοι και αλκαλικοί, ανόργανοι και οργανικοί ανυδρίτες. Η προσθήκη νερού σε ανυδρύτες οξέων ή βάσεων

Ενυδάτωση και Υδρόλυση:
Τα πρωτοταγή και δευτεροταγή αμίδια R(-C=OCNH2) είναι κυρίως στερεές κρυσταλλικές ουσίες ενώ τα τριτοταγή είναι υγρά.
Γενικα, ο δεσμός του αμιδίου παρέχει δομική ακαμψία και αντιστέκεται στην υδρόλυση όπως νάϋλον(πολυαμίδιο), αραμίδιο. Σε βιοχημικό επίπεδο οι δεσμοί του αμιδίου ονομάζονται πεπτιδικοί δεσμοί και είναι οι δεσμοί που συνδέει τα αμινοξέα ώστε να δημιουργούν πρωτεϊνες. (-CO-ΝΗ-). Η εξήγηση είναι πως οι ενώσεις αυτές, εμφανίζουν μεσομέρια μεταξύ του διπλού δεσμού του καρβονυλίου και ενός μερικού διπλού δεσμού αζώτου - άνθρακα  και λόγω της σταθεροποίησης της μεσομέρειας αυτής, τα αμίδια δεν υδρολύονται εύκολα
και λόγω της σταθεροποίησης της μεσομέρειας αυτής, τα αμίδια δεν υδρολύονται εύκολα
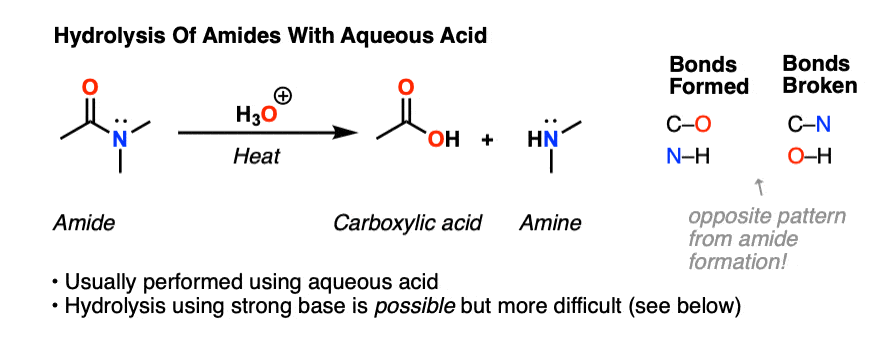
Όμως σε όξινο ή βασικό περιβάλλον ή και με θέρμανση τα αμίδια υδρολύονται σε καρβοξυλικά οξέα και αμμωνία. Τα οξέα και οι βάσεις δρουν καταλυτικά, εφόσον μειώνεται η ενέργεια ενεργοποίησης με την παρουσία τους επειδή επιδρούν σε δέκτες ηλεκτρονίων ή πρωτονίων κι έτσι χαλαρώνει ο δεσμός C-N και υδρολύονται στη συνέχεια.
Η ΑΦΥΔΑΤΩΣΗ ΟΡΓΑΝΙΚΩΝ ΟΥΣΙΩΝ
Α. Παρασκευή συμμετρικών αιθέρων από αφυδάτωση αλκοολών
Οι συμμετρικοί αιθέρες που περιέχουν μικρότερες αλκυλομάδες στη βιομηχανία παρασκευάζονται από αφυδάτωση αλκοολών με κατάλυση από οξέα. Ο σημαντικότερος είναι ο διαιθυλαιθέρας. Άλλοι είναι ο διισοπροπυλαιθέρας και ο δι-η-βουτυλαιθέρας
Χρησιμοποιούνται στους 140οC τα οξέα πθειϊκό ή κατά Lewis BF3, ALCL3, ZnCl2
CH3CH2OH (140oC, ΟΞΙΝΟ) -> CH3CH2OCH2CH3 +H2O
Β. Εστεροποίηση οξέων και αλκοολών με αποβολή νερού
Οι εστέρες κατώτερων καρβοξυλικών οξέων και αλκοολών είναι σώματα υγρά και πτητικά ενώ οι εστέρες ανώτερων καρβοξυλικών οξέων είναι ουσίες κηρώδεις και άοσμες. 
Οι εστέρες είναι κυρίως προϊόντα συμπύκνωσης οξέων και αλκοολών (ή φαινολών) με την αποβολή ενός μορίου νερού και την δημιουργία εστερικού δεσμού. (C=O-O-C-).
Η εστεροποίηση
Είναι αντίδραση ισορροπίας και ο σχηματισμός τους ευνοείται αν ένα από τα αντιδρώντα βρίσκεται σε περίσσεια καθώς και από την παρουσία κατιόντων υδρογόνου ( μειώνεται η ενέργει ενεργοποίησης με την παρουσία τους) και απο την αφαίρεση νερού. (Προσθήκη Πυκνού θειϊκου οξέος). Ευκολα γίνεται κατανοητό ότι οι εστέρες είναι πολύ λίγο διαλυτοί στο νερό
Αντίθετα η προσθήκη νερού ευνοεί την αντίδραση προς την αντίθετη κατεύθυνση και συντελεί στην υδρόλυση του εστέρα.
ΥΔΡΟΛΥΣΗ ΟΡΓΑΝΙΚΩΝ ΟΥΣΙΩΝ (διάσπαση δεσμού με προσθήκη νερού)
α. Υδρόλυση πολυπεπτιδίων (ενζυμική διάσπαση πεπτιδικού δεσμού προσθήκη νερού )
Οι πεπτιδικοί δεσμοί (-CO-ΝΗ-) που αμιδικοί δεσμοί και είναι μοριακά γνωρίσματα των πρωτεϊνών, υδρολύονται παρουσία ενζύμων
β. Υδρόλυση λιπών και ελαίων σε γλυκερόλη και λιπαρά οξέα
γ. Υδρόλυση πολυσακχαριτών σε απλούστερα σάκχαρα
.jpg)
Δήμητρα Σπανού
ΠΗΓΕΣ
Amids - Βικιπαίδεια (wikipedia.org)
Αντίδραση ενυδάτωσης στη χημεία: αρχές και παραδείγματα (helpdoma.ru)
Αντίδραση ενυδάτωσης στη χημεία: αρχές και παραδείγματα (helpdoma.ru)
Υδρόλυση - Βικιπαίδεια (wikipedia.org)
Ενυδάτωση πρωτεϊνών (studopedia.su)
Prof. Blumes Medienangebot: Komplexverbindungen (chemieunterricht.de)
https://studref.com/609077/matematika_himiya_fizik/reaktsiya_eterifikatsii


j.gif)
