Της Δήμητρας Σπανού, Χημικού, καθηγήτριας Δευτεροβάθμιας Εκπαίδευσης 1ου Γυμνάσιο Δάφνης
Μελετώντας την δράση των συνενζύμων γίνεται φανερό περισσότερο από κάθε άλλη φορά, πόσο οι λειτουργίες των οργανισμών και οι βιοχημικές αντιδράσεις είναι αλληλοεξαρτώμενες και η μια είναι συνέχεια της άλλης.
Πολλά ένζυμα χρειάζονται συμπαράγοντες για να δραστηριοποιηθούν. Συμπαράγοντες μπορεί να είναι συνένζυμα ή και μέταλλα. Αν είναι σφικτά συνδεδεμένα στο ένζυμο ονομάζονται προσθετικοί παράγοντες.
Μιλώντας για ένζυμα πρωτεινικής φύσης και τα συνένζυμά τους, μπορούμε να πούμε ότι οι μεν πρωτείνες του ενζύμου κατευθύνουν το ένζυμο για να αναζητήσει το κατάλληλο υπόστρωμα οι συμπαράγοντες (συνένζυμα) ρυθμίζουν το είδος της ενζυμικής δράσης που θα γίνει. Ακόμα γίνεται φανερό, ότι συμβαίνουν αλληλοεξαρτώμενες διαδικασίες και πως η δράση ενός ενζύμου σταματά, εκεί που αρχίζει η δράση ενός άλλου κ.ο.κ. έτσι δεν μιλάμε πια για ένζυμα, αλλά για ολόκληρα Ενζυμικά Συστήματα. 
Τα συνένζυμα είναι μικρό οργανικά μόρια που είναι απαραίτητο να συνδεθούν με ορισμένα ένζυμα ώστε τα ένζυμα αυτά να ενεργοποιηθούν
Πολλά συνένζυμα είναι παράγωγα βιταμινών και σχεδόν όλα περιέχουν στο μόριό τους φωσφορικό οξύ
Το συνένζυμο και το ένζυμο μαζύ ονομάζεται ολοένζυμο
Οι συμπαράγοντες κατατάσσονται σε ομάδες που είναι ανάλογες με τις έξη ομάδες που κατατάσσονται τα ένζυμα: Οξειδοαναγωγάσες, τρανφεράσες, ισομεράσες, υδρολάσες, λιγάσες και λυάσες
1. Συνένζυμα των ενζύμων οξειδοαναγωγικών συσημάτων με ένζυμα τις (οξειδοαναγωγάσες)
Από τα πιο σημαντικά οξειδοαναγωγικά συστήματα των ιστών είναι α. των πυρινονουκλεοτιδίων β. των φλαβοπρωτεινών γ. των κυτταχρωμάτων. Υπάρχουν όμως και άλλα τέσσερα που είναι του ασκορβικού οξέος, του λιποικού οξέος, του γλουταθείου και τα σύστημα κατεχόλης και ο κινόνης
Σε ορισμένες περιπτώσεις απαιτείται η συμμετοχή ενός μόνο οξειδοαναγωγικού συστήματος, όπως κατά την οξείδωση των α αμινοξέων που συμμετέχουν μόνο οι φλαβοπρωτείνες. Στις περισσότερες περιπτώσεις συμμετέχουν περισσότερα συστήματα όπως στην περίπτωση που συμμετέχουν οι δευδρογονάσες και στην συνέχεια οι φλαβοπρωτείνες
α. οξειδοαναγωγικά συστήματα των πυρινονουκλεοτιδίων αποτελούνται από αδενίνη, νικοτιναμίνη, φωσφορικό οξύ και ριβόζη.
Τα συνένζυμα NAD+ και NADP+
Είναι τα νουκλεοτίδια του νικοταναμίδιου NAD+ και NADP+(της ομάδας Β2). μεταφέρουν Υδρογόνο και γι αυτό η δράση τους συνδέεται με των ενζύμων δευδρογονασών . Έτσι τα συνένζυμα αυτά καλούνται και συνδευδρογονάσες



NAD+ Νικoτιvαµιδo-αδεvιvo διvoυκλεoτίδιo (παλιά TPN) NADP+ Νικoτιvαµιδo-αδεvιvo (φωσφoρικό) διvoυκλεoτίδιο (παλιά TPNP) Είναι παράγωγα του νικοτινικού οξέος και η βιταμίνη που περιέχεται στο μόριο είναι η νιασίνη
- Τα NAD+ και NADP+ μεταφέρουν υδρογόνα μεταξύ του μεταβολίτου και των φλαβινοπρωτειδών (με την βοήθεια του ενζύμου δευδρογενάση του μεταβολίτη)
επειδή οι φλαβοπρωτείνες FMN και FAD σαν πιο αναγωγικές ουσίες από τις NAD+ και NADP+ αποσπούν από αυτές τα υδρογόνα και τις επαναφέρουν στην αρχική τους κατάσταση (ανάκτηση του συνενζύμου)
μεταβολίτης.2Η +NAD+ (ή NADP) δίνουν οξειδωθείσα μορφή μεταβολίτη + NAD2Η+ (ή NADP2Η)
NAD2Η+ (ή NADP2Η) με επίδραση FMN (ή FAD) δίνουν NAD (ή NADP) και FMNΗ2 (ή FADΗ)

- Στην συνέχεια μπορούν να αποδόσουν τα Υδρογόνα αυτά σε φλαβοπρωτείδες και να επανέλθουν στην αρχική τους κατάσταση. Τα ένζυμα που θα δράσουν για την μεταφορά των Υδρογόνων των NAD2Η+ (ή NADP2Η) στις φλαβοπρωτείνες είναι οι NAD2Η+ (ή NADP2Η) αφυδρογονάσες
β. τα φλαβινοσυνένζυμα FMN και FAD
Οι φλαβοπρωτεινών (που βρίσκονται στον καρδιακό μυ, στο γάλα και τον κρόκο αυγού) ,Αποτελούνται από τα φλαβινοσυνένζυμα FMN και FAD, τις προσθετικές ομάδες των , την βιταμίνη ριβοφλαβίνη και ριβιτόλη.
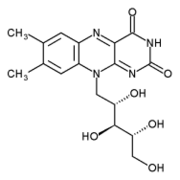

είναι ισχυρότερο οξειδωτικό από το NAD , οξειδώνει
- το NADH στην αναπνευστική αλυσίδα , επαναφέρει δηλαδή τις ανηγμένες μορφές τους στην αρχική τους κατάσταση (NAD) .
- Επίσης και δημιουργεί διπλό δεσμό αναγόμενο σε FADΗ . Στον κύκλο του Krebs το ηλεκτρικό οξύ (succinate) μετατρέπεται σε ηλεκτρικό
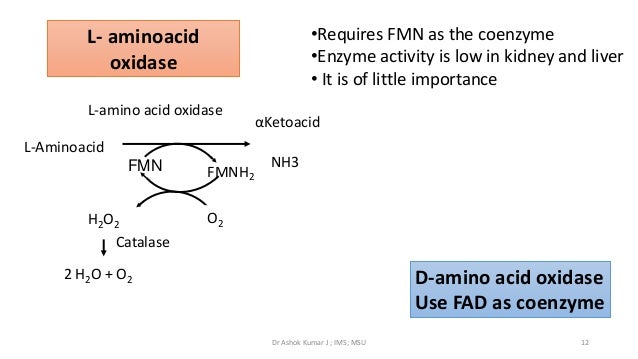
Οι ανηγμένες φλαβοπρωτείνες
μπορούν να οξειδωθούν στην συνέχεια από το μοριακό οξυγόνο.

Επανέρχονται έτσι στην αρχική τους κατάσταση. Γι αυτόν τον λόγο οι φλαβοπρωτείνες αποτελούν ουσιαστικό παράγοντα για την μεταφορά του Υδρογόνου προς το Οξυγόνο .
Η αναγωγική δύναμη αυτών των συνενζύμων είναι η μεταφορά των Η+ και e-
Κατά τον καταβολισμό τους το μακρομόρια της τροφής διασπώνται σε απλούστερες ενώσεις με παράλληλη απελευθέρωση ενέργειας κυρίως

μέσα από οξειδωτικές διαδικασίες κατά τις οποίες παρέχουν τα ηλεκτρόνιά τους και τα υδρογόνα στα συνένζυμα NAD+, FAD,τα οποία ανάγωνται σε NADH, FADH2.
Στην συνέχεια πρέπει να επανέλθουν στην αρχική τους κατάσταση με μια δεύτερη αντίδραση
Ένζυμα που μεταφέρουν υδρογόνο (διάσπαση γλυκόζης, κ.α.) χρησιμοποιούν σαν συνένζυμα οργανικές ενώσεις , παράγωγα του συμπλέγματος Β που δρουν σαν φορείς υδρογόνου και ηλεκτρονίων τα κυριότερα των οποίων είναι το NAD+ το NADP+, και το FAD.
γ. Κυτοχρώματα (Οι αιμοπρωτείδες των κυττάρων)
. Είναι πρωτείνες των κυττάρων πολύ ανάλογα στην δομή τους με την αιμοσφαιρίνη του αίματος. Συνδέονται με βιολογικές μεμβράνες . Συναντώνται στις μεμβράνες του ενδοπλασματικού δικτύου, των μιτοχονδρίων και των χλωροπλαστών καθώς επίσης και των βακτηρίων. Το είδος τους διακρίνεται από το διαφορετικό μήκος κύματος που απορραφά. Βρέθηκαν αρχικά, τρεις ανάλογες πρωτείνες η α. η β. και για αυτό ονομάστηκαν κυτταχρώματα.

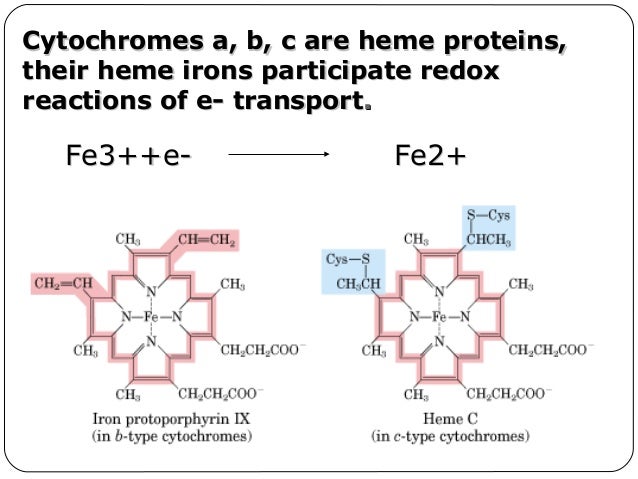
Περιέχουν σαν προσθετική ομάδα, τον δακτύλιο της πρωτοπορφυρίνης ενωμένης με σίδηρο και μεταφέρουν φορτίο (ηλεκτρόνια) όχι άτομα.
Μπορούν να μεταφέρουν ηλεκτρόνια μέσω της πρωτοπορφυρίνης , με την αλλαγή του δισθενούς σιδήρου σε τρισθενή (σιδηροπορφυρίνες) αλλά όχι υδρογόνα.
Δρουν στο κύτταρο κατά τον μεταβολισμό των ουσιών που έχουν καταλήξει εκεί από τις τροφές, (μεταβολίτες). Τα κυτοχρώματα μπορούν να αφαιρέσουν ηλεκτρόνια 1.από τους μεταβολίτες , 2. από τα NAD και NADP (πυριδινονουκλεοτίδια) και 3.από τα FNM και FAD (φλαβονονουκλεοτίδια)
Ανάλογα με τον τρόπο που ενώνεται η προσθετική ομάδα με την πρωτείνη τα κυτοχρώματα κατατάσσονται σε διάφορους τύπους
Cyta , Cytb,Cytc κ.λπ. Το Cytc είναι συνήθως οξειδοτικότερο από το Cytb
Σε κάθε μεταφορά ηλεκτρονίων ελευθερώνεται ενέργεια. Ένα μέρος από την ενέργεια αυτή μετατρέπεται σε θερμότητα και το υπόλοιπο αποθηκεύεται υπό μορφή δεσμών υψηλής ενέργειας στο ATP.
- Κατά την κυτταρική αναπνοή στο μιτοχόνδριο μεταβολίτες μέσω των ενζύμων δευδρογονάσων ελευθερώνουν υδρογόνο (ελευθερώνονται και 9,2 Kcal)
- και μέσω συνενζύμων όπως το NAD απομακρύνεται αυτό το υδρογόνο. Στην συνέχεια το υδρογόνο παραλαμβάνουν φλαβοπρωτείνες.(ελευθερώνονται και 4,6 Kcal)
- Το οξυγόνο που μεταφέρεται από την οξυαιμοσφαιρίνη, και αποδεσμεύεται στο πλάσμα (για λόγους που κυρίως συνδέονται με την μερική πίεση του οξυγόνου στο εκάστοτε περιβάλλον) και από το πλάσμα απορροφάται από τους ιστούς
- Η φλαβοπρωτείνη ελευθερώνει πρωτόνια στο περιβάλλον και ηλεκτρόνια τα οποία περνούν στα κυτοχρώματα β στο c (ελευθερώνονται και 11,6 Kcal)
- και τελικά στο α (ελευθερώνονται και 2,3 Kcal)
- και το α στην συνέχεια τα μεταφέρει στο οξυγόνο. (ελευθερώνονται και 23,1 Kcal)
- Το οξυγόνο ενώνεται με το υδρογόνο για να δώσουν νερό
- Η συνολική ενέργεια που ελευθερώνεται από την απόσπαση ζεύγους ηλεκτρονίων από έναν μεταβολίτη και την μεταφορά του στο οξυγόνο είναι συνολικά 50,8 Kcal.
δ. το λιποικό οξύ
To λιποικό οξύ δρα σαν συνπαράγοντας , στο πολυενζυμικό σύστημα της πυροσταφυλικής αφυδρογονάσης κατά την μετατροπή του πυροσταφυλικού οξέος σε ακετοσυνένζυμοΑ.  Συνδέεται ομοιοπολικά με
Συνδέεται ομοιοπολικά με
έναν αμιδικό δεσμό σε ένα τερματικό υπόλειμμα λυσίνης του συμπλόκου ενζύμου. Το πολυενζ υμικό σύστημα αυτό, αποτελείται από επιμέρους ένζυμα την πυροσταφυλική θειαμίνη, το λιποαμίδιο και το FAD . Το λιποικό οξύ είναι συνπαράγοντας και σε άλλα ενζυμικά συστήματα , δύο από αυτά είναι στον κύκλο του Κρεμπς, το ενζυμικό Σύστημα . Η ομάδα lipoyl
 μεταφέρει ακυλομάδες στo σύμπλοκο της 2οξοοξύ αφυδρογονάσης και μεθυλαμίνη στην διάσπαση συμπλόκου γλυκίνης
μεταφέρει ακυλομάδες στo σύμπλοκο της 2οξοοξύ αφυδρογονάσης και μεθυλαμίνη στην διάσπαση συμπλόκου γλυκίνης
ε. Συνένζυμο Q (CoQ Ουβικινόνη)
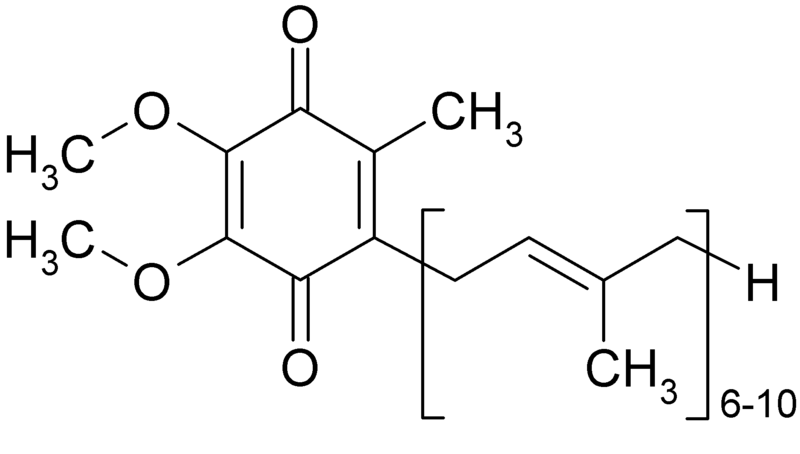 Συστατικό της αλυσίδας της αερόβιας μεταφοράς ηλεκτρονίων και συμμετέχει στην αερόβια κυτταρική αναπνοή η οποία παράγει ενέργεια κυρίως με την μορφή ATP.
Συστατικό της αλυσίδας της αερόβιας μεταφοράς ηλεκτρονίων και συμμετέχει στην αερόβια κυτταρική αναπνοή η οποία παράγει ενέργεια κυρίως με την μορφή ATP.  Υπάρχουν τρεις βαθμίδες οξείδωσης της ουβικινόνης, η πλήρως οξειδωμένη, η πλήρως οξειδωμένη (UBIκινόνης), η ημι κινόνης (ubisemi κινόνες), και πλήρως μειωμένη ( ubiquinol ). Η δράση της βασίζεται στην ικανότητα να μεταφέρει δυο ηλεκτρόνια που μετακινούνται μεταξύ της κετονικής και της αλκοολικής μορφής ή ενός από την μορφή ημικετόλης. που είναι σημαντικό για την αλυσίδα μεταφοράς ηλεκτρονίων στα μιτοχόνδρια.
Υπάρχουν τρεις βαθμίδες οξείδωσης της ουβικινόνης, η πλήρως οξειδωμένη, η πλήρως οξειδωμένη (UBIκινόνης), η ημι κινόνης (ubisemi κινόνες), και πλήρως μειωμένη ( ubiquinol ). Η δράση της βασίζεται στην ικανότητα να μεταφέρει δυο ηλεκτρόνια που μετακινούνται μεταξύ της κετονικής και της αλκοολικής μορφής ή ενός από την μορφή ημικετόλης. που είναι σημαντικό για την αλυσίδα μεταφοράς ηλεκτρονίων στα μιτοχόνδρια.
Συνένζυμα των ενζύμων μεταφοράς ομάδων (τρανφεράσες)
Για να αποφύγει ο οργανισμός την απότομη απελευθέρωση ενέργειας με την διάσπαση ενώσεων που περικλείουν μεγάλα ποσά ενέργειας ακολουθεί τον δρόμο της διάσπασης ( με υδρόλυση κ.α.) ομάδων από τα μόρια (οι ομάδες επίσης περικλείουν ενέργεια σύνδεσης) και την μεταφορά τους σε άλλα μόρια. Έτσι έχουμε ενώσεις, που μεταφέρουν ομάδες με υψηλή ενέργεια σύνδεσης ώστε βοηθούν να προχωρούν άλλες αντιδράσεις που απαιτούν ενέργεια (ΔG>0). Τέτοιες ενώσεις με "υψηλό δυναμικό μεταφοράς ομάδας" ή αλλιώς ενώσεις υψηλής ενέργειας μπορεί να είναι αυτές που μεταφέρουν φωσφορικές ομάδες οι εξης:
α.Ενώσεις που μεταφέρουν φωσφορικές ομάδες
είναι τα
UTP 
CTP
GTP,
ITP κ.λ.π.) και ακόμα 5αδενοσινοτριφωσφορικό οξύ (το γνωστό ATP)
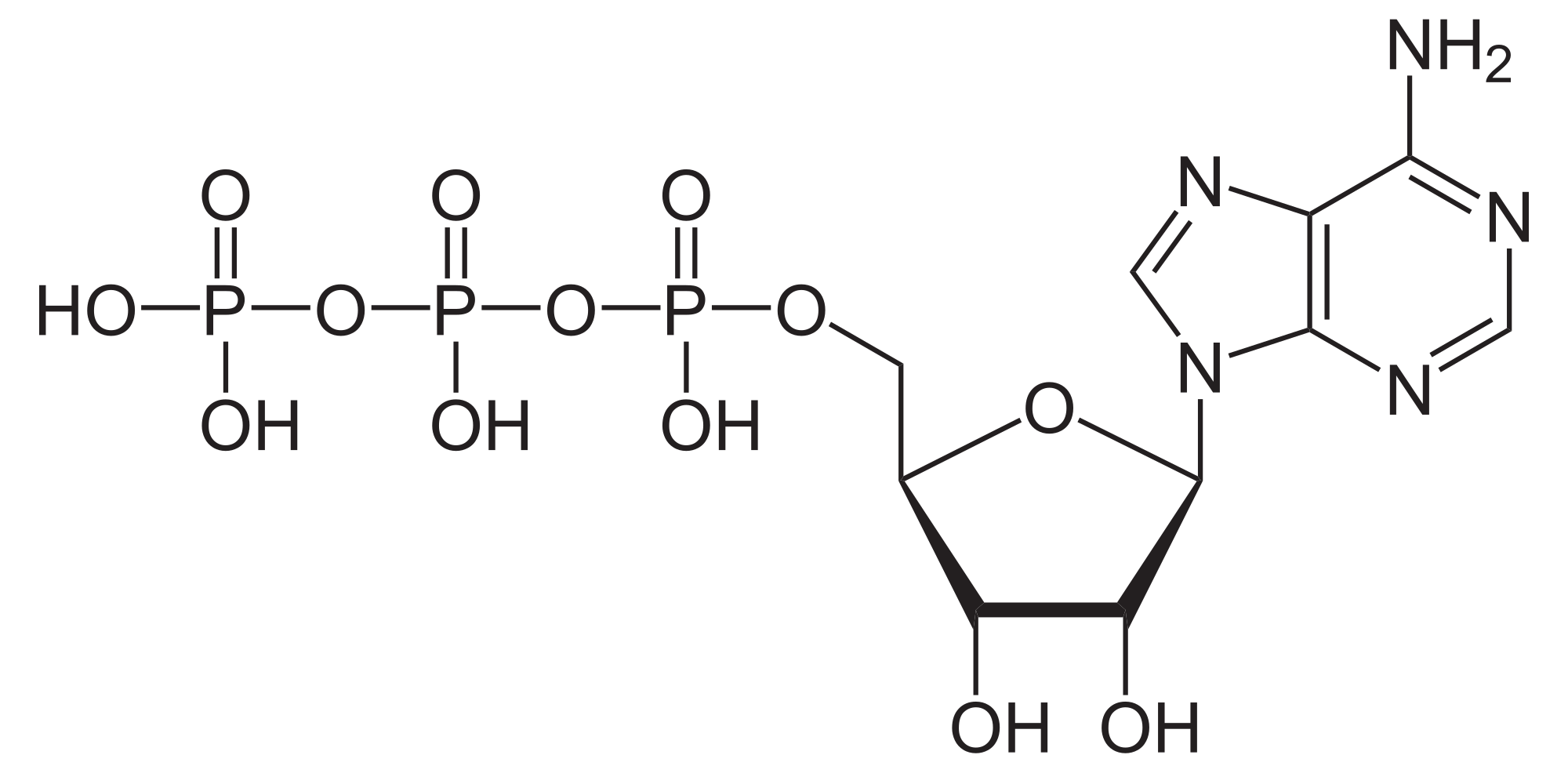
Από αυτές η σταθερότερη ενεργειακά ένωση είναι το ATP 
και λίγο έως πολύ οι υπόλοιπες μεταπίπτουν σε αυτήν.
Το ακετυλο-CοΑ
Συνένζυμο μεταφοράς ομάδας και συγκεκριμένα ομάδας δύο ατόμων άνθρακα είναι και
 Η πλούσια σε ενέργεια σύνδεση της ακετυλομάδας με το συνένζυμο Α μεταφέρεται στον κύκλο του Κρεμπς όπου και ελευθερώνεται το συνένζυμο Α
Η πλούσια σε ενέργεια σύνδεση της ακετυλομάδας με το συνένζυμο Α μεταφέρεται στον κύκλο του Κρεμπς όπου και ελευθερώνεται το συνένζυμο Α 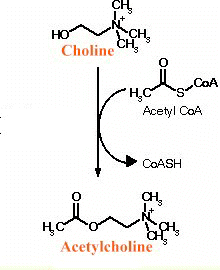
β.Σχετικά με το ATP
Το ATP το συναντάμε σε πολλά σημεία του μεταβολισμού και άλλων βιοχημικών αντιδράσεων, σαν δότη φωσφορικών ομάδων αλλά και σαν αποδέκτη. Με τον απλό αυτό τρόπο μεταφέρεται ενέργεια μέσα στον οργανισμό , ενέργεια που οφείλεται στην σύνδεση της τρίτης φωσφορικής ομάδας (αλλά και των άλλων δύο) στο μοριό του ATP . Η ενέργεια της σύνδεσης δημιουργείται αλλά και "ξοδεύεται" με την αποσύνδεση. Τα ένζυμα μεταφοράς των πλούσιων σε ενέργεια φωσφορικών ομάδων λέγονται κινάσες.
Συγκεκριμένα η ενέργεια του ATP απελευθερώνεται στους χημειότροφους οργανισμούς (που παράγουν ενέργεια από την οξείδωση καυσίμων μορίων (γλυκόζη, λιπαρά κ.α.) με τους εξής τρόπους.
α. με την υδρόλυσή του σε διφωσφορική αδενοσίνη και φωσφορικό
ATP + H2O ↔ ADP + Pi + H+ ; ΔGo = -31 kJ/mol
β. με την υδρόλυσή του σε μονοφωσφορική αδενοσίνη και πυροφοσφορικό
ATP + H2O ↔ AMP + PPi + H+ ; ΔGo = -62 kJ/mol
Την σύνθεση της τριφωσφορικής αδενοσίνης (ATP) από ADP σε διάφορα στάδια του μεταβολισμού συναντάμε σε περιπτώσεις όπως:
- Στην Γλυκόλυση έχουμε την δημιουργία μορίων ATP αλλά και αντίστοιχη κατανάλωση μορίων ATP σε προηγούμενα στάδια
σε δυο στάδια της διαδικασίας μεταφέρει και αποδίδει φωσφορικές ομάδες στην γλυκόζη για να την μετατρέψει σε ενεργοποιημένη 1,6 διφωσφοφρουκτόζη. Στην συνέχεις σαν ADP προσλαμβάνει σε δυο περιπτώσεις φωσφορικές ομάδες και μετατρέπεται σε ATP η μια όταν το 1,3 διφωσφογλυκερινικό οξύ μετατρέπεται σε 3 φωσφογλυκερινικό οξύ, και η δεύτερη όταν το φωσφοενολοπυροσταφυλικό οξύ μετατρέπεται σε πυροσταφυλικό

- Στον κυκλο του Κρεμπς η ενέργεια κατά την δημιουργία τριφωσφορικής γουανοσίνης μεταφέρεται στην συνέχεια στο ATP
Γίνεται μέσα στην μήτρα των μιτοχονδρίων. Το μόριο που εισέρχεται αρχικά στην μήτρα είναι το ακέτυλοσυνένζυμοΑ . Κατά τον κύκλο αυτό και κατά το στάδιο της μετατροπής του ηλεκτροσυνένζυμου Α σε ηλεκτρικό οξύ ένα ελεύθερο μόριο φωσφορικού οξέος εκτοπίζει το CoA και προσκολλάται πρόσκαιρα μετατρέποντάς το σε σουκκινικό. Κατόπιν μεταφέρεται στο συνένζυμο GDP που μετατρέπεται σε GTP. Όμως το GTP εάν πρόκειται να χρησιμοποιηθεί σε χημικές αντιδράσεις σαν δότης ενέργειας, υδρολύεται πρώτα και μετατρέπεται σε ATP
Ενώ στα βακτήρια και τα φυτά χρησιμοποιείται εξ αρχής ADT που καταλήγει στο ATP 
Κατ' αυτόν τον κύκλο, παράγονται ανηγμένα συνένζυμα NADH και FΑDΗ2, που περικλείουν ενέργεια, αποθηκευμένη σε ηλεκτρόνια υψηλής ενέργειας και ακόμα μεταφέρουν ηλεκτρόνια.
- στην οξειδωτική φωσφορυλίωση η ενέργεια των ανηγμένων συνενζύμων NADH και FΑDΗ2 μεταφέρεται στο ATP
Αυτές οι αντιδράσεις απελευθερώνουν σημμαντικά ποσά ενέργειας η οποία πρέπει κάπου να φυλαχθεί . Αυτόν τον ρόλο αναλαμβάνει το μόριο της ATP Με την συμμετοχή του οξυγόνου στην κυτταρική αναπνοή και στην φάση της οξειδωτικής φωσφορυλίωσης δημιουργούνται 10 μόρια ATP από αντίστοιχα μόρια ADP. Στην μεταφορά των ηλεκτρονίων από τα ανηγμένα συνένζυμα NADH και FΑDΗ2 συμμετέχουν 4 ένζυμα ( Αναγωγάση NADH-ουβικινόνης (σύμπλοκο I)
Αναγωγάση ηλεκτρικού-ουβικινόνης (σύμπλοκο II), Κυτοχρωμική αναγωγάση (σύμπλοκο III), Κυτοχρωμική οξειδάση (σύμπλοκο IV) )
Για τις τρείς άλλες ομάδες των ενζύμων τις υδρολάσες τις λιγάσες και τις λυάσες οι συμπαράγοντες είναι μεταλλικά ιόντα
(Υδρολάσες. Διάσπαση δεσμών με συμμετοχή νερού. 4. Λυάσες. Απόσπαση ομάδων χωρίς υδρόλυση. Λιγάσες ή συνθετάσες Συνένωση δύο μορίων και σχηματισμός νέου).
Συνένζυμα των ενζύμων λιγάσων
Η δισμουτάση του σουπεροξειδίου (SOD), που καταλύει την αντίδραση:
-
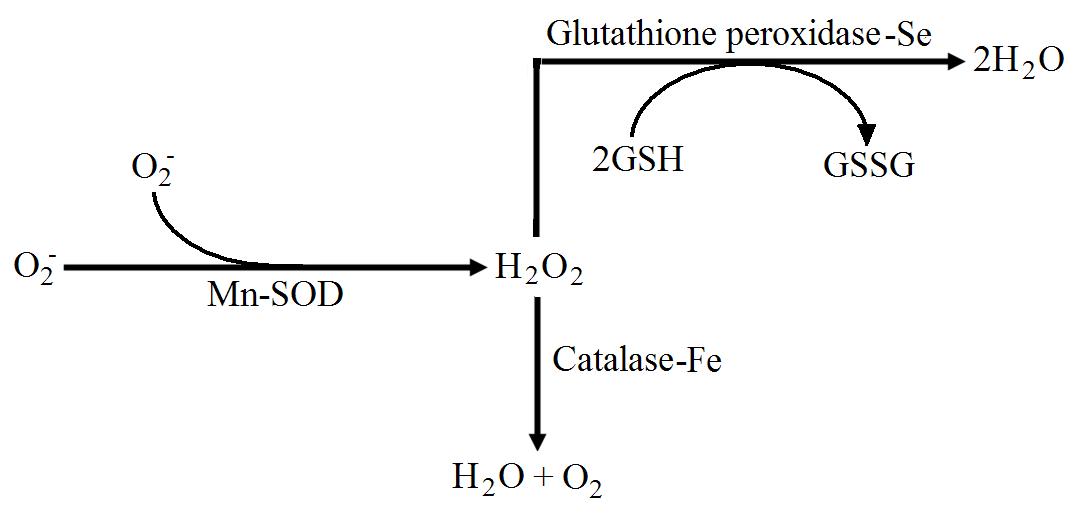

- ∙Ο2- + 2Η+ → Η2Ο2 και είναι απαραίτητο γιατί ,
- απομακρύνει από τον οργανισμό τα ανιόν σουπεροξειδίου (∙O2-) και τα κατιόντα Η+ που προκαλούν οξειδώσεις στα κύτταρα, το απαραίτητο συνένζυμο είναι το Μαγγάνιο
- Ανάλογα για την Υπεροξειδάση της γλουταθειώνης που παίζει ανάλογο ρόλο ο απαραίτητος συμπαράγοντας είναι το σελήνιο:
-
- 2GSH + Η2Ο2 → GSSG + 2Η2Ο το απα
Συνένζυμα των ενζύμων λυάσων
Λυάση μπορεί να θεωρηθεί η ηλεκτρική αυδρογονάση που καταλύει την μετατροπή του ηλεκτρικού οξέος  σε φουμαρικό
σε φουμαρικό  στον κύκλο του Κρεμπς, Είναι ένα πολύπλοκο ένζυμο με συμπαράγοντες φλαβοπρωτείνες και αίμη
στον κύκλο του Κρεμπς, Είναι ένα πολύπλοκο ένζυμο με συμπαράγοντες φλαβοπρωτείνες και αίμη
Η μετατροπή γίνεται σε δυο στάδια
Τελικά όπως καταλαβαίνουμε, τα περισσότερα ένζυμα για να δράσουν, χρειάζονται την συμμετοχή συμπαραγόντων . Άλλη μια ασφαλιστική δικλείδα από τις τόσες και τόσες που παρατηρούμε στα υπερεξελιγμάνα συστήματα των οργανισμών καικυρίως των πιο εξελιγμέγμένων από αυτούς, ώστε να μπορούν να λειτουργούν σε πολύ λεπτές ισορροπίες και στα στενά όρια που ο κάθε ένας από αυτούς έχει τοποθετηθεί να ζει.
Δήμητρα Σπανού
πηγές
BIOXHMEIA Γ Τάξη Γενικού Λυκείου
ΣΗΜΕΙΩΣΕΙΣ ΒΙΟΛΟΓΙΚΗΣ ΧΗΜΕΙΑΣ κατά τας παραδόσεις υφηγητού Α. Γρανίτσα αθήνα 1966
https://www.chem.uoa.gr/courses/Undergraduate/Biochem/Demopoulos/Biochemistry_IΙ/bioch_synenzyma.pdf
https://en.wikipedia.org/wiki/Lipoic_acid
https://en.wikipedia.org/wiki/Ubiquinol
https://biolexikon.blogspot.gr/2010/10/cytochrome.html
https://en.wikipedia.org/wiki/Oxygen–hemoglobin_dissociation_curve
https://ebooks.edu.gr/modules/ebook/show.php/DSGL-C120/480/3166,12755/
Στοιχεία Γενικής και Συγκριτικής Βιολογικής Χημείας Αν. Χρηστομάνου 1961
https://el.wikipedia.org/wiki/Οξειδωτικό_στρες
