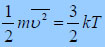Ακατέργαστο
ʃ Fx(x)dx= ʃ m dux/dt dx
W= ʃ m dux/dt dx =m[1/2 ux²] = 1/2 ub² -1/2 ua²
οι ιδιότητές τους και η τάξη μεγέθους τους
Αποδεικνύεται ότι όλες οι βασικές δυνάμεις της φύσης φαίνεται να είναι συντηρητικές. Μην νομίζετε ότι αυτό είναι συνέπεια των νόμων του Νεύτωνα. Στην πραγματικότητα, όσο το φανταζόταν ο ίδιος ο Νεύτωνας, οι δυνάμεις μπορεί να είναι μη συντηρητικές, όπως η τριβή, η οποία φαίνεται μη συντηρητική. Χρησιμοποιώντας τη λέξη «φαινομενικά», παίρνουμε τη σύγχρονη άποψη ότι όλες οι βαθιές δυνάμεις, όλες οι δυνάμεις αλληλεπίδρασης μεταξύ σωματιδίων στο πιο θεμελιώδες επίπεδο, είναι συντηρητικές δυνάμεις.
για ένα μόνο αντικείμενο. Αν εφαρμόζονταν κάποιες δυνάμεις σε αυτό, τότε κάποιες από αυτές θα μπορούσαν να το μετακινήσουν στο σύνολό του και θα βλέπαμε πώς κινείται το κέντρο αυτού του σώματος. Από την άλλη πλευρά, άλλες δυνάμεις θα μπορούσαν, ας πούμε, να «δαπανηθούν» για να αυξήσουν τη δυναμική ή την κινητική ενέργεια των «σωματιδίων» μέσα στο «σώμα». Ας υποθέσουμε, για παράδειγμα, ότι η δράση αυτών των δυνάμεων θα οδηγούσε σε διαστολή ολόκληρου του σμήνους και αύξηση των ταχυτήτων των «σωματιδίων». Η συνολική ενέργεια του «σώματος» θα διατηρούνταν πραγματικά. Αλλά κοιτάζοντας από μακριά με τα αδύναμα μάτια μας, που δεν διακρίνουν τις άτακτες εσωτερικές κινήσεις, θα βλέπαμε μόνο την κινητική ενέργεια ολόκληρου του σώματος, και θα μας φαινόταν ότι η ενέργεια δεν διατηρείται, αν και το όλο θέμα θα ήταν ότι δεν διακρίνουμε τις λεπτομέρειες. Αποδεικνύεται ότι αυτό συμβαίνει πάντα: η συνολική ενέργεια του σύμπαντος, η κινητική ενέργεια συν τη δυναμική ενέργεια, αν το δεις σωστά, είναι πάντα σταθερή.
Έτσι, το συνολικό δυναμικό συν τις κινητικές ενέργειες σε ολόκληρο τον κόσμο είναι σταθερές, και αν ο «κόσμος» είναι ένα απομονωμένο κομμάτι ύλης, τότε η ενέργειά του είναι σταθερή, εκτός αν υπάρχουν εξωτερικές δυνάμεις. Αλλά, όπως είδαμε, μέρος της κινητικής και δυναμικής ενέργειας ενός αντικειμένου μπορεί να είναι εσωτερική (π.χ. εσωτερικές μοριακές κινήσεις), εσωτερική με την έννοια ότι δεν το παρατηρούμε.
Δεδομένου ότι η δυναμική ενέργεια, το ολοκλήρωμα της (Δύναμης)•(ds),
Για ένα συντηρητικό πεδίο
αν τα αρχικά και τελικά σημεία είναι τα ίδια, το έργο είναι μηδέν
Οι υπολογισμοί μπορεί να γίνουν ευκολότερα εάν αντί για ένα διάνυσμα συντηρητικόυ πεδίου δώσουμε την ενός κλίση βαθμωτού δυναμικού οπότε
Το έργο που γίνεται είναι απλά η διαφορά στην αξία αυτού του δυναμικού στα αρχικά και τελικά σημεία της διαδρομής. Αυτά τα σημεία δίνονται με χ = a και χ = b, αντίστοιχα:
Αλλά επίσης, η δυναμική ενέργεια ενός σώματος μπορεί να γραφεί και με άλλους τρόπους ανάλογα με την δύναμη:
όπως εάν πρόκειται για δύναμη ελατηρίου ʃ Fx(x)dx= W= ʃ (-kx) dx και
W= -k[1/2 x²] = 1/2 k(a² -b²)
σαν γινόμενο της μάζας επί μιαν άλλη συνάρτηση ʃ Fx(x)dx= ʃ m dux/dt dx και
W= ʃ m dux/dt dx =m[1/2 ux²] = 1/2 ub² -1/2 ua²
η δυναμική ενέργεια U(x, y, z) ενός σώματος που βρίσκεται στο (x, y, z) μπορεί να γραφτεί ως το γινόμενο του m από μια άλλη συνάρτηση. Ας το ονομάσουμε δυνητικό y.. Το αναπόσπαστο ∫C•ds είναι
-y, παρόμοιο με το ∫F•ds=-U; Διαφέρουν μόνο
Κλίμακα:
U= -∫F•ds=-m∫C•ds=my. (14.7)
Γνωρίζοντας αυτή τη συνάρτηση y (x, y, z) σε κάθε σημείο του χώρου, είναι δυνατό να υπολογιστεί αμέσως η δυναμική ενέργεια του σώματος σε οποιοδήποτε σημείο, δηλαδή U(x, y, z) — m y (x, y, z). Τώρα, όπως μπορείτε να δείτε, έχει γίνει ένα ασήμαντο θέμα.
Αλλά στην πραγματικότητα, αυτό δεν είναι σε καμία περίπτωση ασήμαντο, γιατί μερικές φορές είναι πολύ πιο ευχάριστο να περιγράφεις ένα πεδίο προσδιορίζοντας την κατανομή του δυναμικού σε ολόκληρο τον χώρο παρά να δίνεις C. Αντί για τα τρία μιγαδικά συστατικά μιας διανυσματικής συνάρτησης, είναι ευκολότερο να οριστεί η βαθμωτή συνάρτηση y. Επιπλέον, όταν το πεδίο δημιουργείται από πολλές μάζες, η τιμή y είναι ευκολότερο να υπολογιστεί από τις τρεις συνιστώσες του C: δυναμικά-βαθμωτά, και μπορούν απλά να προστεθούν μαζί χωρίς να ανησυχείτε για τις κατευθύνσεις των δυνάμεων. Και το πεδίο Γ, όπως θα δούμε σε λίγο, είναι εύκολο να ανακατασκευαστεί γνωρίζοντας το y. Ας υποθέσουμε ότι έχουμε σημειακές μάζες m1, m2,... στα σημεία 1, 2..., και θέλουμε να μάθουμε το δυναμικό y σε κάποιο αυθαίρετο σημείο P. Τότε αποδεικνύεται ότι είναι ένα απλό άθροισμα των δυναμικών των επιμέρους μαζών στο σημείο P:
Κλίμακα:
U= -∫F•ds=-m∫C•ds=my. (14.7)
Οι ανελαστικές συγκρούσεις είναι εκείνες στις οποίες η συνολική μεταφορική ενέργεια του συστήματος αλλάζει. Οποιοδήποτε κέρδος ή απώλεια μεταφορικής ενέργειας πρέπει, φυσικά, να αντισταθμίζεται από άλλες αλλαγές στα συγκρουόμενα συστήματα.
Δεδομένου ότι μια χημική αντίδραση συμβαίνει μόνο μέσω της σύγκρουσης των αντιδρώντων σωματιδίων, η δομή τους και η φύση των χημικών δεσμών, καθώς και οι ιδιότητες των ουσιών που προκύπτουν, παίζουν καθοριστικό ρόλο. Επομένως, η αντιδραστικότητα, και κατά συνέπεια ο ρυθμός μιας χημικής αντίδρασης, ακόμη και μεταξύ παρόμοιων ενώσεων, ποικίλλει σημαντικά.
Θα εξετάσουμε φαινόμενα στα οποία τα μόρια δεν αλλάζουν τη δομή τους και η θερμοκρασία δεν είναι ακόμη τόσο υψηλή ώστε να είναι απαραίτητο να λάβουμε υπόψη τη δονητική ενέργεια των ατόμων μέσα σε ένα μόριο. Σε τέτοια φαινόμενα, η αλλαγή στην εσωτερική ενέργεια ενός σώματος συμβαίνει μόνο λόγω αλλαγών στην κινητική ενέργεια των μορίων και στη δυναμική ενέργεια των αλληλεπιδράσεών τους μεταξύ τους. Για το συνολικό ενεργειακό ισοζύγιο, δεν έχει σημασία η ίδια η εσωτερική ενέργεια, αλλά η αλλαγή της. Επομένως, η εσωτερική ενέργεια ενός μακροσκοπικού σώματος μπορεί να γίνει κατανοητή μόνο ως το άθροισμα της κινητικής ενέργειας της θερμικής κίνησης όλων των μορίων και της δυναμικής ενέργειας των αλληλεπιδράσεών τους.
Η εσωτερική ενέργεια είναι συνάρτηση της κατάστασης του σώματος και καθορίζεται από μακροσκοπικές παραμέτρους που χαρακτηρίζουν την κατάσταση θερμοδυναμικής ισορροπίας του σώματος.
Και όταν το δυναμικό είναι σταθερό, δεν υπάρχει πεδίο: αν η δυναμική ενέργεια δεν αλλάξει, τότε δεν υπάρχει δύναμη, γιατί όταν μετακινούμε ένα σώμα από το ένα εσωτερικό σημείο στο άλλο, το έργο που γίνεται από τη δύναμη είναι ακριβώς μηδέν. Γιατί; Επειδή το έργο της μετακίνησης ενός σώματος από το ένα σημείο στο άλλο είναι ίσο με μείον τη μεταβολή της δυναμικής ενέργειας (ή το αντίστοιχο ολοκλήρωμα του πεδίου είναι ίσο με τη μεταβολή του δυναμικού). Αλλά η δυναμική ενέργεια και στα δύο σημεία είναι η ίδια, πράγμα που σημαίνει ότι η μεταβολή της είναι ίση με μηδέν, και επομένως δεν γίνεται καμία εργασία με καμία κίνηση μέσα στο σφαιρικό στρώμα. Και αυτό είναι δυνατό μόνο όταν δεν υπάρχουν δυνάμεις μέσα στο στρώμα.
Η θεωρία των ενεργών συγκρούσεων (TAC) βασίζεται στη μοριακή θεωρία των αερίων, η οποία υποστηρίζει ότι η αέρια φάση έχει μια συγκεκριμένη κατανομή σωματιδίων με βάση την ταχύτητα (κατανομή Maxwell) και την ενέργεια (κατανομή Boltzmann). Σύμφωνα με τις έννοιες της TAC, τα σωματίδια πρέπει να συγκρουστούν για να συμβεί αλληλεπίδραση.
Σύμφωνα με τη μοριακή κινητική θεωρία των αερίων, ο συνολικός αριθμός συγκρούσεων των μορίων A και B ( Z AB ) ανά μονάδα όγκου ανά μονάδα χρόνου καθορίζεται από την αναλογία:
![]() (1
(1
ΑΠΟ ΤΗΝ ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ (MAXWELL- BOLTZMAN)
ΣΤΑ ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΚΑΙ ΤΗΝ ΘΕΩΡΙΑ ΤΩΝ ΕΝΕΡΓΩΝ ΣΥΓΚΡΟΥΣΕΩΝ
Στις στατιστικές κατανομές των Maxwell (για τις ταχύτητες των μικροσωματιδίων) και Boltzman (για τις ενέργειες των σωματιδίων) που ισχύουν σε υψηλές θερμοκρασίες (και περιβάλλοντος) και χαμηλές συγκεντρώσεις σωματιδίων μελετήθηκαν τα αέρια μη αλληλεπιδρώντων σωματιδίων (ιδανικά)
Σύμφωνα με την κινητική θεωρία ιδανικού αερίου, τα σωματίδια (άτομα ή μόρια) που το αποτελούν την αέρια μάζα, κινούνται ελεύθερα μέσα σε στο ακίνητο δοχείο που περιέχεται το αέριο και δεν αλληλεπιδρούν μεταζύ τους εκτός από πρακτικά στιγμιαίες ελαστικές συγκρούσεις και δεν υπάρχει απώλεια κινητικής ενέργειας
Ο συντελεστής τριβής μεταξύ τους είναι μηδέν και δεν υπάρχουν ελκτικές δυνάμεις μεταξύ τους
Θεωρητικά, τα μόρια του ιδανικού αερίου θεωρούνται μικρές σφαίρες με όγκο αμεληταίο
Να σημειώσουμε ότι όλα τα πραγματικά αέρια παρουσιάζουν ιδανική συμπεριφορά σε χαμηλές πιέσεις και υψηλές θερμοκρασίες γιατί στις συθήκες αυτές οι δυνάμεις αλληλεπίδρασης θεωρούνται εξαιρετικά μικρές.

Όμως τις πιο πολλές φορές η συμπεριφορά των αερίων δεν είναι ιδανική. Έχουμε τότε τα πραγματικά αέρια. Η κίνησή τους εξακολουθεί όπως και στα ιδανικά αέρια, αλλά υπάρχει επιπλέον δυναμική ενέργεια λόγω αλληλεπιδράσεως μεταξύ αυτών. Συμβαίνουν επίσης και συγκρούσεις μεταξύ τους αλλά οι συγκρούσεις αυτές δεν είναι πάντα ελαστικές. δηλαδή υπάρχει απώλεια ενέργειας που μετατρέπεται σε άλλη μορφή
στην ιστοσελίδα
Στη θεωρία των ενεργών συγκρούσεων (S. Arrhenius) πιστεύεται ότι υπό ορισμένες προυποθέσεις οι συγκρούσεις των μορίων ενός αερίου μπορεί να προκαλέσουν αλληλεπίδραση μεταξύ των σωματιδίων, να δηλαδή υπάρξει αλλοίωση της αρχικής μορφής τους και να γίνει μετατροπή των αρχικών σωμάτων σε κάποια άλλα, ακριβώς την στιγμή της σύγκρουσης των σωματιδίων- μορίων μεταξύ τους
Να θυμηθούμε ότι για τα μη αλληλεπιδρώντα σωματίδια στα ιδανικά αέρια, υπήρξε αρχικά η παραδοχή πως τα σωματίδια θεωρούνται σαν ελαστικές σφαίρες χωρίς συγκεκριμένη δομή και διαστάσεις (δηλαδή χωρίς όγκο).
Όμως στην πραγματικότητα τα μόρια που συγκρούονται έχουν και συγκεκριμένες δομές και διαστάσειςς με την σύγκρουση αναδιατάσονται για να δώσουν κάποια άλλα σωματίδια- μόρια με διαφορετικές δομές.
Η προυπόθεση για να συμβει αυτό είναι η επάρκεια ενέργειας που θα κάνει τις συγκρούσεις ενεργές, δηλαδή θα δώσει χημικές αντιδράσεις
Οι αλλαγές που προκύπτουν από αυτό
Είναι μόνο η δημιουργία νέων σωματίδιων διαφορετικών από τα αρχικά σε δομή και ιδιότητες αλλά και σε αριθμό σωματιδίων
- Η αλλαγή του αριθμού των σωματιδίων (έχοντας υπ όψη την σχέση των μικροσκοπικών ιδιοτήτων με τις μακροσκοπικές)
μπορεί να επιφέρει αλλαγές στον συνολικό όγκο του συστήματος -αερίου, την Πίεση ή την Θερμοκρασία
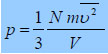
Ταυτόχρονα οι ενεργές συγκρούσεις επιφέρουν και άλλη μεταβολή στο σύστημα που ισχύει για τα πραγματικά (αλλά όχι για τα ιδανικά αέρια)
- Οι συγκρούσεις εδώ δεν είναι ελαστικές και μπορεί να υπάρχει μεταβολή στην ενέργεια, μετατροπή σε άλλη μοργή ενέργειας όπως θερμική ή και απώλεια ενέργειας
Ας δούμε τι σημαίνουν αυτά:
Εφόσον η ενέργεια του συνόλου των σωματιδίων αποτελεί , όπως θα δούμε, την εσωτερική ενέργεια του συστήματος
Σύμφωνα με την εξίσωση της κινητικής θεωρίας των Maxwell- Boltzman
σημειώνεται πως ( f(x) = exp(x) = ex.)
ο αριθμός των σωματιδίων που βρίσκονται σε κάθε μια ενεργειακή κατάσταση σχετίζεται με την Ενέργεια και την θερμοκρασία
Αλλά και από την σύνδεση των μικροκαταστάσεων (κινητική θεωρία) με τις μακροκαταστάσεις ο συνολικός αριθμός των σωματιδίων σχετίζεται με την πίεση τον όγκο του συστήματος και την μέση ταχύτητα των σωματιδίων
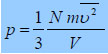 |
|
Από τις δυο αυτές σχέσεις βγαίνει: p= N /V. kT ή pV= NkT
Τώρα θα πρεπει να δούμε την εσωτερική ενέργεια του συστήματος θερμοδυναμικά ώστε να κατανοήσουμε τις αλλαγές που επιφέρουν οι ενεργές συγκρούσεις των σωματιδίων
Η ΕΣΩΤΕΡΙΚΗ ΕΝΕΡΓΕΙΑ ΣΥΣΤΗΜΑΤΟΣ ΣΩΜΑΤΙΔΙΩΝ ΚΑΙ
ΤΟ ΧΗΜΙΚΟ ΔΥΝΑΜΙΚΟ ΣΥΣΤΗΜΑΤΩΝ ΜΕ ΜΕΤΑΒΛΗΤΟ ΑΡΙΘΜΟ ΣΩΜΑΤΙΔΙΩΝ
Σε ένα σύστημα, η συνολική ενέργεια όλων των μικροσκοπικών του στοιχείων του συστήματος (κινητική, δυναμική λόγω αλληλεπιδράσεων κ.λ.π.), αποτελεί την Eσωτερική Eνέργεια του συστήματος .
Συμβολίζεται με U και μετράται σε μονάδες ενέργειας (joule ή calories) Ισχύουν τα:
- H εσωτερική ενέργεια αποτελεί εσωτερική κατάσταση ενός συστήματος και εξαρτάται μόνο από τις παραμέτρους του συστήματος T, V, P και όχι από τον τρόπο που έχει διαμορφωθεί.
- Ακόμη, η εσωτερική ενέργεια ενός συστήματος είναι ίση με το άθποισμα των εσωτερικών ενεργειών των μερών του συστήματος
- Δεν μπορεί να μετρηθεί άμεσα και μετράμε μόνο τις μεταβολές της ΔU
Οι αλλαγές στις τιμές της εσωτερικής ενέργειας ΔU καθορίζονται από την διαφορά μεταξύ της ενέργειας που μπορεί να ελευθερωθεί στην διάρκεια πιθανών εσωτερικών διεργασιών ΤΔS και το συνολικού έργου στη αλληλεπίδραση με το εξωτερικό περιβάλλον PΔV . Αν έχουμε χημικές αντιδράσεις και μεταβολή του αριθμού σωματιδίων dNi προστίθεται ο όρος ΣμιdNi ,
Να θυμηθούμε ότι S είναι η εντροπία που είναι ένα φυσικό μέγεθος που χρησιμοποιείται μαζί με την θερμοκρασία Τ για να περιγράψει ένα θερμοδυναμικό σύστημα και αυξάνεται όταν αυξάνεται η αταξία στο σύστημα.
Στον όρο ΣμιdNi , το μ λέγεται χημική ισχύς ή χημικό δυναμικό. Είναι μια θερμοδυναμική συνάρτηση που χρησιμοποιείται για να περιγράψει κατάσταση συστημάτων με μεταβλητό αριθμό σωματιδίων. Είναι ίσο με την μεταβολή της ενέργειας που υπάρχει όταν μεταβάλεται κατά ένα ο αριθμός των σωματιδίων στο σύστημα, χωρίς το σύστημα να ανταλλάσσει θερμότητα με το περιβάλλον (αδιαβατικά)
ΜΗ ΙΔΑΝΙΚΑ ΑΕΡΙΑ
Τα σωματιδία που την αποτελούν τα υλικά σώματα βρίσκονται σε μια διαρκή δράση που περιλαμβάνει, ανάλογα και με την φυσική τους κατάσταση, τυχαίες ή καθορισμένες κινήσεις,
Ενώ τα αέρια συστήματα μη αλληλεπιδρώντων σωματιδίων, που κινούνται διαγράφοντας μικρότερες ή μεγαλύτερες ευθίγραμμες τροχαιές και ακόμα υπάρχουν συγκρούσεις μεταξύ τους (αλλά ελαστικές που δεν αλλοιώνουν την φύση των σωματιδίων και δεν μετατρέπουν την κινητική ενέργεια σε άλλες μορφές) , οι ταχύτητες και οι ενέργειές τους περιγράφονται από κατανομές πιθανοτήτων των Maxweel Boltzman
Όμως, τα περισσότερα σώματα- συστήματα σωματίδιων συμπεριλαμβάνουν και άλλους τύπους σωματιδίων ( διατομικά και πολυατομικά μόρια, ιόντα και πολυατομικά ιόντα και άλλα συσσωματώματα) οι κινήσεις τους είναι πιο πολύπλοκες και περιλαμβάνουν και άλλες ενέργειες όπως ενέργεια από ταλαντώσεις και περιστροφές μικρότερων ή μεγαλύτερων τροχαιών, ακόμα και από ηλεκτρικές κ.λ.π. δυνάμεις.
Η ΘΕΩΡΙΑ ΤΩΝ ΕΝΕΡΓΩΝ ΣΥΓΚΡΟΥΣΕΩΝ ΤΩΝ ΣΩΜΑΤΙΔΙΩΝ
Ακόμα, οι συγκρούσεις μεταξύ των σωματιδίων (μόρια, ελεύθερες ρίζες κ.λ.π.), δεν είναι πάντα ανελαστικές, αλλά πολλές από αυτές έχουν μοιραία αποτελέσματα που μπορεί να είναι και η απώλεια κινητικής ενέργειας αλλά και αλλοιώσεις των μορίων ή μετατροπής τους σε κάποια άλλα
Έτσι αυτές οι κινήσεις των μορίων, έχουν σαν αποτέλεσμα να υπάρχει ένας αριθμός από αυτά που συγκρούονται μεταξύ τους ( ΖΑΒ) που να επιφέρουν αλλαγές στην φύση των σωματιδίων και την ενέργειά τους ΖΑΒ ενεργές.
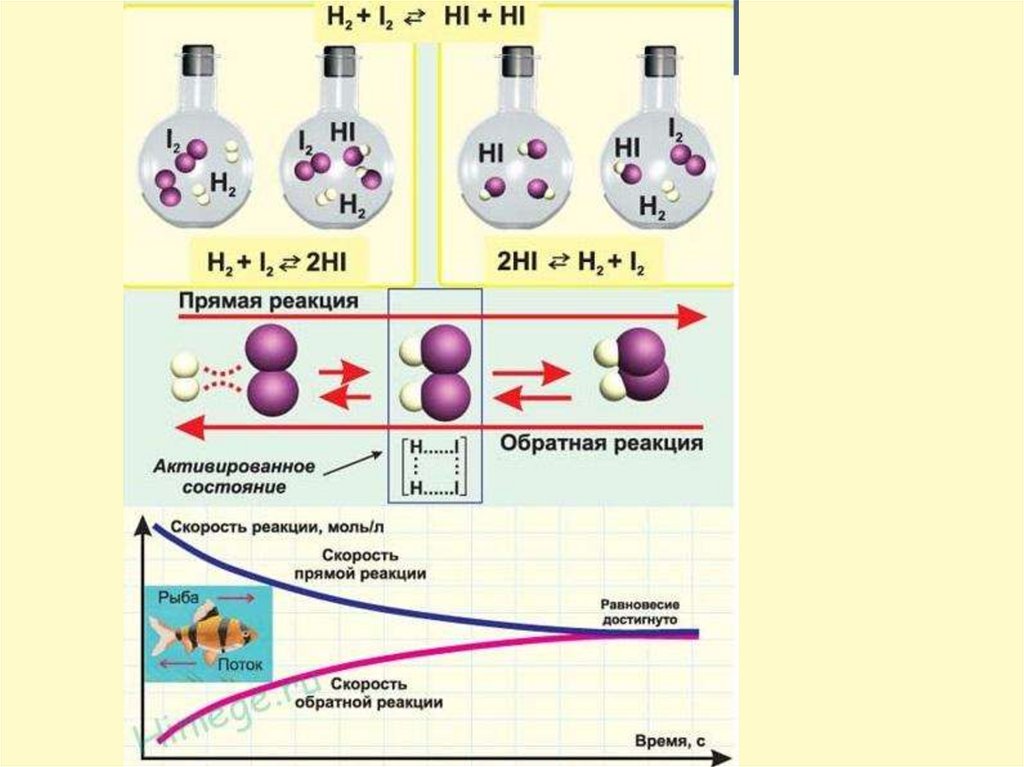
Αυτό υποστηρίζει η Θεωρία της Ενεργής Σύγκρουσης που βασίζεται στη Μοριακή Θεωρία των αερίων και σύμφωνα με αυτή τα σωματίδια πρέπει να συγκρούονται
Σύμφωνα με την Κινητική Θεωρία ο συνολικός αριθμός των συγκρούσεων για μόρια Α και Β ανά μονάδα όγκου καθορίζεται από τις ιδιότητες και την γεωμετρία των σωματιδίων και τον αριθμό τους ανά μονάδα όγκου
Ένας αριθμός από τις συγκρούσεις αυτές οδηγούν σε χημικές αντιδράσεις.
Όταν υπάρχει αλληλεπίδραση μεταξύ των μορίων τότε οι συγκρούσεις ορίζονται σαν ενεργές συγκρούσεις
Για να είναι οι συγκρούσεις ενεργές πρέπει:
α. τα σωματίδια να περάσουν ένα φράγμα ενέργειας το ύψος του οποίου είναι η τιμή της ενέργειας ενεργοποίησης
Πρέπει τα σωματίδια έχουν μια ελαχίστη περίσσεια ενέργειας τουλάχιστον ίση με την ενέργεια ενεργοποίησης, ώστε να περάσουν το φράγμα ενέργειας. Αυτή η ενέργεια όμως μπορεί να προκληθεί και από εξωτερικές αιτίες: απορρόφηση κβάντων φωτός στην διάρκεια φωτοχημικών αντιδράσεων, η δράση ηλεκτρικών εκκενώσεων, ο βοβαρδισμός με ηλεκτρόνια, σωματια α, νετρονίων κ.α.
β. τα μόρια που συγκρούονται εκτός από την ενέργεια ενεργοποίησης πρέπει να έχουν και τον κατάλληλο προσανατολισμό
Αυτό εξαρτάται από την επιφάνεια του μορίου που "βλέπει " το άλλο μόριο με το οποίο συγκρούεται. Το υπολογίζουμε ορίζοντας την ενεργό διάμετρο των μορίων
Εάν υπάρχουν μόρια Α και Β δεν υπάρχει ελξη ή άπωση μεταξύ τους και αυτά κινούνται ευθύγραμμα το ένα προς το άλλο μέσα σε έναν κύλινδρο ακτίνας r
ισχύει: (σ1 + σ2)/2 =σ12=r
αν υπάρχει έλξη (σ1 + σ2)/2 =σ12>r
αν υπάρχει άπωση (σ1 + σ2)/2 =σ12<r
Η ποσότητα πσ2 λέγεται αποτελεσματική διατομή των μορίων και έχει μεγάλη σημασία στην κινητική των χημικών αντιδράσεων
Ο αριθμός των συγκρουσεων και οι ενεργές συγκρούσεις
Εάν οι συνολικές συγκρούσεις ανά μονάδα όγκου είναι ΖΑΒ και οι ενεργές συγκρούσεις ΖΑΒ ενεργές ισχύει
ΖΑΒ >ΖΑΒ ενεργές και
ΖΑΒ ενεργές= ![]() και
και ![]() είναι από την θεωρία του Boltzman
είναι από την θεωρία του Boltzman
¨Έτσι όμως και λαμβάνοντας υπ όψη την αποτελεσματικότητα την αποτελεσματικότητα των συγκρούσεων, οι ενεργές συγκρούσεις είναι λιγότερες από την τιμή που προκύπτει από την θεωρία του Boltzman (π'ανω) για τον λόγο
η εξίσωση των ενεργών συγκρούσεων παίρνει μπροστά έναν παράγονται και καταλήγει σ αυτήν την μορφή
ZABενεργεί. = ![]()
Υπάρχουν θεωρίες που περιγράφουν τον μηχανισμό μιας χημικής αντίδρασης όπως η θεωρία του ενεργοποιημένου συμπλέγματος, η θεωρία ενεργής σύγκρουσης, η θεωρία των μονομοριακών αντιδράσεων, η θεωρία των αντιδράσεων μεταφοράς κ.α.. Όλες όμως σε γενικές γραμμές δέχονται την ιδέα του ενεργειακού φράγματος και της ενέργειας ενεργοποίησης.
Εάν κατά την πραγματοποίηση των ενεργών συγκρούσεων υπάρξουν διεργασίες που η ενέργεια που απαιτούν
Η εξίσωση που προκύπτει είναι η βασική εξίσωση TAC για τη σταθερά ρυθμός διμοριακής αντίδρασης. Προφανώς ότι είναι παρόμοια με την εξίσωση Arrhenius
![]()
όπως για παράδειγμα
Η ενέργεια των χημικών αντιδράσεων
Κατά τις χημικές αντιδράσεις, κατά τις μετατροπές δηλαδή χημικών ουσιών σε άλλες, μεταβάλλεται η χημική ενέργεια του συστήματος. Αποτέλεσμα είναι να ελευθερώνεται (στο περιβάλλον) ή να απορροφάται (από το περιβάλλον), ενέργεια ίση με τη διαφορά των χημικών ενεργειών των αρχικών και τελικών ουσιών.
καρυστος καστρο πόρτες (1).jpg)
Δήμητρα Σπανού
ΠΗΓΕΣ
Επίδραση της συγκέντρωσης των αντιδραστικών ουσιών. Ο νόμος των ενεργών μαζών
Η Εσωτερική Ενέργεια και οι Ιδιότητές της | Χημική θερμοδυναμική. Σχολικό βιβλίο
§3. Εσωτερική ενέργεια — ZFTS, MIPT
11.1 Θεωρία ενεργής σύγκρουσης
активные столкновения частиц газа
11.1 Θεωρία ενεργής σύγκρουσης
Θεωρία Ενεργής Σύγκρουσης - UTTP
Επίδραση της συγκέντρωσης των αντιδραστικών ουσιών. Ο νόμος των ενεργών μαζών
ακατεργαστο
αναφέρεται
Για μη ιδανικά αέρια ή υγρά, απαιτείται μια χωρική συνάρτηση κατανομής για να προσδιοριστούν οι ιδιότητες συστημάτων που δεν βρίσκονται σε ισορροπία αλλά αλλάζουν με την πάροδο του χρόνου. Είναι απαραίτητο να χρησιμοποιηθεί η συνάρτηση κατανομής ταχύτητας και η χωρική συνάρτηση κατανομής, οι οποίες είναι οι ίδιες συναρτήσεις του χρόνου. [σελ.115] Οι πληροφορίες σχετικά με τον αριθμό των μορίων με δεδομένη ταχύτητα ονομάζονται συνάρτηση κατανομής ταχύτητας.
Ο χημικός δεσμός συνοδεύεται από μεταβολή της συνολικής ενέργειας του συστήματος και υπάρχουν διαφορετικοί τρόποι που πραγματοποιείται και εξηγείται έχοντας υπ' όψη με την ενέργεια ιοντισμού των χημικών στοιχείων, την ηλεκτραρνητικότητα, την ηλεκτροσυγγένεια Τα μόρια θεωρούνται κι αυτά συστήματα σωματιδίων (ατομα, υποατομικά σωματίδια)
Τα άτομα για να συγκροτούν μόρια χημικών στοιχείων ή χημικών ενώσεων απαιτείται ένα σύνολο δυναμικής ενέργειας. Είναι η ηλεκτρομαγνητική ενέργεια για να συγκρατούνται τα άτομα στο μόριο , η έλξη των μορίων και των υποατομικών σωματιδίων η περιστροφική κίνηση ατόμων και οι ταλαντώσεις τους
Η ενέργεια αυτή
ακατεργαστο
Συνάρτηση Κατανομής Ταχύτητας - Εγχειρίδιο Χημικού 21
Κατανομή ταχύτητας - Εγχειρίδιο χημικού 21
Για μη ιδανικά αέρια ή υγρά, απαιτείται μια χωρική συνάρτηση κατανομής για να προσδιοριστούν οι ιδιότητες συστημάτων που δεν βρίσκονται σε ισορροπία αλλά αλλάζουν με την πάροδο του χρόνου. Είναι απαραίτητο να χρησιμοποιηθεί η συνάρτηση κατανομής ταχύτητας και η χωρική συνάρτηση κατανομής, οι οποίες είναι οι ίδιες συναρτήσεις του χρόνου. [σελ.115] Οι πληροφορίες σχετικά με τον αριθμό των μορίων με δεδομένη ταχύτητα ονομάζονται συνάρτηση κατανομής ταχύτητας.
Έτσι, για να προσδιοριστεί η ιδιότητα ενός ιδανικού αερίου σε ισορροπία, είναι απαραίτητο να γνωρίζουμε τη συνάρτηση κατανομής της ταχύτητας. Για μη ιδανικά αέρια ή υγρά, απαιτείται μια συνάρτηση χωρικής κατανομής για τον καθορισμό των ιδιοτήτων συστημάτων που δεν βρίσκονται σε ισορροπία, αλλά αλλάζουν στο χρόνο, είναι απαραίτητο να χρησιμοποιηθούν συναρτήσεις κατανομής ταχύτητας και χωρικής κατανομής, οι οποίες είναι οι ίδιες συναρτήσεις του χρόνου.
Έτσι, για να προσδιοριστεί η ιδιότητα ενός ιδανικού αερίου σε ισορροπία, είναι απαραίτητο να γνωρίζουμε τη συνάρτηση κατανομής της ταχύτητας. Για μη ιδανικά αέρια ή υγρά, απαιτείται μια συνάρτηση χωρικής κατανομής για τον καθορισμό των ιδιοτήτων συστημάτων που δεν βρίσκονται σε ισορροπία, αλλά αλλάζουν στο χρόνο, είναι απαραίτητο να χρησιμοποιηθούν συναρτήσεις κατανομής ταχύτητας και χωρικής κατανομής, οι οποίες είναι οι ίδιες συναρτήσεις του χρόνου.
Οι πληροφορίες σχετικά με τον αριθμό των μορίων που έχουν μια δεδομένη ταχύτητα ονομάζονται συνάρτηση κατανομής ταχύτητας. Σε αυτή την περίπτωση, τέτοιες πληροφορίες δίνουν άμεσα την τιμή της συνολικής ενέργειας του συστήματος, αφού είναι το αριθμητικό άθροισμα των κινητικών ενεργειών όλων των επιμέρους σωματιδίων. Αν N v ) σημαίνει τον αριθμό των μορίων που έχουν ταχύτητα, τότε η συνολική κινητική ενέργεια (υποθέτοντας ότι οι μάζες είναι ίδιες) θα είναι ίση με [σελ.114]
Αυτή η υπόθεση μπορεί να θεωρηθεί ως ανάλογο της συνθήκης Lyapunov στο κεντρικό οριακό θεώρημα, και σημαίνει ότι οι μικρές αποκλίσεις είναι πιο πιθανές από τις μεγάλες σε μικρές χρονικές περιόδους. Μια πειραματική μελέτη του φάσματος του μετώπου υδροδυναμικής διαταραχής, που πραγματοποιήθηκε σε μια σειρά εργασιών [10-12], δείχνει ότι η πυκνότητα της συνάρτησης κατανομής ταχύτητας των σωματιδίων ενός διεσπαρμένου μέσου μειώνεται γρήγορα με την απόσταση από το κέντρο κατανομής. Το τελευταίο επιβεβαιώνει την αποδεκτή υπόθεση.
Οι δυσκολίες στη μέτρηση των διεγερμένων καταστάσεων των προϊόντων ανασυνδυασμού σχετίζονται με την ευαισθησία των μεθόδων μέτρησης διεγερμένων καταστάσεων σε τραχύ περιβάλλον. Για παράδειγμα, τα μόρια οξυγόνου και αζώτου δεν είναι πολικά μόρια των οποίων οι δονητικές καταστάσεις είναι ισχυρές. Οι διεγερμένες ηλεκτρονικές καταστάσεις τους έχουν μεγάλη διάρκεια ζωής και δεν εκπέμπουν πολύ. Επομένως, πρέπει να χρησιμοποιούνται άλλες μέθοδοι, όπως, για παράδειγμα, φθορισμός που προκαλείται από λέιζερ ή ιονισμός πολυφωτονίων λέιζερ. Οι μοριακές δέσμες είναι πολύ αποτελεσματικές για τη μελέτη του ανασυνδυασμού σε ορισμένες επιφάνειες. Συγκεκριμένα, μπορούν να χρησιμοποιηθούν για τη μελέτη του χρόνου παραμονής προσροφημένων ατόμων ή μορίων σε μια επιφάνεια. Οι μετρήσεις καθιστούν δυνατό τον προσδιορισμό της συνάρτησης κατανομής ταχύτητας και του ρυθμού ανασυνδυασμού. Οι πληροφορίες σχετικά με την κατανομή των σωματιδίων στην επιφάνεια μπορούν να αποτελέσουν τη βάση για μοντέλα που λαμβάνουν υπόψη τη διεγερμένη κατάσταση των σωματιδίων σε ετερογενή ανασυνδυασμό. [σελ.35]
Ας εξετάσουμε τώρα τη χρήση των συναρτήσεων ταχύτητας (1) και κατανομής παλμών (p). Ισορροπία Οι συναρτήσεις Maxwellian της μορφής (1,69) κανονικοποιούνται από τον αριθμό των σωματιδίων ενός δεδομένου τύπου (μέγεθος P). [σ.24]
Η έννοια της μέσης μάζαςΗ εξίσωση κίνησης του μείγματος περιλαμβάνεται στο σύστημα εξισώσεων του υπό εξέταση προβλήματος, στο οποίο η ταχύτητα του υγρού σωματιδίου νοείται ως η μέση ταχύτητα μάζας, δηλαδή w = wp. Το ζήτημα της ισοδυναμίας της μέσης ταχύτητας μάζας ενός μείγματος και της ταχύτητας ως κινηματικής έννοιας στη μηχανική ενός ρευστού και ενός αερίου εξετάζεται λεπτομερώς στο [1.3] με βάση τη συνάρτηση κατανομής ταχύτητας για έναν δεδομένο τύπο μορίου [σελ.31]
Συναρτήσεις κατανομής ταχύτητας και η εξίσωση Boltzmann [σελ.539]
Μετάβαση από Η συνάρτηση κατανομής ταχύτητας στη συνάρτηση κατανομής ακτίνας μπορεί να προκύψει από τις γνωστές σχέσεις που δίνονται κατά τη διάρκεια της χημείας των κολλοειδών. [σελ.183]
Με τη βοήθεια της συνάρτησης κατανομής που βρέθηκε, είναι δυνατό να προσδιοριστεί η πυκνότητα του αριθμού των σωματιδίων στην περιοχή αραίωσης πίσω από το σώμα ενσωματώνοντας τη συνάρτηση κατανομής ταχύτητας [σελ.96]
Στο [39, 41] με βάση την κινητική εξίσωση για τη συνάρτηση κατανομής με ταχύτητες, συντεταγμένες και θερμοκρασίες στερεών σωματιδίων Λαμβάνεται επίσης μια εξίσωση για τη μέση θερμοκρασία των στερεών σωματιδίων. Ορισμένες γενικεύσεις του συστήματος εξισώσεων μεταφοράς έχουν επίσης ληφθεί στο [43, 44, 47]. Για παράδειγμα, στο [47] μια εξίσωση για τη ροπή της ποσότητας [σελ.52]
η συνάρτηση κατανομής ταχύτητας του Maxwell έχει τη μορφή [σελ.91]
Δηλώνοντας τις συναρτήσεις κατανομής ταχύτητας των μορίων Α και Β μέσω /a (ub) και /b (ub) και αντικαθιστώντας τα μαζί με το (12.17) έως το (12.2), παίρνουμε ένα σύστημα δύο ολοκληρωτικές εξισώσεις για τις συναρτήσεις κατανομής /a και /b. [σελ.140]
Η μετάβαση από τη συνάρτηση κατανομής με ρυθμούς εναπόθεσης f(y) στη συνάρτηση κατανομής ακτίνας f(l) γίνεται με τον τύπο [σελ.199] Μετά από I 3,5 Hg,
οι διαδικασίες μέγιστης διόγκωσης μέσα σε κάθε αέριο και η διαδικασία μεταφοράς ενέργειας από Τα μόρια αργού σε μόρια μεθανίου έρχονται σε δυναμική ισορροπία μεταξύ τους και οι συναρτήσεις κατανομής ταχύτητας αποκτούν μια μορφή Maxwell. Το σύστημα έρχεται σε κατάσταση πλήρους ισορροπίας με χρόνο i 12 τόνους,-.
Ταυτόχρονα, μόνο οι ισότροπες συνιστώσες της συνάρτησης κατανομής ταχύτητας σε πεδία σταθερής και υψηλής συχνότητας συμπίπτουν. Κατά συνέπεια, μόνο χαρακτηριστικά που εξαρτώνται από το μέγεθος της ταχύτητας, αλλά όχι από την κατεύθυνσή της, μπορούν να χρησιμοποιηθούν για σύγκριση. Έτσι, πολλά πειραματικά και θεωρητικά αποτελέσματα που λαμβάνονται για ορισμένες καταστάσεις μπορούν να επεκταθούν και σε άλλες. [περ.250]



 οπότε
οπότε 
 σημειώνεται πως
σημειώνεται πως