της Δήμητρας Σπανού, χημικού, καθηγήτριας Δευτ/θμιας Εκ/σης μόνιμης στο 1ο Γυμνάσιο Δάφνης

Ένα ποιήμα του Ιωάννη Γρυπάρη
Ὁ λύχνος τῆς ψυχῆς
Πάρε τὸ λύχνο τῆς ψυχῆς ποὺ ἂν τρέμει μὰ δὲ σβήνει
καὶ τὰ σκοτάδια τὰ πηχτὰ στὸ λίγο φῶς ποὺ χύνει
ἀριοπερίχυτα ἂς διαβοῦν κι ἀτράνταχτα ἂς μεριάσουν
κι οἱ πεντασκότιδες σπηλιὲς ἂς ξεμεσημεριάσουν.
Σκιαχτὰ τ᾿ ἀγρίμια οὐρλιάζοντας στὰ βάθη ἀποτραβιοῦνται,
μὲ τὶς οὐρές τους δέρνονται καὶ μὲ τὰ νύχια σκιοῦνται,
σὰ νὰ μὴ φτάνει ὁ τρόμος τους μονάχα νὰ τοὺς δώσει
δρόμο νὰ φύγουνε τὸ φῶς ποὺ θὰ τὰ περιζώσει.
ΤΑ ΕΝΖΥΜΑ ΚΑΙ ΤΑ ΕΝΖΥΜΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΤΗς ΤΡΟΦΗΣ.

Μια χημική αντίδραση για να γίνει, πρέπει να ξεπεράσει την ενέργεια μιας ενδιάμεσης κατάστασης που είναι πάντα υψηλότερη από αυτης των αντιδρώντων την λεγόμενη ενέργεια ενεργοποίησης. Αυτό συνήθως γίνεται με την παροχή ενέργειας στα αντιδρωντα συνήθω με την μορφή θερμότητας, ώστε να φτάσουν στο σημείο της ενδιάμεσης ενέργειας ενεργοποίησης και να ξεκινήσει η αντίδραση.

Υπάρχουν ουσίες που όταν συνυπάρχουν με τα σώματα της αντίδρασης έχουν την ικανότητα να καταβιβάζουν την ενέργεια ενεργοποίησης
ώστε επιταχυνει την αντίδραση χωρίς να επηρεάζει την τελική θέση είναι η κατάλυση. Πολύ κοινή στις αντιδράσεις της Βιοχημείας είναι η κατάλυση εφόσον οι αντιδράσεις πρέπει να ολοκληρωθούν σε ορισμένο χρονικό διάστημα χωρίς η θερμοκρασία του κυττάρου να ξεπεράσει τους 37 βαθμούς Κελσίου. Οι βιολογικοί καταλύτες που είναι πρωτεινικής φύσης που ονομάζονται ένζυμα είναι ο συνηθισμένος τρόπος διεξαγωγής των βιοχημικών αντιδράσεων στο κύτταρο.
Τα ένζυμα στις χημικές αντιδράσεις παραμένουν αναλοίωτα μετά το τέλος τους και μπορούν να καταλύσουν την ίδια αντίδραση πολλές φορές και για αυτό απαντώνται σε μικρές ποσότητες.
Παρουσιάζουν μικρή ή μεγάλη εξειδίκευση στις αντιδράσεις που καταλύουν.
Τα αντιδρώντα και τα προιόντα της αντίδρασης που καταλύει ένα ένζυμο, λέγονται υποστρώματα του ενζύμου αυτού
.jpg)
Κατά την αντίδραση το αντιδρών ονομάζεται υπόστρωμα (S) και μετατρέπεται σε προιόν (P). Στην ενζυμική κατάλυση αρχικά γίνεται η πρόσδεση του υποστρώματο πάνω στο ένζυμο σε ένα σημείο (σημείο πρόσδεσης) με δεσμούς υδρογόνου, δυνάμεις Van der Walls ή ηλεκτροστατικές δυνάμεις.
Η κατάλυση γίνεται σε άλλη κατάλληλα διαμορφωμένη περιοχή το ενεργό κέντρο. Αυτό αποτελείται από ομάδες αμινοξέων που μπορεί να βρίσκονται και μακρυά, όμως η τριτοταγής δομή της πρωτείνης τις κάνει να πλησιάζουν κοντα.
Στις οξειδοαναγωγικές αντιδράσεις του οργανισμού, υπάρχουν ένζυμα που ενώνονται απευθείας με το οξυγόνο (οξειδάσες ) είτε από άλλο υπόστρωμα (δευδρογονάσες ή ρεδουκτάσες)
Πολλά από αυτά για να δράσουν χρειάζονται ένα πρόσθετο τμήμα μη πρωτεινικό. όπως ένα μεταλλικό ιόν, ή ένα μικρό οργανικό μοριο, που ονομάζεται συνένζυμο.
Η ΓΛΥΚΟΛΥΣΗ και τα ΕΝΖΥΜΑ ΤΗΣ

Εξακινάση (Hexakinase)
.JPG)
Βήμα1: Φωσφρυλίωση της Γλυκόζης σε 6φωσφορικη γλυκόζη με την δαπάνη ενός μορίου ATP που μετατρέπεται σε ΑDP.
Γίνεται με το Ένζυμο Εξακινάση. Είναι ένζυμο που υπάγεται στις φωσφοκινάσες οι οποίες επιφέρουν φωσφορυλιώσεις χωρίς την διάσπαση του γλυκοσιδικού δεσμού. Η εξακινάση φωσφορυλιώνει την γλυκόζη, στο 6ο άτομο άνθρακα. Ανάλογα με τον τύπο της εξακινάσης για την γλυκόζη (γλυκοκινάση) υπάρχουν οι γαλακτοκινάση και η φρουκτοκινάση για την φωσφορυλίωση της γαλακτόζης και της φρουκτόζης
Να σημειώσουμε ότι, απουσία γλυκόζης οι δυο λοβοί της εξακινάσης είναι διαχωρισμένοι. Με την πρόσδεση της γλυκόζης η στερεοδιάταξη του ενζύμου αλλάζει και οι δυο λοβοί πλησιάζουν ο ένας το άλλον και περιβάλλουν το υπόστρωμα και δημιουργούν ευνοικές συνθήκες για την κατάλυση
.jpg)
Ισομεράση της φωσφορικής γλυκόζης (Phospho glycose isomerase)
Βήμα2. Ισομεριωση της 6φωσφορικής γλυκόζηςι προς μια πεντόζη την 6φωσφορική φρουκτόζη .
Η υδρόλυση του ATP είναι εδώ αποτέλεσμα δυο αντίθετων αντιδράσεων που δεν δίνουν τελικό προιόν αλλά παροδικά ενέργεια.
6Φωσφορική Γλυκόζη + ΑTP <--> 1,6 διφωσφορική Γλυκόζη + ΑDP
Φωσφοφρουκτοκινάση (Phosphofructokinase)
 Βήμα3. Δεύτερη φωσφορυλίωση της 1 φωσφορικής φρουκτόζης με δότη την ATP στην θέση 1. Το ένζυμο που καταλύει την δεύτερη φωσφορυλίωση είναι η κινάση της 6φωσφοφρουκτόζης, ένα ενζυμο που έχει αλλοεστερικές ιδιότητες.
Βήμα3. Δεύτερη φωσφορυλίωση της 1 φωσφορικής φρουκτόζης με δότη την ATP στην θέση 1. Το ένζυμο που καταλύει την δεύτερη φωσφορυλίωση είναι η κινάση της 6φωσφοφρουκτόζης, ένα ενζυμο που έχει αλλοεστερικές ιδιότητες.
αλδολάση διφωσφορικής φρουκτόζης ( Fructose biphosphate aldolase) 
Βήμα4 . Η διφωσφοφρουκόζη διασπάται σε δύο μόρια από 3 άτομα άνθρακα το κάθε ένα που είναι : ένα μόριο φωσφο-γλυκερυναλδεύδης και ένα μόριο φωσφοδιυδ6ροξυκετόνη PO4CH2COCH2(OH). με την βοήθεια του ενζύμου αδολάση. H φωσφοδιυδροξυκετόνη μετατρέπεται σε φωσφογλυκεριναλδεύδη.
ισομεράση των φωσφορικων τριοζών (triose phosphate isomerase)
5. Βήμα . H φωσφορική υδροξυκετόνη ισομεριώνεται και δίνει επίσης την 3fωσφορική Dγλυκεριναλδεύδη. Ένζυμο ηι ισομεράση των φωσφορικων τριοζών
.JPG)
Αυτό το ένζυμο αποτελείται από το ενεργό κέντρο του με βασικά στοιχεία το γλουταμινικό και την ιστιδίνη και οκτώ παράλληλες αλυσίδες που περιβάλλονται γύρω από οκτώ έλικες και δίνουν το σχήμα "βαρέλι" Τον τύπο αυτό της στερεοχημικής δομής ενζύμου τον συναντάμε και σε άλλα ένζυμα όπως κινάση , αλδολάση του πυροσταφυλικου

αφυδρογονάση και φωσφογλυκοκινάση
Βήμα 6 Δεύτερη φωσφρυλίωση της Pγλυκερυναλδεύδης
αφού πρώτα γίνει αφυδρογόνωση, ενυδάτωση και τελικά φωσφορυλίωση.
.JPG)
Το ένζυμο της αφυδρογόνοσης, e;inai μια αφυδρογονάση poy περιέχει κυστείνη και προσθετική ομάδα το ΝΑD+
Βήμα7ο Οξειδωτική φωσφορυλίωση όπου η 3φωσφορική γλυερυναλδεύδη οξειδώνεται προς γλυκερινικό οξύ
Η 3φωσφορική γλυερυναλδεύδη ι δέχεται μια δεύτερη φωσφορυλίωση και δημιουργείται ένα διφωσφορικό σύμπλοκο υψηλής ενέργειας και ταυτόχρονα
ΤΑ ΕΝΖΥΜΑ ΣΤΟΝ ΚΥΚΛΟ ΤΟΥ ΚΙΤΡΙΚΟΥ ΟΞΕΟΣ
Πυροσταφυλική δευδρογονάση (PDH)
Η μετατροπή του πυροσταφυλικού σε ακέτυλοσυνένζυμο Α και η δημιουργία κιτρικού οξέος ώστε να ξεκινήσει το κύκλος του Κρεμπς
Η αντίδραση γίνεται σε τρία στάδια 1. αποκαρβοξυλίωση 2. Οξείδωση 3. Σχηματισμός του ακέτυλοσυνενζύμουΑ

Η μετατροπή του πυροσταφυλικού σε ακέτυλοσυνένζυμο Α είναι μια αντίδραση οξειδωτικής αποκαρβοξυλίωσης που καταλύεται από ένα σύμπλεγμα τριών ενζύμων την πυροσταφυλική δευδρογονάση (PDH)
Η πυροσταφυλική αφυδρογονάση είναι σύμπλεγμα από τρία ένζυμα την πυροσταφυλική αφυδρογονάση, την Διυδρολιπουλοτρανσακετυλάση και την διυδρολιπουλοαφυδρογονάση και πέντε συνένζυμα την πυροφωσφορική θειαμίνη, (ΤPP) το λιποικό οξύ , το FAD,(συμπαράγοντες)και το CoA και το NAD+(στοιχειομετρικοί συμπαράγοντες)
Στην αρχή γίνεται η αποκαρβοξυλίωση από την πλευρά της δευδρογονάσης του πυροσταφυλικού με την βοήθεια του συνενζύμου πυροφωσφορικής θειαμίνης (TPP)
Στο δεύτερο από τα 3 ένζυμα του συμπλέγματος η τρανακετυλάση του δενδρολιποικού μια μονάδα του η ακυλολιπουλολυσίνη οξειδώνεται με την αφαίρεση υδρογόνου από το τρίτο ένζυμο που είναι η δευδρογονάση του δευδρολιποικού.
Έτσι η ακυλομάδα που έχει μείνει απότοπυροσταφυλικό, προσδένεται σε θείο της μονάδας της ακυλολιπουλολυσίνη και έτσι μεταφέρεται στο συνένζυμο Α για να δώσει το ακέτυλοσυνένζυμο Α
κιτρική συνθάση
1ο βήμα Συμπύκνωση του ακέτυλοσυνένζυμουΑ και του οξαλοξικού οξέος από όπου προκύπτει το κιτρικό οξύ
 Η αντίδραση καταλύται από το ένζυμο κιτρική συνθάση. Πρέπει η παραγωγή του κιτρικού να έχει υψηλή απόδοση και γι αυτόν τον λόγο το ένζυμο αυτό φροντίζει αρχικά να περιορίσει άλες παράπλερες αντιδράσεις (λ.χ. Υδρόλυση του ακέτυλοσυνένζυμουΑ) κατά την πορεία της αντίδρασης το ένζυμο υφίσταται στερεοχημικές αλλαγές και ενώνεται πρώτα με το οξαλοξικό και στην συνέχεια με το ακέτυλοσυνένζυμοΑ.
Η αντίδραση καταλύται από το ένζυμο κιτρική συνθάση. Πρέπει η παραγωγή του κιτρικού να έχει υψηλή απόδοση και γι αυτόν τον λόγο το ένζυμο αυτό φροντίζει αρχικά να περιορίσει άλες παράπλερες αντιδράσεις (λ.χ. Υδρόλυση του ακέτυλοσυνένζυμουΑ) κατά την πορεία της αντίδρασης το ένζυμο υφίσταται στερεοχημικές αλλαγές και ενώνεται πρώτα με το οξαλοξικό και στην συνέχεια με το ακέτυλοσυνένζυμοΑ.
ακοκινάση
2ο βήμα
.JPG)
Η αφυδάτωση του κιτρικού οξέος σε sic ακονικιικό και συνέχεια η ενυδάτωση ισοκιτρικό οξύ
Για να μεταφερθεί το ΟΗ σε μια θέση πιο "βολική"για την αποκαρβοξυλίωση. επιδρά το ένζυμο ακοκινάση που περιέχει θείο και σίδηρο που δεν είναι ενωμένος και έτσι συντελεί στην αφυδάτωση του κιτρικού και στην ενυδάτωσή του στην συνέχεια προς ισοκιτρικό.
ακονιτάση
3ο βήμα. Το ισοκιτρικό οξειδώνεται και μετατρέπεται σε α κετογλουταρικό οξύ
Είναι η πρώτη οξείδωση του κύκλου) και γίνεται με την παρουσία ενζύμου που είναι πάλι ακοκινάση που χρησιμοπιήθηκε στο προηγούμενο στάδιοτης ισομερίωσης. Για την αφυδρογόνωση που προηγείται της αποκαρβοξυλίωσης υπάρχουν δυο συνένζυμα το NAD και το NADP Μάλιστα υπάρχουν δυο ανάλογα ένζυμα στα μιτοχονδρια που χρησιμοποιούν NAD ή NADP σαν συνένζυμα. Με αφυδρογόνωση δημιουργείται κετοξύ το οξαλοηλεκτρικό που αυθόρμητα στο ίδιο ενζυμο γίνεται μια πρώτη αποκαρβοξυλίωση του 3ου άνθρακα, που συνδέεται επίσης στον σίδηρο της ακοκινάσης.
Παράγεται α κετογλουταρικό οξύ εφόσον ο δεύτερος άνθρακας μετατρέπεται σε κετονικό
Τα συνένζυμα ΝΑD ή ΝΑΔP που μετατρέπονται σε ανηγμένα NADH ή NADPH (συζευγμένη αντίδραση)
α κετογλουταρικής αφυδρογονάσης
4ο βήμα. Το α κετογλουταρικό οξύ μετατρέπεται σε ηλεκτρυλοσυνένζυμοΑ
Εδώ ένα κετοξύ αποκαρβοξυλιώνεται με αποτέλεσμα τον σχηματισμό ενός υψηλής ενέργειας θειοεστερικού δεσμού με το 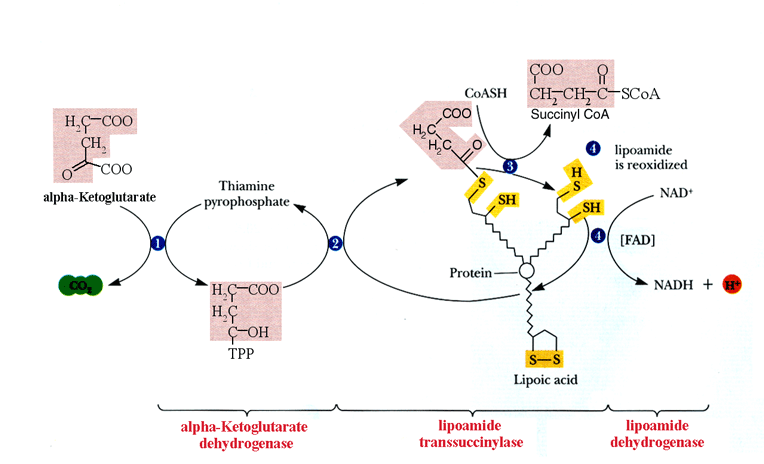 συνένζυμο
συνένζυμο
Γίνεατι με την παρουσία συμπλέγματος τριών ενζύμων και πέντε συνενζύμων NAD TPP, FAD, λιποιδικού οξέος και συνένζυμουΑ, της α κετογλουταρικής αφυδρογονάσης)
Στο πρώτο στάδιο Το α κετογλουταρικό οξύ χάνει αρχικά το ένα καρβοξύλιό με ένζυμο είναι την κετογλουταρική αποκαρβοξυλάση με συνένζυμο την πυροφωσφορική θειαμίνη (TPP), ενώ παράλληλα απομακρύνεται Υδρογόνο (α αφυδρογόνωση ) και μετατρέπεται σε ηλεκτρική μονοαλδεύδη ( COOHCH2CH2CHO) με συνένζυμο το NAD που προσλαμβάνει ενέργεια και μετατρέπεται σε ανηγμένο NADH.
Στην συνέχεια η ηλεκτρική μονοαλδεύδη ( COOHCH2CH2CHO) με το ενζυμο αφυδρογονάση και συνένζυμοτο NAD+ παρουσία του συνενζύμουΑ
ενώνεται με το συνένζυμοΑ με έναν θειοεστερικό δεσμό υψηλής ενέγειας με το ηλεκτρικό οξύ (4 άνθρακες) που προκύπτει από την αποκαρβοξυλίωση.
Το ακετυλο συνένζυμο Α αποβάλει την ακετυλομάδα του και Έτσι παίρνουμε το ηλεκτρυλοσυνένζυμοΑ . Η συνολική ελεύθερη ενέργεια ΔG= -30kj/mol
Συπέρασμα: Παραφωγή 1 μοριο CO2 κια 1 μόριο NADH
ηλεκτρική συνθετάση
5ο βήμα. Το ηλεκτροσυνένζυμο Α μετατρέπεται σε ηλεκτρικό οξύ
e.JPG)
Η ηλεκτρική συνθετάση μεταφέρει αποδεσμέυει το συνένζυμο Α από το ηλεκτροσυνένζυμοΑ χρησιμοποιώντας μια φωσφορική ομάδα. Την ομάδα αυτή μεταφέρει στην συνέχεια στο ADP μετατρέποντάς το σε ATP. ( Αυτό σημαίνει επίσης και την μεταφορά ενέργειας του θειοεστερικού δεσμού σε ενέργεια μεταφοράς φωσφορικών ομάδων στο ATP).
To ΑDP για να φnωσφορυλιωθεί προσδένεται σε αμινοτελική περιοχή του ενζύμου όπου σχηματίζεται πτυχή για καλύτερη πρόσδεση και ενεργοποίηση .
ηλεκτρική αφυδρογονάση
Βήμα 6ο Το ηλεκτρικό οξύ μετατρέπεται σε φουμαρικό με το ένζυμο ηλεκτρική αφυδρογονάση. Το συνένζυμο -δέκτης του υδρογόνου είναι το FAD του οποίου δακτύλιος προσδένεται σε ένα μόριο ιστιδίνης του ενζύμου. 
Η ηλεκτρικη αφυδρογονάση είναι μια πρωτείνη σιδήρου θείου. Πέριέχει σε τρία σημεία του συμπλοκοποιημένα σίδηρο και Θείο
Το ένζυμο που χρησιμοποιείται έχει στρεχημική εξειδίκευση ώστε να αφαιρεθούν trans ηλεκτρόνια και να δημιουργηθεί ο διπλός δεσμός του φουμαρικού οξέος. Διαφέρει από τα άλλα ένζυμα, γιατί είναι πάνω στην μιτοχονδριακή μεμβράνη και συνδεεται με την αλυσίδα μεταφοράς ηλεκτρονίων Η αντίδραση είναι αμφίδρομη.
φουμαρική υδατάση
Βήμα 7ο Ενυδάτωση του φουμαρικού οξέος και παραγωγή μηλικού με ένζυμ την φουμαράση (υδατάση)
Η  ενυδάτωση του φουμαρικού στον διπλό δεσμό του δίνει μηλκό οξύ με ένζυμο την φουμαρική υδατάση. Παράγονται δύο τύπων φουμαράσες η μια στα μιτοχόνδρια και μια στο κυτοσόλιο
ενυδάτωση του φουμαρικού στον διπλό δεσμό του δίνει μηλκό οξύ με ένζυμο την φουμαρική υδατάση. Παράγονται δύο τύπων φουμαράσες η μια στα μιτοχόνδρια και μια στο κυτοσόλιο
μηλική αφυδρογονάση
Βήμα 8ο
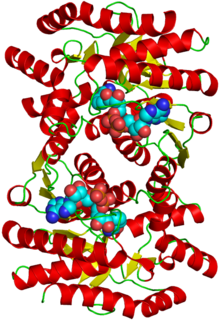
Δημιουργία του οξαλοξικού οξέος από το μηλικό οξύ με ένζυμο την μηλική αφυδρογονάση και συνένζυμο το NAD (4άνθρακες)
Η μηλική αφυδρογονάση αφαιρεί υδρογόνο από την υδροξυλομάδα του μηλικού και την οξειδώνει σε ομάδα καρβονυλίου
TΑ ΕΝΖΥΜΑ ΣΤΗΝ ΑΝΑΠΝΕΥΣΤΙΚΗ ΑΛΥΣΙΔΑ
Α. τα δυο βοηθητικά υποστρώματα ουβικινόνη και κυτόχτωμα c
1. Ουβικινόνη (ενεργό κέντρο)
Η ουβικινόνη ή συνένζυμο Q10 απαραίτητη στην αναπνευστική αλυσίδα, βρίσκεται σε πολλές φυτικές και ζωικές πηγές όπως σόγια, κοτόπουλο, μοσχάρι, χοιρινό, ελαιόλαδο, μπρόκολο, κουνουπίδι, σπανάκι, φρούτα. Είναι ακόμα και ένα σπουδαίο αντιοξειδωτικό για τον οργανισμό αφού εξουδετερώνει ελεύθερες ρίζες.
2.Κυτόχρωμα c
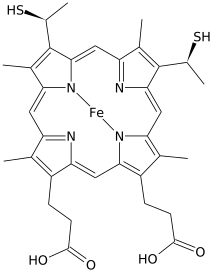

Είναι χαλαρά συνδεδεμένο στην μιτοχονδρακή μεμβράνη προς την μεριά του ενδιάμεσου χώρου του μιτοχονδρίου. Είναι μια υδροδιαλυτή πρωτείνη με προσθετική ομάδα την αίμη. που συνδέεται με 2 τύπων δεσμούς, έναν σταθερό θειοεστερικό και έναν αμινοξέων της πρωτείνης ιστιδίνης και μεθειονίνης που συντονίζονται με τον σίδηρο της αίμης
. Η ουβικονόνη υφίσταται μερική αναγωγή σε ημικινόνη. Τα ηλεκτρόνια μεταφέρονται στο . κυτόχρωμα b του δεύτερου σύμπλοκου, μέσω μιας πρωτείνης που περιέχει σίδηρο και είναι συνδεδεμένη με το κυτόχρωμα b.
B . Τα 4 κύρια ένζυμα της αναπνευστικής αλυσίδας
Συμπλεγμα Ι
1. NADH αναγωγάση του συνένζυμου Q10 (ουβικινόνης). -Mitochondrial NADH:ubiquinone oxidoreductase (complex I)
Είναι η πρώτη αντλία πρωτονίων από την εσωτερική πλευρά του μιτοχονδρίου στην έξω πλευρά της μεμβράνης του
Μεγάλο ένζυμο από 34 πολυπεπτιδικές αλυσίδες. Προσθετική ομάδα το φλαβινομονονουκλεοτίδιο FNA. Περιλαμβάνει ομάδα συμπλόκων
S-Fe (Fe4S4 και Fe2S2) σετουλάχιστον 4 σημεία με οξειδοαναγωγικό δυναμικό γύρω στα -300mV
που σε αυτά βασίζονται οι αναγωγικές του ιδιότητες Fe+2 -> Fe+3
Σύμπλεγμα ΙΙ
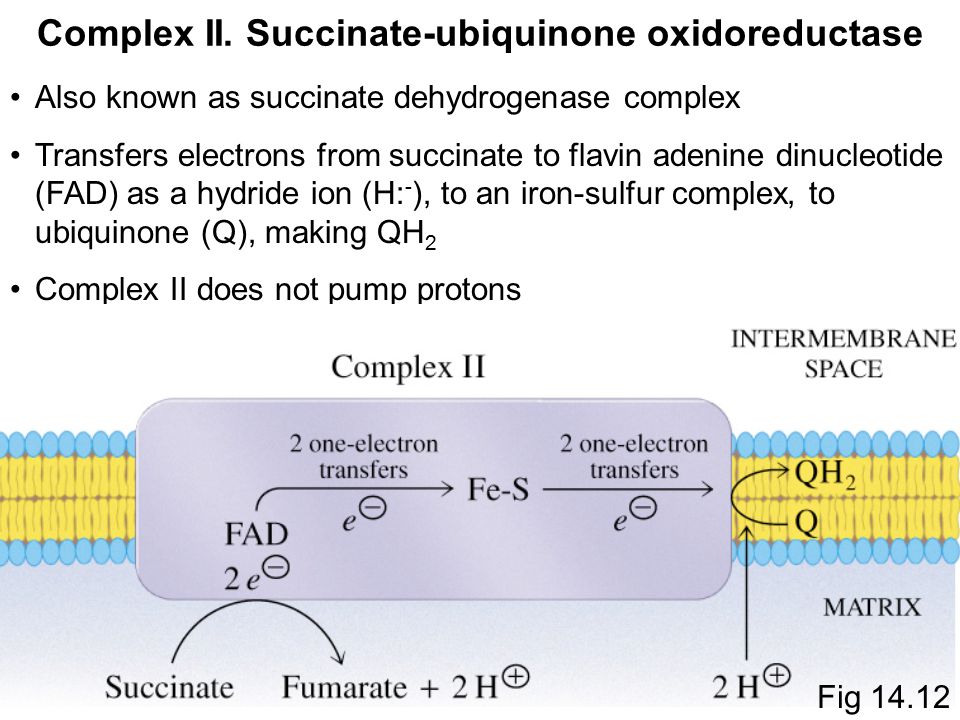
2.Αναγωγάση ηλεκτρικού- ουβικινόνης. -succinate ubiquinone oxidoreductase (complex II)
Ειναι ένζυμο του κύκλου του Κρεμπς εξειδικευμένο να μεταφέρει υδρογόνο και ηλεκτρόνια από το ηλεκτρικό οξύ στην ουβικινόνη. Περιέχει επίσης συνδεδεμένη μια πρωτείνη με FAD και δύο κέντρα το ένα Fe2S2 και το άλλο Fe4S4-πρωτείνη. Η ενέργειάτης δεν επαρκεί για την μεταφορά ηλεκτρονίων διαμέσου της μιτοχονδριακής μεμβράνης.
Σύμπλεγμα ΙΙΙ
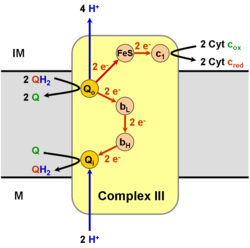
3.Αναγωγάση ουβιυδροκινόνης -κυτοχρώματος c (cytc ubiquinone reductase (complex III) )
Είναι σύμπλεγμα 3 κυτοχρωμάτων bk, b1,c και μιας πρωτείνης. Τα κυτοχρώματα Cyt bk, Cyt b1 έχουν προσθετική ομάδα την αίμη και διαφέρουν ως προς το δυναμικό οξειδναγωγής. στο Cb1 παρουσία ATP ανεβαίνει από -30 mV σε +245mV. To κυτόχρωμα c1 περιέχει την αίμη σε ομοιοπολική σύνδεση και αποτελεί πρωτείνη της μεμβράνης.. Το cytc που είναι χαλαρά συνδεδμένο, μετακινείται προς το συμπλοκο ΙV μετά την οξείδωσή του.
Σύμπλεγμα ΙV
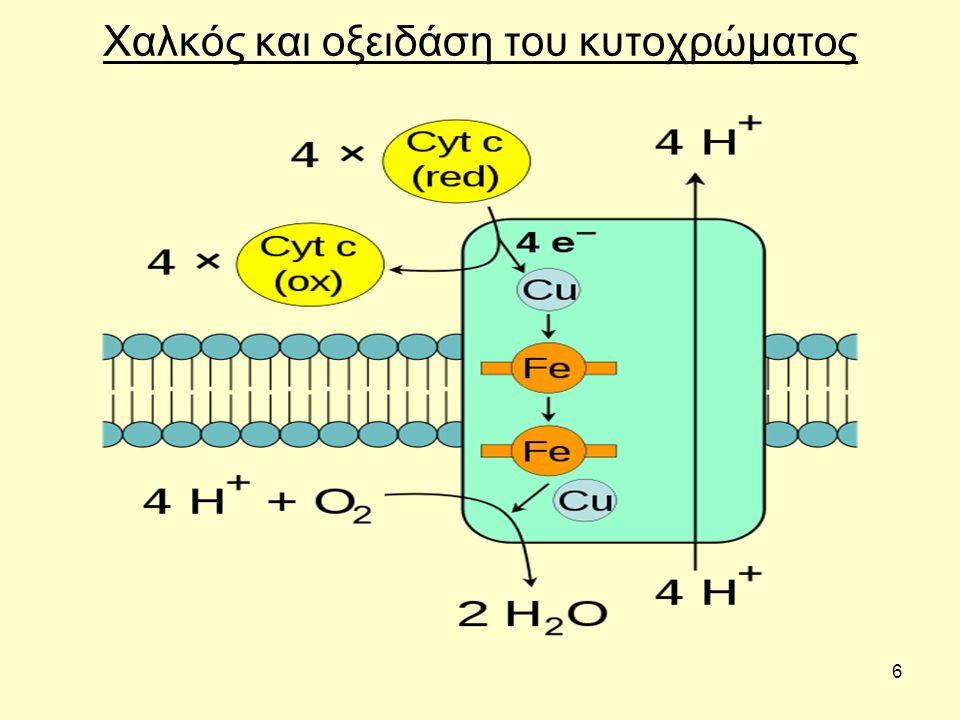
4. Οξειδάση του κυτοχρώματος c. - Oξειδωτικό ένζυμο cytochrome c oxidase
Είναι διαμεμβρανιακό πρωτεινικό σύμπλοκο, Περιέχει δύο μόρια χαλκού και δύο μόρια αίμης. Είναι το ένζυμο που αντιδρά με το οξυγόνο που το βρίσκει στο εσωτερικό του μιτοχονδρίο. Παραλαμβάνει τα ηλεκτρόνια από το κυτόχρωμαC και που βρίσκεται στην έξω πλευρά της μεμβράνης και τα μεταφέρει στο οξυγόνο που έρχεται από τον εσωτερικό χώρο. Με βάση τις οπτικές ιδιότητες και την ικανότητα ντίδρασης με το οξυγόνο διακρίνουμε δυο κυτοχρώματα το α και το α3 (εκτός από το c).που H θέση σλυνδεσης της αίμης με μια από τις πεπτιδικές αλυσίδες, δεν είναι ακριβώς
Το σύμπλοκο της οξειδωτικής φωσφορυλίωσης
Σύμπλοκο V
 Μιτοχονδριακή ΑΤΡάση. Αυτό το σύπλοκο βρίσκεται στα κομβία της μιτοχονδριακής μεμβράνης κπρος το εσωτερικό μέρος και αποτελείται από πρωτείνες με διαφορετικές λειτουργείες. Μια από αυτές συντελεί στην ενεργητική μεταφορά πρωτονίων στον χώρο του μιτοχονδρίο μεταξύ εσωτερικής και εξωτερικής μεμβράνης και έτσι συντελεί στην ανάπτυξη δυναμικού της έσω μεμβράνης με ενεργητικό τρόπο ενώ το ίδιο συμβαίνει και παθητικά λόγω ωσμοτικών φαινομένων κατά την υδρόλυση των συνενζύμων NADH. Ένα άλλο μέρος της ΑΤΡάσης η F απότελείται από κλάδους ,F1, F0, F6,... H F1 ΑΤΡάση κάνει την κυρίως κατάλυση. Αυτή η πρωτείνη , μπορεί να λειτουργήσει αντιστρεπτά, όταν αποχωριστεί από τον μίσχο και να κάνει υδρόλυση του ATP.
Μιτοχονδριακή ΑΤΡάση. Αυτό το σύπλοκο βρίσκεται στα κομβία της μιτοχονδριακής μεμβράνης κπρος το εσωτερικό μέρος και αποτελείται από πρωτείνες με διαφορετικές λειτουργείες. Μια από αυτές συντελεί στην ενεργητική μεταφορά πρωτονίων στον χώρο του μιτοχονδρίο μεταξύ εσωτερικής και εξωτερικής μεμβράνης και έτσι συντελεί στην ανάπτυξη δυναμικού της έσω μεμβράνης με ενεργητικό τρόπο ενώ το ίδιο συμβαίνει και παθητικά λόγω ωσμοτικών φαινομένων κατά την υδρόλυση των συνενζύμων NADH. Ένα άλλο μέρος της ΑΤΡάσης η F απότελείται από κλάδους ,F1, F0, F6,... H F1 ΑΤΡάση κάνει την κυρίως κατάλυση. Αυτή η πρωτείνη , μπορεί να λειτουργήσει αντιστρεπτά, όταν αποχωριστεί από τον μίσχο και να κάνει υδρόλυση του ATP.
Σε σύνδεση με το υπόλοιπο σύμπλεγμα, συντελεί στην δημιουργία του ATP από ADP και φωσφορικά. Η F1 κατά μια ερμηνέια ταλαντεύεται μεταξύ δύο θέσεων - χωροδιατάξεων. Σχηματίζεται σαν ενδιάμεση ουσία το φωσφορυλιωμένο ένζυμο καταναλώνοντας ενέργεια και μεταφέρει στην συνέχεια την φωσφορική ρίζα στο ADP.
Δήμητρα Σπανού
ΠΗΓΕΣ
https://slideplayer.gr/slide/11402851/
Βασική Βιοχημεία Κ. Δημόπουλος
Βιοχημεία Κανετάκης
Βασικές αρχές κυτταριής Βιολογίας A. Bray
https://en.wikipedia.org/wiki/Succinate_dehydrogenase
https://en.wikipedia.org/wiki/Malate_dehydrogenase
https://sites.google.com/site/chem471/06
https://www.chemistry.wustl.edu/~edudev/LabTutorials/Cytochromes/cytochromes.html
SlidePlayer.gr960 × 720Αναζήτηση βάσει εικόνας
6 6 Χαλκός και οξειδάση του κυτοχρώματος
SlidePlayer960 × 720Αναζήτηση βάσει εικόνας
15 Complex II. Succinate-ubiquinone oxidoreductase
Wikipedia250 × 248Αναζήτηση βάσει εικόνας
Coenzyme Q – cytochrome c reductase
Βιοχημεία (Γ Γενικού Λυκείου - Τεχνολογικής Κατεύθυνσης: Κύκλος ...
- Η γλυκερόλη αντιδρά με λιπαρά οξέα για να σχηματίσει λιπίδια:
CH 2 OHCH (OH) CH 2 ΟΗ + Γ 17 H 35 COOH → CH 2 OHCH (OH) CH 2 OOCC 17 H 35
- Τα απλά σάκχαρα συνδυάζονται για να σχηματίσουν δισακχαρίτες και νερό:
C 6 H 12 O 6 + Γ 6 H 12 O 6 → Γ 12 H 22 O 11 + Η 2 O
- Τα αμινοξέα συνδυάζονται για να σχηματίσουν διπεπτίδια:
NH 2 CHRCOOH + NH 2 CHRCOOH → NH 2 CHRCONHCHRCOOH + H 2 O.
- Το διοξείδιο του άνθρακα και το νερό αντιδρούν για να σχηματίσουν γλυκόζη και οξυγόνο κατά τη διάρκεια της φωτοσύνθεσης:
6CO 2 + 6Ώρες 2 Ο → Γ 6 H 12 O 6 + 6Ο2
Παραδείγματα καταβολισμού
Οι καταβολικές διεργασίες είναι το αντίθετο των αναβολικών διεργασιών. Χρησιμοποιούνται για την παραγωγή ενέργειας για αναβολισμό, την απελευθέρωση μικρών μορίων για άλλους σκοπούς, την αποτοξίνωση χημικών ουσιών και τη ρύθμιση μεταβολικών οδών. Για παράδειγμα:
- Στην κυτταρική αναπνοή, η γλυκόζη και το οξυγόνο αντιδρούν για να σχηματίσουν διοξείδιο του άνθρακα και νερό
C 6 H 12 O 6 + 6Ο 2 → 6CO 2 + 6Ώρες 2 O
- Στα κύτταρα, το υπεροξείδιο του υδροξειδίου διασπάται σε νερό και οξυγόνο:
2H 2 O 2 → 2 ώρες 2 Ο + Ο 2
Πολλές ορμόνες δρουν ως σήματα για τον έλεγχο του καταβολισμού. Οι καταβολικές ορμόνες περιλαμβάνουν επινεφρίνη, γλυκαγόνη, κορτιζόλη, μελατονίνη, υποκρετίνη και κυτοκίνες. Οι καταβολικές ασκήσεις είναι αερόβιες ασκήσεις, όπως οι αερόβιες προπονήσεις, που καίνε θερμίδες καθώς το λίπος (ή οι μύες) διασπάται.
Αμφιβολικές οδοί
Η μεταβολική οδός, η οποία μπορεί να είναι είτε καταβολική είτε αναβολική ανάλογα με τη διαθεσιμότητα ενέργειας, ονομάζεται αμφίβολη οδός. Ο κύκλος γλυοξυλικού και ο κύκλος κιτρικού οξέος είναι παραδείγματα αμφιβολικών οδών. Αυτοί οι κύκλοι μπορούν είτε να παράγουν ενέργεια είτε να τη χρησιμοποιούν, ανάλογα με τις κυτταρικές ανάγκες.



.jpg)


.jpg)
 Βήμα3. Δεύτερη φωσφορυλίωση της 1 φωσφορικής φρουκτόζης με δότη την ATP στην θέση 1. Το ένζυμο που καταλύει την δεύτερη φωσφορυλίωση είναι η κινάση της 6φωσφοφρουκτόζης, ένα ενζυμο που έχει αλλοεστερικές ιδιότητες.
Βήμα3. Δεύτερη φωσφορυλίωση της 1 φωσφορικής φρουκτόζης με δότη την ATP στην θέση 1. Το ένζυμο που καταλύει την δεύτερη φωσφορυλίωση είναι η κινάση της 6φωσφοφρουκτόζης, ένα ενζυμο που έχει αλλοεστερικές ιδιότητες. 

Η αντίδραση καταλύται από το ένζυμο κιτρική συνθάση. Πρέπει η παραγωγή του κιτρικού να έχει υψηλή απόδοση και γι αυτόν τον λόγο το ένζυμο αυτό φροντίζει αρχικά να περιορίσει άλες παράπλερες αντιδράσεις (λ.χ. Υδρόλυση του ακέτυλοσυνένζυμουΑ) κατά την πορεία της αντίδρασης το ένζυμο υφίσταται στερεοχημικές αλλαγές και ενώνεται πρώτα με το οξαλοξικό και στην συνέχεια με το ακέτυλοσυνένζυμοΑ.


 συνένζυμο
συνένζυμο 
 ενυδάτωση του φουμαρικού στον διπλό δεσμό του δίνει μηλκό οξύ με ένζυμο την φουμαρική υδατάση. Παράγονται δύο τύπων φουμαράσες η μια στα μιτοχόνδρια και μια στο κυτοσόλιο
ενυδάτωση του φουμαρικού στον διπλό δεσμό του δίνει μηλκό οξύ με ένζυμο την φουμαρική υδατάση. Παράγονται δύο τύπων φουμαράσες η μια στα μιτοχόνδρια και μια στο κυτοσόλιο