Δήμητρα Σπανού, χημικός, συνταξιούχος καθηγήτρια Μέσης Εκπαίδευσης από 30-6-2025
ΟΡΓΑΝΟΜΕΤΑΛΛΙΚΗ ΧΗΜΕΙΑ
Είναι η χημεία των ενώσεων στις οποίες ένα οργανικό υπόλειμμα ή ένωση συνδέεται άμεσα με ένα άτομο μετάλλου ή σπανιότερα άλλου ηλεκτροθετικού στοιχείου όπως το πυρίτιο και το Βόριο. Ο δεσμός C-A είναι κυρίως ομοιοπολικός (πολικός ή όχι). Η πολικότητα του δεσμού καθορίζει και την σταθερότητα αυτών των ενώσεων. Ενώσεις μετάλλων μεγάλης πολικότητας δεσμού Md+ - Cd - διασπώνται εύκολα. Τέτοιες είναι οι οργανομεταλλικές ενώσεις ομάδων Ι, ΙΙα, ΙV, V.
Η πολικότητα αντίθετα μειώνεται με την αύξηση του αριθμού των περιόδων . Οργανομεταλλικές ενώσεις μετάλλων κ.α. όπως Hg, Sn, Pb, Sείναι σταθερές με τα κατώτερα μέλη υγρά και τα ανώτερα στερεά, αντίθετα με τα κατώτερα αλκυλοπαράγωγα μετάλλων (ομάδας Ι) που είναι υγρά. Η πολικότητα καιαστάθεια αυξάνεται εκ νέου στις ομάδες IV, V
Για αντίστοιχο λόγο επίσης αυτό τα οργανικά άλατα που είναι ιοντικές ουσίες δεν εντάσσονται στις οργανομεταλικές ενώσεις γιατί είναι ιοντικές
Παρ' όλα αυτά, σε πολύπλοκες οργανομεταλλικές ενώσεις τα χαρακτηριστικά τους εξαρτώνται κατά πολύ από τη φύση των προσδεμάτων των υποκαταστατών και σε μικρότερο βαθμό από τη φύση του μετάλλου.
Γ
Ο ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ

ΠΟΙΕΣ ΕΙΝΑΙ ΟΙ ΟΡΓΑΝΟΜΕΤΑΛΛΙΚΕΣ ΕΝΩΣΕΙΣ
Οργανομεταλλικές ενώσεις, θεωρούνται οι χημικές ενώσεις στις οποίες άτομα άνθρακα ή οργανικές ομάδες συνδέονται απευθείας με άτομα μετάλλου, δηλαδή περιέχουν έναν δεσμό του ατόμου του άνθρακα ενός οργανικού μορίου και ενός μετάλλου.
Από τα μέταλλα οργανομεταλλικές δίνουν τα μέταλλα των αλκαλίων, των αλκαλικών γαιών και των μετάλλων μεταπτώσεως
Μερικές φορές ορισμένα μεταλλειοειδή όπως το Βόριο (Β) το Pυρίτιο (Si) και το Σελήνιο (Se) δίνουν οργανομεταλλικές ενώσεις
Τα κυανιούχα ( -C≡N), τα καρβίδια (MC) , και τα μεταλλικά καρβονύλια (>C=O) παρ' ότι περιέχουν δεσμό MC, δεν θεορούνται οργανομεταλλικές ενώσεις αλλά εντάσσονται στις ανόργανες ενώσεις
Ακόμη στις οργανομεταλλικές συμπεριλαμβάνονται οριακά και ορισμένες ενώσεις όπως υδρίδια μετάλλων μετάπτωσης (Na[AlH4]) , Na[BH4] και σύμπλοκα μεταλλικής φωσφίνης [Pt(PPh3)3] 2
ΤΥΠΟΙ ΔΕΣΜΩΝ ΣΕ ΟΡΓΑΝΟΜΕΤΑΛΛΙΚΕΣ ΕΝΩΣΕΙΣ
Έχουμε τύπους δεσμών:
1. Οργανομεταλλικές ενώσεις με Δεσμούς σ ομοιπολικούς (σιδηροκένιο-δις(κυκλοπενταδιενυλ)σίδηρος [Fe(C5H5)2] )
2. Οργανομεταλλικές ενώσεις με Δεσμούς π ομοιπολικούς δότη και π επαναφοράς και συνεργιτικός (-(υκλοπενταδιενυλ)σίδηρος [Fe(C5H5)2] )
3. Οργανομεταλλικές ενώσεις με Δεσμούς ιοντικούς (CH3-Na+)
4. Ηλεκτρονιακά φτωχοί δεσμοί
5. Οργανομεταλλικές ενώσεις με απεντοπισμένους Δεσμούς Μετάλλων
Α.ΟΡΓΑΝΟΜΕΤΑΛΛΙΚΕΣ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ σ και π
σ ΔΕΣΜΟΙ ΣΕ ΟΡΓΑΝΟΜΕΤΑΛΛΙΚΑ ΣΥΜΠΛΟΚΑ ομάδων Ι, ΙΙα, ΙV, V (ομοιοπολικά)
Οργανομεταλλικές Ενώσεις με δεσμούς MC τύπου σ σχηματίζουν κυρίως μη μεταβατικά μέταλλα ομάδων Ι, ΙΙα, ΙV, V.που περιέχουν μόνο δεσμούς MC πολυκεντρικούς δεσμούς. Οργανομεταλλικές ενώσεις μεταβατικών μετάλλων που συνδέονται με το μέταλλο με έναν ομοιοπολικό δεσμό (συνήθως με πολικό χαρακτήρα) σ δύο ηλεκτρονίων δύο κέντρων. Είναι λιγότερο σταθερές από αυτές των ομάδων Β ομάδων και προχωρούν με θραύση του δεσμου CM kai χρησιμοποιούνται στις οργανικές συνθέσεις. όπως η οργανομεταλικές ένωση Grignard
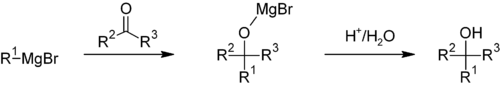
Tα οργανομεταλλικά των Li, Mg, Al, είναι ευαίσθητα στην υγρασία και το Ο2 του αέρα, ενώ αλκυλικά παράγωγα Li, Na, Be, Zn, Al, Ca, In, Tl, Sb, Bi αναφλέγονται αυθόρμητα στον αέρα
Πιθανόν αυτά τα σύμπλοκα να οδηγούνται σε προτιμητέες οδούς αποσύνθεσης λόγω του ακόρεστου χαρακτήρα των μετάλλων
Η ομάδα συνδέεται με το μέταλλο με έναν δίκεντρο ομοιοπολικό δεσμο δύο ηλεκτρονίων, πολλές φορές πολικού χαρακτήρα (Na(C5H5))
Οργανομεταλλικές Ενώσεις με δεσμούς MC τύπου σ σχηματίζουν επίσης και τα μεταβατικά μέταλλα
π ΔΕΣΜΟΙ ΣΕ ΟΡΓΑΝΟΜΕΤΑΛΛΙΚΑ ΣΥΜΠΛΟΚΑ (ομοιοπολικά)
Δεσμός δότη (βάση κατά Lewis) ( Υποκαταστάτες L)
- [Θυμόμαστε ότι : Βαση κατά Lewis είναι κάθε ουσία που μπορεί να προσφέρει ένα ζεύγος ηλεκτρονίων προς σχηματισμό ομοιοπολικού δεσμού] (π.χ. :ΝΗ3, Η2Ο:, Cl-, Ο2- , :ΝΟ3, :CO κ.α.)]
Οργανομεταλλικές με δεσμούς MC τύπου π σχηματίζουν κυρίως μεταβατικά μέταλλα που περιέχουν δεσμούς ΜC -ετεροάτομο.
¨οπως αναφέρθηκε, ενώσεις μετάλλων μεγάλης πολικότητας δεσμού Md+ - Cd - διασπώνται εύκολα. Τέτοιες είναι οι οργανομεταλλικές ενώσεις ομάδων Ι, ΙΙα, ΙV, V.
Η πολικότητα αντίθετα μειώνεται με την αύξηση του αριθμού των περιόδων και μαζί και η σταθερότητα των συμπλόκων..
Τα ετεροάτομα που συναντάμε σε δεσμούς τύπου π είναι ενώσεις που
συνδέονται με pi -όπως : οεφινικό, ακετυλένιο, αλλύλιο, κυκλοπενταδιένιο, καρβοράνιο.
Γειτνιάζουν με παράγωγα καρβονυλίου, ισονιτριλίου, κυανίου, καρβενίου
Εδώ,
τα (n-1)d τροχιακά των μεταβατικών μετάλλικών κέντρων των στοιχείων μεταπτώσεως υβριδοποιούνται με κενά ns και np τροχιακά .
Ο δεσμός πραγματοποιείται με με την αλληλεπίδραση των γεμισμένων τροχιακών του συνδέτη με τα κενά μεταλλικά τροχιακά .
Στα μέταλλα μεταπτώσεως αυτού του τύπου είναι σταθερές με σχηματισμό σύμπλόκων με βάσεις Lewis (R2O, R2S, R3P, R3As, RO-, X-).
Παραδείγματα: [Ag(NH3)2]+ , [ Ni(CN)4]2- , [Fe (CO)5], [Ti(Cl6]2- .

π Δεσμός Επαναφοράς ( Υποκαταστάτες Χ)
Διαφορετικά, τα πλήρη (n-1)d τροχιακά των μεταβατικών μετάλλων με κατάλληλη συμμετρία τείνουν να αλληλοκαλυφθούν με τα διαθέσιμα αντιδεσμικά π τροχιακά που υπάρχουν πρωτίστως σε καρβονυλομάδες, στις βινυλομάδες ή φαινυλοομάδες κ.α.
Εδώ το μέταλλο παραχωρεί ηλεκτρονιακή πυκνότητα για να ενισχύσει την ηλεκτρονιακή πυκνότητα μεταξύ Μετάλλου -Άνθρακα
Πρόκειται για π σύμπλοκα δηλαδή ενώσεις μετάλλων μετάπτωσης που περιέχουν π συνδεδεμένους οργανικούς συνδέτες (ολεφίνες, ακετυλένιο, αλλύλιο, κυκλοπενταδιενύλιο και καρβοράνιο).
Ο δεσμός πραγματοποιείται με την επιστροφή ηλεκτρονίων (που είχαν παραχωρηθεί από τα μεταλλικά τροχιακά στα κατώτερα κενά τροχιακά συνδέτη)
Από τη φύση του δεσμού γειτνιάζουν με παράγωγα καρβονυλίου, κυανίου, και καρβενίου
αν υπάρχουν p συνδέτες στο μόριο
Ο δεσμός που πραγματοποιείται μεταξύ μετάλλου- οργανικού συνδέτη σαν αποτέλεσμα των γεμισμένων τροχιακών του συνδέτη με τα κενά οργανικά τροχιακά (δότης-δέκτης) αλλά και σαν αποτέλεσμα επιστροφής ηλεκτρονίων από μεταλλικά τροχιακά σε κατώτερα κενά τροχιακά συνδέτη.
Το μέταλλο εδώ μπορεί να αλληλεπιδράσει με όλα τα άτομα άνθρακα του pi ηλεκτρονικού συστήματος
[Fe(C5H5)2] 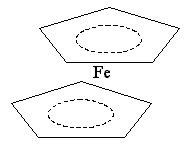
ενώσεις σάντουιτς
καθένα από τα ιόντα κυκλοπενταδιενύλιου παρέχει 3 ζεύγη π ηλεκτρονίων και
οι δέκτες των ζευγών ηλεκτρονίων είναι τα τροχιακά του υβρυδοποιημένου σιδήρου sp3d2-
ή με ορισμένα από αυτά.
Η στοιχειομετρία υπακούει στον κανόνα των 18 ηλεκτρονίων ή καλύτερα στην εξίσωση των εξωτερικών ηλεκτρονίων του με αυτά του πλησιέστερου ευγενούς αερίου
Β. Συνεργιστικός δεσμός
Είναι ο πιο αντιπροσωπευτικός δεσμός στις οργανομεταλλικές ενώσεις στις οποίες ο υποκαταστάτης που διαθέτει μόνο d τροχιακά που μπορούν να συμμετάσχουν σε δεσμό π επαναφοράς, αλλά δρα ταυτόχρονα και σαν δότης ηλεκτρονίων
Οι υποκαταστάτες αυτοί μπορούν
1. να δρουν σαν δότες σε έναν σ δεσμό ή να προσφέρουν ηλεκτρόνια από τα π μοριακά τροχιακά τους σε κενά d μοριακά τροχιακά του μετάλλου
2 να δέχονται ηλεκτρόνια από τα συμπληρωμένα d τροχιακά του μετάλλου στα κενά π* αντιδεσμικά τροχιακά τους τα οποία να επανατοποθετούνται για τον δεσμό π επαναφοράς
Τέτοιοι υποκαταστάτες είναι: το μονοξείδιο του άνθρακα (:CO), το μονοσουλφίδιο του ά νθρακα (:C=S), το ισονιτρίλια (:CN-R), το καρβένια (:CR2) , το κυανίδια :C=-N κ.α.
ΠΟΛΙΚΟΤΗΤΑ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ
Στις οργανομεταλλικές ενώσεις ο δεσμός M-C πολώνεται στην κατεύθυνση του βέλουςως εξής: Μd+-> - Cδ-
Γ.ΙΟΝΤΙΚΟΙ ΔΕΣΜΟΙ ΣΕ ΟΡΓΑΝΟΜΕΤΑΛΛΙΚΕΣ ΕΝΩΣΕΙΣ
Εξαιρετικά ηλεκτροθετικά μέταλλα δίνουν οργανομεταλλικές ιοντικές ενώσεις . Το κατιόν αντιπροσωπεύει το μεταλλικό κέντρο και το ανιόν η οργανική καρβανιδομάδα. Χαρακτηριστικές τέτοιες ενώσεις δίνουν τα αλκάλια και οι αλκαλικές γαίες (εκτός από λίθιο και Μαγνήσιο) . Διαθέτουν ιδιότητες άλατος και είναι συνήθως στερεές ουσίες
Δ. ΗΛΕΚΤΡΟΝΙΑΚΑ ΦΤΩΧΟΙ ΔΕΣΜΟΙ
ΠΟΛΥΚΕΝΤΡΙΚΟΙ ΔΕΣΜΟΙ ΣΕ ΣΥΜΠΛΟΚΟ - ΠΟΛΥΠΥΡΗΝΙΚΑ ΣΥΝΠΛΟΚΑ
Είναι ασθενέσθεροι από τους ομοιπολικούς, όταν ηλεκτρόνια σθένους των μεθυλομάδων δεν επαρκουν για να συμπληρώσουν όλα τα αντιδεσμικά τροχιακά με ζεύγη
Στοιχεία από την 1Α καιIIΑ ομάδας και ΙΙΙΑ ομάδα, όπως το Αργίλιο, Μαγνήσιο, Βηρύλλιο και Λίθιο συναρμολογημένα με μια μεθυλομάδα σχηματίζουν πολυκεντρικούς δεσμούς
Πολυκεντρικοί δεσμοί μπορεί να εμφανιστούν με 2 ή 3 ή 4 κέντρα.
Συνήθως σε περιπτώσεις πολυκεντρικού δεσμού το φορτίο μετατοπίζεται προς την μια κατεύθυνση. Παράδειγμα στο σύμπλοκο [Al(CH3)3]2 (σχήματα) τα μήκη των δεσμών Al-C και Li-C είναι άνισα
Στους πολυκεντρικούς δεσμούς, αναλογα με την φύση συμμετοχής του συνδέτη διακρίνουμε
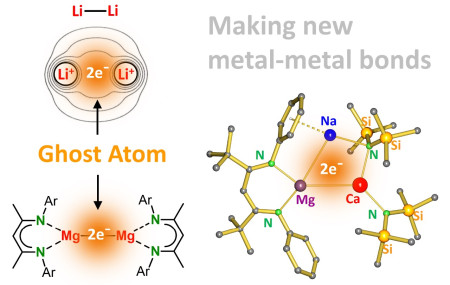
1 ΑΜΕΣΗ ΕΠΙΚΟΙΝΩΝΙΑ. ΔΕΣΜΟΙ ΜΕΤΑΛΛΟΥ- ΜΕΤΑΛΛΟΥ ΣΕ ΣΥΜΠΛΟΚΟ
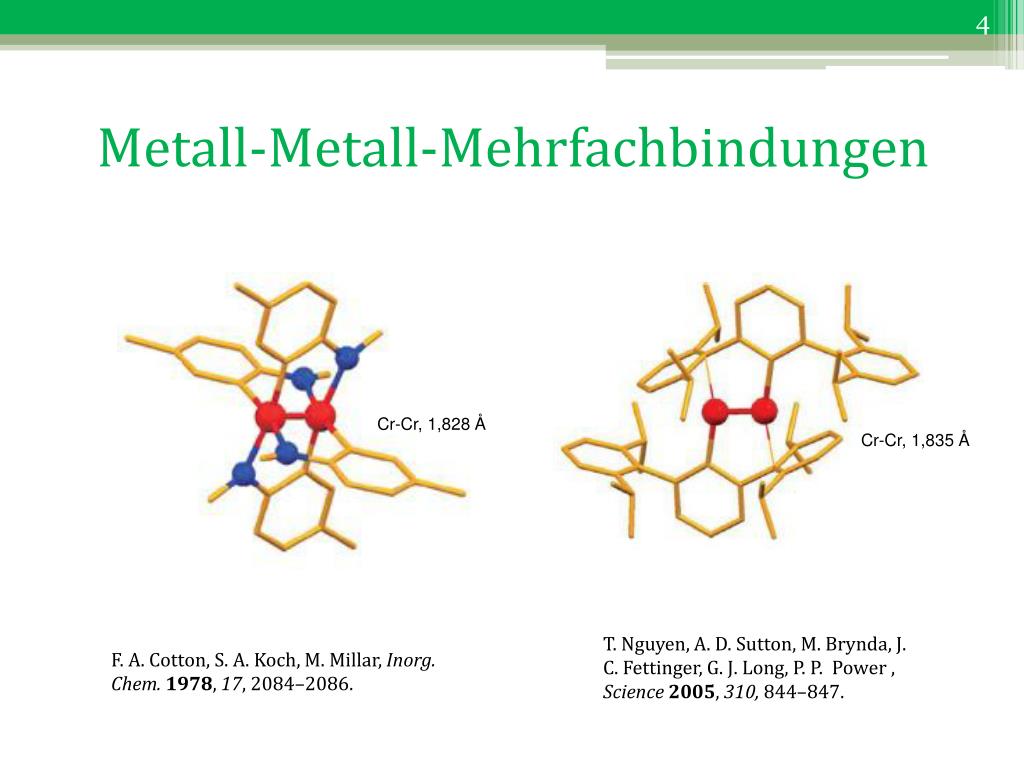 Σε πολυπυρηνικά συμπλέγματα, δημιουργούνται ορισμένες φορές δεσμοί μεταξύ μετάλλου- μετάλλου ως αποτέλεσμα επικάλυψης των δεσμών σθένους τροχιακών γειτονικών ατόμων μετάλλων
Σε πολυπυρηνικά συμπλέγματα, δημιουργούνται ορισμένες φορές δεσμοί μεταξύ μετάλλου- μετάλλου ως αποτέλεσμα επικάλυψης των δεσμών σθένους τροχιακών γειτονικών ατόμων μετάλλων
τροχιακών τύπου d-s ή p γειτονικών ατόμων μετάλλου.
Είναι κυρίως συνέπεια σε κάποιον ειδικό χωροταξικό προσανατολισμό και στενής ενέργειας σε μεταβατικά μέταλλα.
Περιγράφεται ως αλληλεπίδραση των ατομικών τροχιακών των δύο κέντρων των μετάλλωνxy
Συμβαίνει με αλληλεπίδραση ατομικών μεταλλικών τροχιακών προς σχηματισμό μοριακών τροχιακών σ, π και δ που η πλήρωσή τους καθορίζει την πολλαπλότητα του δεσμού. Η πολλαπλότητα του δεσμού Μ-Μ μπορεί να φτάσει από 1 έως 4
σ σύζευξη: Δεσμοί τύπου σ συμβαίνουν όταν υπάρχει αξονική επικάλυψη dz2 τροχιακών
π δεσμοί : όταν επικαλύπτονται dxz και dyz τροχιακά
δ δεσμός: όταν γίνεται επικάλυψη dτροχιακών (πρόκειται για κοντινά άτομα μετάλλου με υψηλή επικάλυψη )
Ο δεσμός Μ-Μ είναι διαφορετικός και εξαρτάται κυρίως από τη συμμετοχή του συνδέτη στηνγέφυρα Μ-Μ. Υπάρχουν δεσμοί Μ-Μ άμεσης επικοινωνίας χωρίς συμμετοχή συνδέτη γέφυρας .
Μοριακές ενώσεις με δεσμούς Μ-Μ συμπεριφέρονται διαφορετικά από κοινλές μεταλλικές ενώσεις και βρίσκουν εφαρμογές στην χημεία των υλικών ή σαν διμεταλλικοί καταλύτες. Η ενέργεια του δεσμού από αρκετές δεκάδες έως εκατοντάδες Kj/mol.
2. Δεσμός γέφυρας σχηματίζεατι μέσω υποκαταστατών που δεσμεύουν μεταλλικά κέντρα δημιουργώντας μια ηλεκτρονική αλληλεπίδραση γέφυρας Ενώσεις με έλλειψη ηλεκτρονίων δημιουργούν γεφυρωμένες διηλεκτρικές πολυκεντρικές συνδέσεις .
Ε. Απεντοπισμένοι δεσμοί Μετάλλων
Η δεύτερη περίπτωση τα τριμερή παρουσιάζουν ενδιαφέρον γιατί τα 3 ατομικά τροχιακά δίνει 3 μοριακά τροχιακά: ένα δεσμικό , ένα αντιδεσμικό κι ένα μη δεσμικό. Τα 2 ηλεκτρόνια τοποθετούνται στο δεσμικό όμως καταλήγει σε ένα δίκτυο δεσμών απεντοπισμένου στα 3 άτομα. π.χ. τα λιθιοαλκύλια4.jpg)
Στο τριμεθυλοαργίλιο οι μεθυλομάδες δεν έχουν μονήρες ζεύγος ηλεκτρονίων και δεν υπάρχει επαρκής αριθμός ηλεκτρονίων για τον σχηματισμό συμβατικών γεφυρών δότη-δέκτη. Ο απεντοπισμός του φορτίου οδηγείπολλές οργανομεταλλικές ενώσεις της κύριας ομάδας σε σχηματισμό τετραέδρων, ή πολυ;edrvn
Ο ΚΑΝΟΝΑΣ ΤΩΝ 18 ΗΛΕΚΤΡΟΝΙΩΝ
Σύμφωνα με αυτόν, η στοιχειομετρία των περισσότερων αυτών συμπλεγμάτων, υπακούει στον κανόνα των 18 ηλεκτρονίων Ο αριθμός των ηλεκτρονίων σθένους σε κάθε μέταλλο συμπλόκου να είναι ίσος με τον αριθμό ηεκτρονίων στο κέλυφος αδρανούς αερίου που βρίσκεται πλησιέστερα στο μέταλλο. Αν τα τροχιακά σθένους που χρησιμοποιούνται κατά τον σχηματισμό δεσμού συνδέτη είναι τα nd, (n+1)s , (n+1)p αυτά πρέπει να είναι γεμάτα με 18 ηλεκτρόνια
Το κέλυφος ατόμου ή ιόντος ενός μετάλλου συμπληρώνεται με τον αριθμό των ηλεκτρονίων που μεταφέρονται από τους συνδέτες.
Συνήθως θεωρείται ότι, τα άτομα αλογόνων, υδρογόνου και οι ομάδες CN, OR, SR κυρίως μεταφέρουν 1 ηλεκτρόνιο. οι ομάδες CO, R3N, R3P από δύο ηλεκτρόνια, το ΝΟ τρία ηλεκτρόνια και εάν συμβεί δεσμός Μετάλλου- μετάλλου από ένα ηλεκτρόνιο στο κάθε ένα.
Κάποια παραδείγματα:
1) Το σύμπλοκο [Cr(CO)6] Aθροίζουμε τα ηλεκτρόνια που μεταφέρονται από τους συνδέτες 6.2 =12 και προσθέτουμε τα ηεκτρόνια του κελύφους που προέρχονται από το χρώμιο και είναι ηλεκτρόνια 3d4 4s2 =6 Σύνολο 18 ηλεκτρόνια .4.svg.png)
2) Το σύμπλοκο [RhCl(H)2 (CO) (PPh)2 ]Το ρόδιο είναι στην d9 με 9 ηλεκτρόνια 4d8 5s1, δανείζει 3 από αυτά στoυς X υποκαταστάτες Cl και Η(2) και μένει RhCl(H)2 (CO) (PPh)2 με 6 ηλεκτρόνια. Υπολογίζουμε τώρα τα ηλεκτρόνια στο κέλυφος στο μέταλλο: 2 από το CO/ 2.2=4 από τα 2 PPh/ 2 (1 +1επιστροφής) στο Cl, 2. 2 (1+1επιστροφή) στο H, και 6 που έχουν απομείνει στο Rh όλα είναι 18
9%20IR%20Spectra.gif)
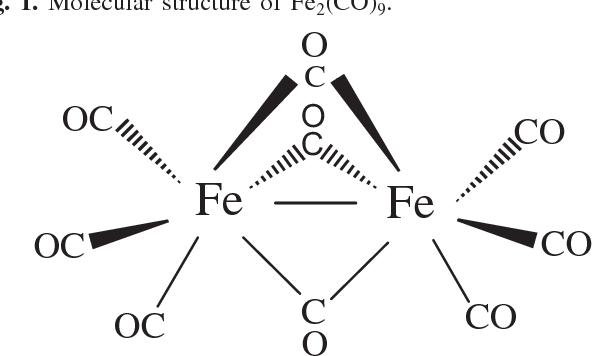 3)Το σύμπλοκο Fe2 (CO)9 .
3)Το σύμπλοκο Fe2 (CO)9 .
.jpg)
ΠΗΓΕΣ
Οργανομεταλλικές ενώσεις - Βικιπαίδεια
https://klouras.chem.upatras.gr/attachments/article/24/09_Phoshines_Alkenes.pdf
05.COMPLEX IONS AND COORDINATION COMPOUNDS (INTRODUCTION)PPP.pdf
Δεσμοί μετάλλου-μετάλλου | Σύνθετες ενώσεις. Σχολικό βιβλίο
Οργανομεταλλικές ενώσεις - Βικιπαίδεια
Molekulare Metall-Metall Bindungen, Geisteratome und Elektronen ...
ακατεργαστο
Οργανομεταλλικές ενώσεις — Χημική Εγκυκλοπαίδεια
file:///C:/Users/user/Downloads/chap02%20(1).pdf
p-συνδέτες στο μόριο (CO, κυκλοπενταδιενύλιο κ.λπ.). 2) Οργανομεταλλικές ενώσεις με ιοντικό δεσμό M-C. Τέτοιες ενώσεις είναι ουσιαστικά μεταλλικές. άλατα καρβανίων. Είναι χαρακτηριστικά της αλκαλικής και αλκαλικής γης. μέταλλα (με εξαίρεση τα Li και Mg), π.χ. Na+(C, 5, H,5)-, K+(C-=CR) κ.λπ. 3) Ενώσεις με έλλειψη ηλεκτρονίων. με γεφυρωμένους πολυκεντρικούς δεσμούς δύο ηλεκτρονίων M—C—M. Αυτά περιλαμβάνουν. Li, Mg, Be, Al. 4) p-Σύμπλοκα ενώσεων. μέταλλα που περιέχουν p-δεσμευμένο org. συνδέτες (αλκένια, αλκύνια, αρωματικές ενώσεις κ.λπ.). Οι οργανομεταλλικές ενώσεις αυτού του τύπου είναι χαρακτηριστικές των μετάλλων μετάπτωσης. Μόνο μερικά παραδείγματα είναι γνωστά για μέταλλα μη μετάπτωσης.
Είναι γνωστές πλήρεις οργανομεταλλικές ενώσεις, στις οποίες ένα άτομο μετάλλου συνδέεται μόνο με άτομα C και μικτές ενώσεις, στις οποίες περιέχουν επίσης δεσμό μετάλλου-ετεροατόμου.
ακατέργαστο
Курс лекций по химии металлоорганических соединений. Часть I.