Δήμητρα Σπανού, συνταξιούχος καθηγήτρια χημικός Β/θμιας Εκπ/σης
σε επεξεργασία
ΤΙ ΕΙΝΑΙ ΦΑΣΗ ΕΝΟΣ ΣΥΣΤΗΜΑΤΟΣ
Φάση είναι το μέρος ενός συστήματος που είναι χημικά ομοιογενές και σταθερό χωρικά και στις φυσικές ιδιότητες .
Διαχωρίζεται από τα άλλα ομογενή συστατικά του συστήματος με οριακές επιφάνειες (όριο διεπαφής)
Φάσεις μπορεί να έχουμε σε συστήματα που αποτελούνται από ένα συατατικό ή σε συστήματα με πολλά συστατικά
Φάσεις δημιουργούνται λόγω φυσικής κατάστασης (στερεά, υγρή και αέρια φάση) αλλά και λόγω αλλοτροπικών μορφών στερεού όπως λευκός μαύρος και κόκκινος φωσφόρος, το διαμάντι, ο γραφίτης ο ξυλάνθρακας κ.α. στον άνθρακα.
Τα υγρά και τα στερεά ονομάζονται συμπυκνωμένες φάσεις
ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΔΙΑΓΡΑΜΜΑΤΑ ΦΑΣΕΩΝ ΣΥΣΤΗΜΑΤΟΣ
Εάν σε συστήματα που συνυπάρχουν φάσεις οι οποίες διαχωρίζονται από διαχωριστική επιφάνεια διαθερμική, κινητή και διαπερατή στην ύλη.
Εάν σε αυτές τις φάσεις (ή κάποια από αυτές) οι εντατικές ιδιότητες (Τ P μi) δεν έχουν τις ίδιες τιμές, τότε, θερμότητα, έργο ή και ύλη¨ "ρεει" μεταξύ τους μέχρι ναεξισωθούν οι Πιέσεις τους, οι θερμοκρασίες τους και τα χημικά δυναμικά τους. Τότε λέμε ότι οι φάσεις είναι σε ισορροπία
Τα .διαγράμματα φάσεων είναι γραφικές παραστάσεις που αναπαραστούν τις περιοχές πίεσης και θερμοκρασίας που οι επιμέρους φάσεις είναι θερμοδυναμικά σταθερές. Οι περιοχές χωρίζονται μεταξύ τους με οριακές γραμμές φάσης που αντιπροσωπεύουν ζεύγη τιμών Πίεσης- θερμοκρασίας που οι φάσεις βρίσκονται σε ισορροπία μεταξύ τους
Εξετάζοντας συστήματα ενός συστατικού μπορούμε να έχουμε φάσεις : Φάσεις μεταξύ στερεάς και υγρής κατάστασης και ακόμη στερεάς και αέριας φάσης
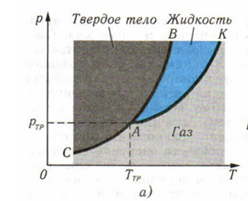
Για ορισμένες τιμές της P-T τρεις φάσεις (συνήθως η στερεα ή υγρή και η αέρια) έχουν ίδιες τιμές. Είναι σημεία που συναντιόνται οριακές γραμμές φάσεων. Αυτό είναι το τριπλό σημείο.

Ακόμα φάσεις μεταξύ υγρού και δύο ή περισσότερων κρυσταλλικών μορφών στερεού (νερό και διαφορετικές κρυσταλλικές μορφές πάγου) ή μεταξύ στερεού και διαφορετικές αλλοτροπικές μορφές του σε ισορροπία με ατμούς (ρομβικό και μονοκλινές θείο και ατμοί θείου)
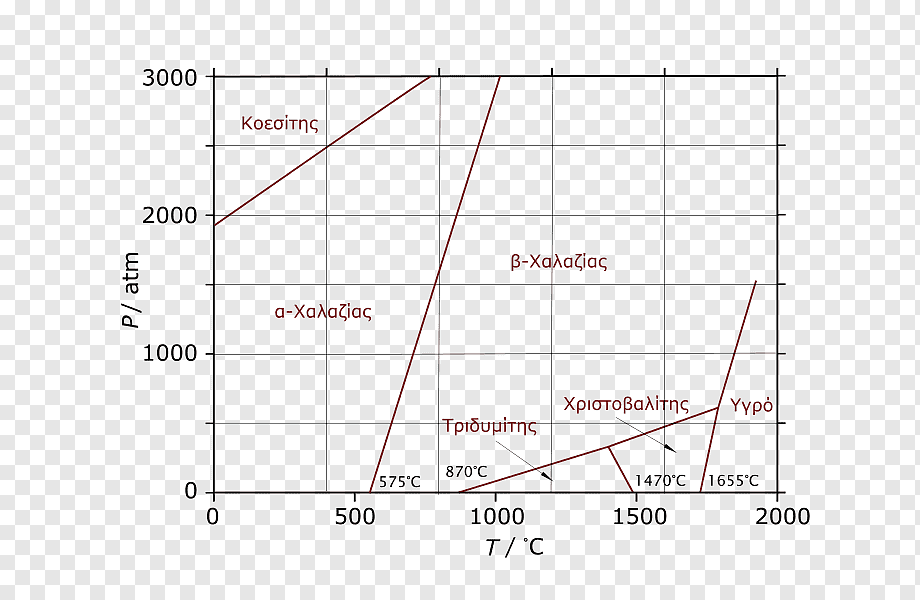
ή στερεο σύστημα ενός συσστατικού από διαφορετικές στερεοισομερείς μορφές του στερεού (ορυκτά του πυριτίου: α χαλαζίας, β χαλαζίας, τριδυμίτης,
Εάν υπάρχει ισορροπία φάσεων ετερογενούς συστήματος σε δεδομένες συνθήκες Πίεσης θερμικρασίας, και έρθει κάποια αλλαγή στις συνθήκες αυτές η αρχική ισορροπία διαταράσσεται
Συνήθως οι καμπύλες φάσεων μας δίνουν τις συνθήκες Πίεσης και θερμοκρασίας που έχουμε ισορροπία των φάεων σε ένα σύστημα, όχι όμως ποσοτηκά μεγέθη
ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΙΣΟΡΡΟΠΙΑ- ΒΑΘΜΟΙ ΕΛΕΥΘΕΡΙΑΣ- Ο KANONAΣ ΤΟΥ GIBBS
Καταλήγουμε λοιπόν στο συμπέρασμα ότι η κατάσταση του συστήματος ελέγχεται από μεταβλητές που εξαρτώνται από το σύστημα
Ο αριθμός των εντατικών παραμέτρων που μπορούν κάθε φορά να μεταβάλλονται ανεξάρτητα λέγεται αριθμός θερμοδυναμικών βαθμών ελευθερίας (f)
Για σύστημα με r συστατικά οι παράμετροι είναι r +2 (2 είναι για την θερμοκρασία και πίεση)
Με την αλλαγή των εξωτερικών συνθηκών πολλές φορές η ισορροπία διαταράσσεται, η συγκέντρωση μεταβάλλεται και πολλές φάσεις ισως εξαφανιστούν και αντικατασταθούν με νέες, έως ότου δημιουργηθεί μια νέα κατάσταση ισορροπίας
Ο αριθμός των φάσεων ανάλογα με τη σύνθεση (συστατικά) και τις εξωτερικές συνθήκες ορίζεται από τον κανόνα φάσης (Νόμος ισορροπίας φάσεων του Gibbs) . Εδώ ορίζεαται ο βαθμός ελευθερίας του θερμοδυναμικού συστήματος που είναι ο αριθμός που δίνει το πλήθος των ανεξάρτητων μεταβλητών που καθορίζουν την εσωτερική ενέργεια του συστήματος
ισχύει: f= r+2-φ
Από εδώ έχουμε: Αν το σύστημα είναι από 1 συστατικό οι βαθμοί ελευθερίας είναι f= r+2-φ άρα f= 1+2-1 -> F =2
Αν όμως έχουμε σύνθετο σύστημα που οι φάσεις του φ είναι σε ισορροπία τότε οι βαθμοί ελευθερίας δίνονται από : F= r+2 -φ
ΒΑΘΜΟΙ ΕΛΕΥΘΕΡΙΑΣ ΓΙΑ ΚΑΘΕ ΣΥΣΤΑΤΙΚΟ ΘΕΡΜΟΔΥΝΑΜΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ
ΕΞΙΣΩΣΗ GIBBS DUHEM
Στις ισορροπίες των φάσεων ισχύει η εξίσωση των P, T, μi. Τότε για κάθε συστατικό ισχύει η εξίσωση
GIBBS- DUHEM
που δείχνει ότι η μεταβολή μιας εντατικής παραμέτρου δεν είναι ανεξάρτητη από τις μεταβολές των άλλων παραμέτρων.
Στην εξίσωση που δίνεται η σχέση μεταξύ τριών εντατικών παραμέτρων μόνο οι δύο από τις τρεις μπορούν να μεταβάλλονται ανεξάρτητα κάθε φορά. Η τρίτη δίνεται από την εξίσωση Π.χ. Για μεταβολή των P, T το μ εξαρτάται από την σχέση τους. Για μεταβολή στο P, μ η Τ είναι εξαρτημένη κ.λ.π. Αυτό άλλωστε εξάγεται και από τον κανόνα του Gibbs ; Οι βαθμοί ελευθερίας είναι 2 για 1 συστατικό(r=1) και μία φάση (φ=1)
f= r+2-φ
f= 1+2-1 =2
ΠΩΣ ΜΕΛΕΤΑΜΕ ΤΗΝ ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ
'Οταν έχουμε φάσεις στο σύστημα, μελετάμε την ισορροπία του με την ενέργεια Gibbs . Να θυμηθούμε ότι
H Ενέργεια Gibbs είναι συνεχές ως συνάρτηση και είναι γνωστή και σαν Χημικό δυναμικό και υπολογίζεται διατηρώντας σταθερή την Θερμοκρασία και την Πίεση και μεταβλητό τον αριθμό των σωματιδίων.
Το Χημικό Δυναμικό ενός είδους είναι η ενέργεια που μπορεί να απορροφηθεί ή να απελευθερωθεί λόγω αλλαγής του αριθμού σωματιδίων δεδομένου είδους.
Το χημικό δυναμικό ενός είδους εκφράζεται ως η μερική παράγωγος της ενέργειας Gibbs προς τον αριθμό σωματιδίων
και ορίζεται ως ο ρυθμός μεταβολής της ελεύθερης ενέργειας G του συστήματος λόγω της αλλαγής στον αριθμό των ατόμων ή μορίων των ειδών
dG = + Vdp -SdT + ΣμιdNi (1) dG = (θG/θT)V,n dT +(θG/θP),T,ndP + Σ(θG/θn)S,V dn (2)
(θG/θn1)S,V,n2, n3...ni. = μ1 χημικό δυναμικό συστατικού 1 που είναι η ενέργεια που μπορεί να απορροφηθεί ή να απελευθερωθεί λόγω αλλαγής του αριθμού των σωματιδίων με σταθερά τα υπόλοιπα . Το ίδιο για n2, n3 ,,,
Σε μια ουσία που βρίσκεται σε ισορροπία το χημικό δυναμικό είναι το ίδιο αν οι φάσεις που υπάρχουν (στερεα, υγρή κ.λ.π.) είναι μεταξύ τους σε ισορροπία
Αν λοιπόν υπάρχει υγρή και στερεά φάση μιας ουσίας σε ισορροπία μεταξύ τους, τότε η χημική ουσία Το δυναμικό εντός της υγρής φάσης ισούται με αυτό στη στερεά φάση.
Με την αλλαγή των εξωτερικών συνθηκών πολλές φορές η ισορροπία διαταράσσεται, η συγκέντρωση μεταβάλλεται και πολλές φάσεις ισως εξαφανιστούν και αντικατασταθούν με νέες, έως ότου δημιουργηθεί μια νέα κατάσταση ισορροπίας
ώστε να επιτευχθεί πάλι ισότητα των χημικών δυναμικών κάθε φάσης
Τα χαμηλότερα χημικά δυναμικά βρίσκονται για τα στερεά, έτσι η στερεά φάση για χαμηλότερες θερμοκρασίες είναι η πιο σταθερή. Όμως ανάλογα με την θερμοκρασία το χημικό δυναμικό άλλης φάσης μπορεί να πάρει τιμή κάτω από την τιμή του χημικού δυναμικού του στερεού. Σε αυτές τις περιπτώσεις γίνεται μετάβαση φάσης
Έτσι η ισορροπία μεταξύ των φάσεων σε ένα θερμοδυναμικό σύστημα βασίζεται στον αριθμό σωματιδίων στην κάθε φάση και στην μετακίνησή τους μεταξύ των φάσεων έως ότου οι ενέργειες Gibbs των φάσεων εξισωθούν το οποίο σημαίνει ότι θα έρθει εξίσωση των χημικών δυναμικών τους
Εστω ότι σε ένα σύστημα δεν επικρατεί ισορροπία και το χημικό δυναμικό είναι διαφορετικό ανά περιοχή. Έστω σε μια περιοχή1 είναι μ και σε άλλη περιοχή 2 είναι μ΄. με μ>μ' ΟΙ περιοχές 1 και 2 μπορεί να βρίσκονται στην ίδια φάση ή σε διαφορετικές φάσεις.
Τότε μεταφέρεται ποσότητα σωματιδίων dn1 από την περιοχή1 στην περιοχή 2
και η ελεύθερη ενέργεια Gibbs (ελεύθερη ενθαλπία) μειώνεται κατά μdn στην περιοχή 1 και αυξάνεται κατά μ΄dN στην περιοχή2 . Η μεταβολή της ενέργειας Gibbs (ελεύθερης ενθαλπίας είναι dG =(μ΄- μ )dn
Αν μετά την διαδικάσία τα νέα χημικά δυναμικά στην περιοχή 1 και περιοχή 2 είναι ίσα μμετά = μ΄μετά το σύστημα έχει φτάσει στη θερμοδυναμική ισορροπία
Σε μια δεδομένη πίεση, η φάση βρίσκεται πάντα εντός συγκεκριμένου εύρους θερμοκρασίας των οποίων το χημικό δυναμικό εκεί είναι χαμηλότερο από οπουδήποτε αλλού
ΔΙΑΤΑΡΑΧΗ ΣΤΗΝ ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ- ΜΕΤΑΒΑΣΕΙΣ ΦΑΣΕΩΝ
Σαν αποτέλεσμα αλλαγών σε εξωτερικές παραμέτρους μια ουσία μπορεί να υποστεί μια μετάβαση φάσης
Η μετάβαση φάσης αποτελεί έναν αυθόρμητος μετασχηματισμός μιας φάσης σε μια άλλη φάση που γίνεται σε δεδομένη πίεση, θερμοκρασία και χημικό δυναμικό.
Οι μεταβάσεις μεταξύ των φάσεων σε συγκεκριμένες συνθήκες πίεσης και θερμοκρασίας μπορεί να είναι σε εξέλιξη πολλά χρόνια πολλές η μετατροπή του άνθρακα σε διαμάντι, όμως μεταβάσεις όπως σε υγρά και σε αέρια γίνονται με μεγάλύτερες ταχύτητες εφόσον και τα μόρια έχουν μεγαλύτερη κινητικότητα.
Συνήθως οι μεταβάσεις φάσεων εκφράζονται με συναρτήσεις που δίνονται με όρους παραγώγων θερμοδυναμικών λειτουργιών
Οι μεταβάσεις φάσεων αναφέρουμε τις:
Μεταβάσεις φάσεων πρώτης τάξης : Εξάτμιση(ή συμπύκνωση), τήξη (ή κρυστάλλωση) , εξάχνωση (ή απόθεση) Αλλαγή στις κρυσταλλικές δομές (πάγος)
Οι μεταβάσεις πρώτου είδους εκφράζονται με συναρτήσεις που δίνονται με όρους πρώτων παραγώγων θερμοδυναμικών λειτουργιών
Μεταβάσεις φάσεων δευτέρης τάξης : από την σιδηρομαγνητική στην παραμαγνητική φάση, από κανονικό μέταλλο σε υπεραγωγό
Μεταβάσεις φάσεων νιοστής τάξης: εκφράζονται με συναρτήσεις που δίνονται με όρους νιοστών παραγώγων θερμοδυναμικών λειτουργιών
Συνήθως, για τη μελέτη της ισορροπίας σε απομονωμένο σύστημα (που αντιστοιχεί πάντα στην μέγιστη Εντροπία) προτιμάται η ενέργεια Helmholtz με σταθερό όγκο και θερμοκρασία που η απόδοσή του σε μια πλήρως αντιστρεπτή μεταβολή και είναι ίση με την εργασία που κάνει το σύστημα σε εξωτερικά σώματα
F (ή A) = U - TS Η ισορροπία στο σύστημα επιτυγχάνεται όταν η ενέργεια Helmholtz ελαχιστοποιείται
Ωστόσο, όταν έχουμε φάσεις στο σύστημα αυτό, μελετάμε την ισορροπία του με την ενέργεια Gibbs
ΜΕΤΑΒΑΣΕΙΣ ΦΑΣΕΩΝ ΠΡΩΤΗΣ ΤΑΞΗΣ (ΠΡΩΤΟΥ ΕΙΔΟΥΣ)
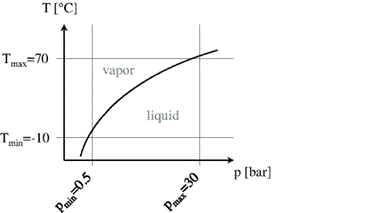
Περιλαμβάνουν την συμπύκνωση, εξάτμιση, τήξη, κρυστάλλωση (πήξη) , αλλαγή στην τροποποίηση των κρυστάλλων. Στα διαγράμματα φάσεων οι γραμμές που διαχωρίζουν τις φάσεις παριστάνουν συναρτήσεις της μορφής P(T) και αποτελούν τις διατεταγμένες (T, Ρ) που οι δύο φασεις βρίσκονται σε ισορροπία.

Οι αναλυτικές μορφές αυτών των συναρτήσεων είναι δύσκολο να προσδιοριστούν,
Για παράδειγμα, η διαδικασία βρασμού εξαρτάται από πολλούς παράγοντες (επιφάνεια υγρού, παραγωγή κίνηση και μέγεθος φυσαλίδων, τοιχώματα δοχείου, εξωτερικές συνθήκες περιβάλλοντος κ.λ.π.) και συνήθως οι καμπύλες αυτές λαμβάνονται πειραματικά.
Παρ' όλα αυτά είναι δυνατή η εύρεσή τους υπό ορισμένες προϋποθέσεις. Είναι δυνατή μια δυναμική ισορροπία δύο φάσεων της ύλης όμως μόνο σε ένα ορισμένο εύρος θερμοκρασιών.

Με την ολοκλήρωση της διαφορικής εξίσωσης P(T) =P΄=dP/dT έχουμε την κλιση της γραμμής ισορροπίας φάσεων.
Η ισορροπία αυτή αντιστοιχεί σε καμπύλη τήξης p=f(T).
Η εστιγμένη γραμμή δίνει την κρυσταλλοποίηση
ΣΧΕΣΕΙΣ ΠΟΥ ΠΕΡΙΓΡΑΦΟΥΝ ΤΙΣ ΓΡΑΜΜΕΣ ΜΕΤΑΒΑΣΗΣ ΣΕ ΙΣΟΡΡΟΠΙΕΣ ΦΑΣΕΩΝ
ΕΞΙΣΩΣΗ GIBBS - DUHEM, ΕΞΙΣΩΣΗ CLAPEYRON, ΕΞΙΣΩΣΗ CLAPEYRON- CLAUSIUS
Στις γραμμές μετάβασης, κάθε σημείο τους έχει ίδιες τις εντατικές ιδιότητες των δύο φάσεων δηλαδή αν η γραμμή αυτή χωρίζει τις φάσεις Α και Β σε κάθε σημείο της έχουμε΅Ρ(Α) +Ρ(Β), Τ(Α) + Τ(Β) και μ(Α)=μ(Β). Σε γειτονικό σημείο της καμπύλης έχουμε μεταβολή της πίεσης καά dP της θερμοκρασίας κατά dT και του χημικού δυναμικού κατά dμ. Οι μεταβολές περιγράφονται με την
εξίσωση Gibbs- Duhem που δείχνει πως συνδέονται οι μεταβολές αυτές. Για κάθε φάση έχουμε:
dμ = -SdT +VdP και διαιρώντας με το n έχουμε dμ = -SmdT +VmdP που διαφοροποιεί την εξίσωση για κάθε φάση με τον δείκτη m . Στην ισορροπία φάσεων ισχύει μ(Α)=μ(Β). Εξισώνοντας τα dμ όπως προκύπτουν από τηνGibbs-Duhem, φτάνουμε στην dP/dT = ΔSm/ΔVm.
( ο δείκτης m μπαίνει όταν n=1 )
Η εξίσωση dP/dT = ΔSm/ΔVm είναι η εξίσωση Clapeyron που δίνει κλίση της καμπύλης του διαγράμματος φάσεων εφόσον υπάρχει διαφορά της γραμμομοριακής εντροπίας ΔSm και του γραμμομοριακού όγκου ΔVm των δύο φάσεων εκατέρωθεν της καμπύλης ισορροπίας.
Εάν θέσω ΔS= ΔΗ/Τ γίνεται dP/dT = ΔΗm/ΤΔVm και έτσι φτάνουμε στην επιθυμητή σχέση P(T) =P΄=dP/dT
ΔΗm ( είναι η θερμότητα που απορροφάται υπό σταθερή πίεση κατά την μετατροπή 1mol της φάσεως 1 στην φάση 2 (λανθάνουσα θερμότητα ανά mol τήξεως / εξαtτμίσεως)
Βρίσκει εφαρμογή σε όλες τις μετατροπές φάσεων (εξαέρωση, εξάχνωση, τ'ηξη, μετατροπή μιας κρυσταλλικής μορφής σε άλλη.
dP/dT = ΔΗεξατμηση /ΤΔVm ή dP/dT = ΔΗεξάτμηση /Τ[Vm(g)-Vm(l) ]
dP/dT = ΔΗεξάχνωσης/ΤΔVm ή νdP/dT = ΔΗεξάχνωσης/Τ[Vm(g)- Vm(s)],
dP/dT = ΔΗτήξης/ΤΔV m ή dP/dT = ΔΗτήξης/Τ[Vm(l) -Vm(s)]
Εάν η μία φάση είναι αέρια δηλαδή σε εξάτμηση και εξάχνωση ,η εξίσωση Clapeyron απλοποιείται ως εξής: Θεωρούμε τον όγκο του αερίου πολύ μεγαλύτερο ώστε ο όγκος του υγρού σε εξάτμηση και του στερεού στη εξάχνωση δεν υπολογίζεται και έτσι έχουμε
dP/dT = ΔΗεξατμηση/ΤVm(g)
dP/dT = ΔΗεξάχνωσης/ΤVm(g)
Σε κάθε περίπτωση γia nn=1το ΔΗm γίνεται ΔΗ εξαερώσεως, ή ΔΗεξαχνώσεως,
Αν υποτεθεί ότι ισχύει η καταστατική εξίσωση των τελείων αερίων γίνεται:
dP/dT = ΔΗεξαέρωσης /ΤVm(g) =dP/dT = PΔΗεξαέρ./RΤ2 =
H εξίσωση
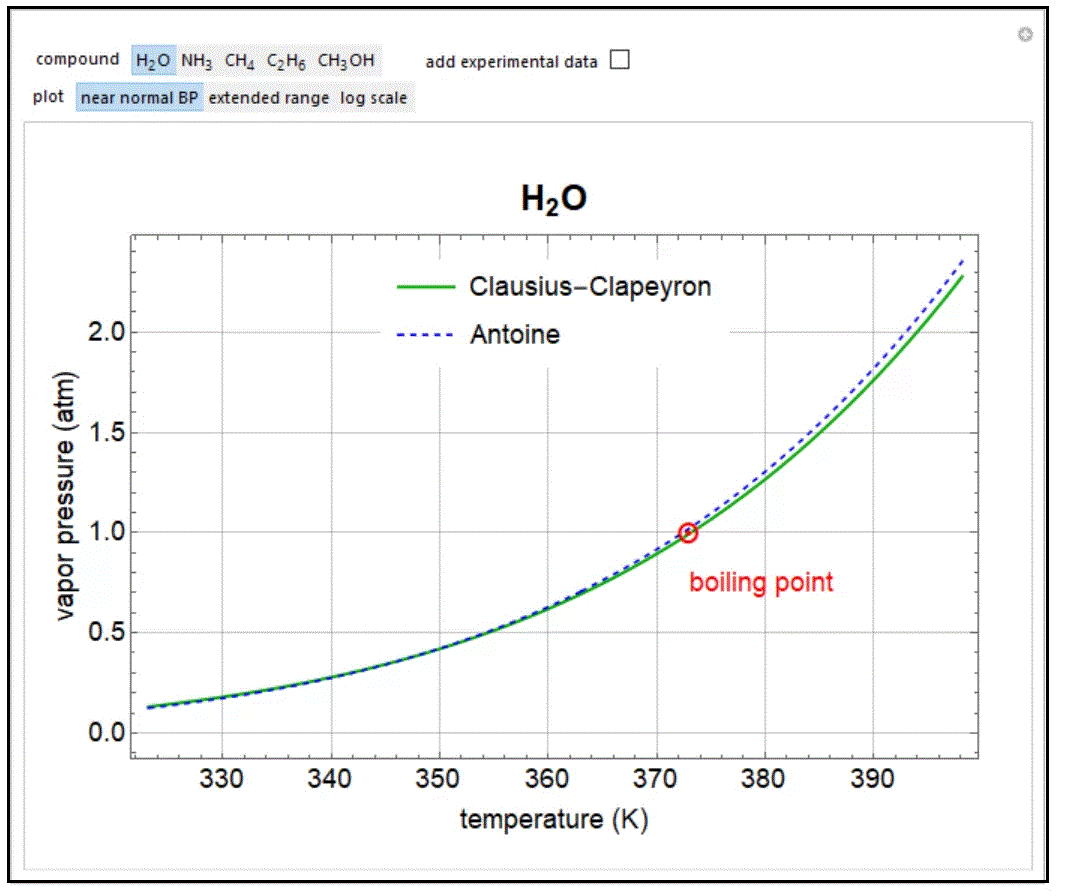
Η ΕΞΙΣΩΣΗ CLAUSIUS CLAPEYRON (dP/ dT = ΔΗεξαερ/ΤΔV .(συνύπαρξης f υγρού- αερίου σε ισορροπια/ στερεού- αερίου σε ισορροπια σε αλλαγές φάσεων 1ου είδους)
Εάν έχουμε μετατροπή σε αέριο (εξάτμιση, εξάχνωση) και για χαμηλές τιμές τάσεως ατμών, η εξίσωση Clapeyron γίνεται η εξίσωση CLAUSIUS CLAPEYRON
Η εξίσωση μπορεί να γραφεί : dP/dT =( ΔΗm/ΔVm ) .1/Τ [dP/dT = Ρ΄ =Ρ΄(Τ)] Η ΔΗm (γραμμομοριακή ενθαλπία θεωρείται σταθερά και για ο λόγος ΔΗm/T είναι η κλίση της εφαπτομένης συνύπαρξης στερεού -υγρού. και είναι ίση με ΔSm (γραμμομοριακή μεταβολή της Εντροπίας )
Έτσι έχουμε από την Clapeyron > dP/dT =ΔΗεξαε/ΤVm(g)=PΔΗεξαε/RΤ2 από ιδανικά αέρια Αν ΔΗ εξαερ =L = σταθ
γίνεται 1/dT (dP/P) = ΔΗεξαε/RT2 . dP/P = L/R ( dT/T2 ). και ολοκληρώνοντας έχουμε dlnP =( -ΔHεξερ./Ρ)1/Τ +l και
P= exp(l)exp[(-Δηεξ/R).1/T]
ΔΗm=qp =L (qp είναι η θερμότητα που απορροφάται υπό σταθερή πίεση κατά την μετατροπή 1mol της φάσεως 1 στην φάση 2 (λανθάνουσα θερμότητα ανά mol τήξεως / εξαtτμίσεως)

Δήμητρα Σπανού
ΠΗΓΕΣ
https://el.wikipedia.org/wiki/%CE%94%CE%B9%CE%AC%CE%B3%CF%81%CE%B1%CE%BC%CE%BC%CE%B1_%CF%86%CE%AC%CF%83%CE%B5%CF%89%CE%BD
CO2-Phase-Diagram.jpg (700×609)
Κεφάλαιο 16. Ισορροπίες Φάσεων σε Πολυσυστατικά Συστήματα | Βιβλίο Lime
Τήξη και κρυστάλλωση. Διάγραμμα ισορροπίας στερεάς, υγρής και αέριας φάσης. Τριπλό σημείο.
https://el.wikipedia.org/wiki/%CE%94%CE%B9%CE%AC%CE%B3%CF%81%CE%B1%CE%BC%CE%BC%CE%B1_%CF%86%CE%AC%CF%83%CE%B5%CF%89%CE%BD
σε επεξεργασία
(∂G/∂T)p = −S ή ![]()
Με διαφόριση γίνεται dG =- SdT +VdP + Σμιdni υπό σταθερή Τ, Π η dG= ι - SdT +VdP + Σμιdni γίνεται dG = Σμιdni
Σε ισορροπίες φάσεων dG=0 Σμιdni =0
ΛΑΝΘΑΝΟΥΣΑ ΘΕΡΜΟΤΗΤΑ ΤΗΞΕΩΣ/ ΕΞΑΤΜΗΣΕΩΣ. ΛΑΝΘΑΝΟΥΣΑ ΘΕΡΜΟΤΗΤΑ ΕΞΑΧΝΩΣΕΩΣ
Αν οι μεταβολές των φάσεων στερεού -υγρού- αερίου, γίνονται υπό συνθήκες αντιστρεπτές, οι καμπύλες των φάσεων δίνονται από τις καμπύλες τήξεως p=f(T) , ζέσεως .
Η καμπύλη ζέσεως είναι συνάρτηση της πυκνότητας ροής της γραμμομοριακής ελεύθερης ενέργειας Gibbs Gm του υγρού προς το αέριο και της αντίστοιχης του αερίου προς το υγρό.
Αντίστοιχα στις καμπύλες τήξεως (Μεταβάσεις πρώτου είδους)
προς την πυκνότητας ροής της γραμμομοριακής ελεύθερης ενέργειας Gibbs Gm του στερεού προς υγρού και αντίστροφα, κατά την τήξη. Επειδή, οι συνθήκες μεταβολών δεν είναι εύκολο να περιγραφούν, για παράδειγμα, η διαδικασία βρασμού εξαρτάται από πολλούς παράγοντες (επιφάνεια υγρού, παραγωγή κίνηση και μέγεθος φυσαλίδων, τοιχώματα δοχείου, εξωτερικές συνθήκες περιβάλλοντος κ.λ.π.) συνήθως οι καμπύλες αυτές λαμβάνονται πειραματικά.
Το ίδιο ισχύει κατά την τήξη στερεού σε υγρό και την καμπύλη τήξεως
Γενικά όμως και εφόσον κατά την ισορροπία φάσεων εξισώνεται η Gm προς τις δύο κατευθύνσεις ΔGm1= ΔGm2 και ΔGm= ΔΗm -TΔSm καταλήγουμε στο ΔSm =ΔΗm/T και ΔΗm=qp =L (qp είναι η θερμότητα που απορροφάται υπό σταθερή πίεση κατά την μετατροπή 1mol της φάσεως 1 στην φάση 2 (λανθάνουσα θερμότητα ανά mol τήξεως / εξαtτμίσεως)
Κατά την εξαέρωση από τη σχέση ΔΗm =ΔUm + PΔVm όπου ο ΔVm περίπου Vm = nRT/P (από νόμο ιδανικών αερίων και ΔS εξ = ΔΗεξ/Τ άρα ΔΗεξ= ΔSεξ.Tb .
Όμως μέσω μετασχηματισμών Legrendre έχπυμε G= U -TS +PV Καταλήγουμε σε G = ΣμιNi
Για ένα απομονωμένο σύστημα η ι2σορροπία μεταξύ των φάσεων είναι κατάσταση δυναμική. Οι ποσότητες από την θερμότητα το έργο ή τα σωματίδια (ύλη) που περνά από την φάση 1 στην φάση 2 είναι ίσος με αυτόν που περνά από την φάση 2 στην φάση 1.

.gif)
