Δήμητρα Σπανού, χημικός, συνταξιούχος καθηγήτρια Β/θμιας Εκπ/σης-από 30-6-2025
ΕΙΣΑΓΩΓΙΚΟ
ΟΙ ΦΑΣΕΙΣ ΕΝΟΣ ΣΥΣΤΗΜΑΤΟΣ 2 ΣΥΣΤΑΤΙΚΩΝ ΣΕ ΙΣΟΡΡΟΠΙΑ
Φάση είναι το μέρος ενός σύνθετου συστήματος που είναι ομογενές κατά την χημική σύσταση και τις φυσικές ιδιότητες και διαχωρίζεται από τα άλλα ομογενή συστατικά του συστήματος με οριακές επιφάνειες
Φάσεις μπορεί να έχουμε σε συστήματα που αποτελούνται από ένα συατατικό ή σε συστήματα με πολλά συστατικά
Η ισορροπία φάσεων σε ένα θερμοδυναμικό σύστημα είναι μια κατάσταση στην οποία οι συνυπάρχουσες φάσεις έχουν μακροσκοπικές παραμέτρους σταθερές στο χρόνο, θερμοκρασία, πίεση, σύνθεση και δεν υπάρχουν μακροσκοπικές ροές ύλης ή ενέργειας μεταξύ των φάσεων
Εαν διαχωρίσουμε τις ουσίες σε διαλύτη και διαλυμένη ουσία διακρίνουμε ισορροπίες
ΙΣΟΡΡΟΠΙΑ ΔΙΑΛΥΜΑΤΟΣ ΚΑΙ ΚΑΘΑΡΟΥ ΣΤΕΡΕΟΥ ΔΙΑΛΥΤΗ, και παίρνουμε την ΚΑΜΠΥΛΗ ΣΗΜΕΙΟΥ ΠΗΞΕΩΣ
ΙΣΟΡΡΟΠΙΑ ΚΟΡΕΣΜΕΝΟΥ ΔΙΑΛΥΜΑΤΟΣ ΚΑΙ ΣΤΕΡΕΑΣ ΔΙΑΛΥΜΕΝΗΣ ΟΥΣΙΑΣ και παίρνουμε την ΚΑΜΠΥΛΗ ΔΙΑΛΥΤΟΤΗΤΑΣ
Εαν δεν διακρίνουμε διαλύτηκαί διαλυμένη ουσία και θεωρήσουμε μόνο την ύπαρξη δύο μη αντιδρώντων ουσιων στο διάλυμα που η μία διαλύεται στην άλλη παίρνουμε το ΔΙΑΓΡΑΜΜΑΤΑ ΦΑΣΕΩΝ ΣΥΣΤΗΜΑΤΟΣ ΔΥΟ ΣΥΣΤΑΤΙΚΩΝ
Για σύστημα 2 συστατικών
Οι βαθμοί ελευθερίας είναι F= r+2 -φ. ή F= 2+2 -φ.
Για 1 φάση (στερεά ή υγρή ήαέρια) οι βαθμοί ελευθερίας είναι 3 (τρισδιάστατο διάγραμμα με Πίεση, Θερμοκρασία και σύσταση της φάσης σε κάθε ένα από τα δύο συστατικά)
Για διάγραμμα ισορροπίας δύο φάσεων (π.χ. στερεα- υγρά) οι βαθμοί ελευθερίας είναι 2
ΣΥΣΤΑΣΗ ΦΑΣΕΩΝ
ΓΡΑΜΜΟΜΟΡΙΑΚΟ ΚΛΑΣΜΑ x, XHMIKO ΔYNAMIKO μ
γραμμομοριακά κλάσματα xi = ni /Σni .
H Ελεύθερη Ενέργεια Gibbs συνδέεται με το χημικό δυναμικό μ με τη σχέση G=nμ για ένα συστατικό ενώ για σύστημα πολλών συστατικών
G= Σ niμι =Σ ni Gi .
μi=Gi λέγεται μερική γραμμομοριακή ελεύθερη ενέργεια Gibbs
ΟΙ ΦΑΣΕΙΣ ΕΝΟΣ ΣΥΣΤΗΜΑΤΟΣ 2 ΣΥΣΤΑΤΙΚΩΝ ΣΕ ΙΣΟΡΡΟΠΙΑ
Φάση είναι το μέρος ενός σύνθετου συστήματος που είναι ομογενές κατά την χημική σύσταση και τις φυσικές ιδιότητες και διαχωρίζεται από τα άλλα ομογενή συστατικά του συστήματος με οριακές επιφάνειες
Φάσεις μπορεί να έχουμε σε συστήματα που αποτελούνται από ένα συατατικό ή σε συστήματα με πολλά συστατικά
Η ισορροπία φάσεων σε ένα θερμοδυναμικό σύστημα είναι μια κατάσταση στην οποία οι συνυπάρχουσες φάσεις έχουν μακροσκοπικές παραμέτρους σταθερές στο χρόνο, θερμοκρασία, πίεση, σύνθεση και δεν υπάρχουν μακροσκοπικές ροές ύλης ή ενέργειας μεταξύ των φάσεων
ΔΙΑΓΡΑΜΜΑΤΑ ΦΑΣΕΩΝ ΣΥΣΤΗΜΑΤΟΣ ΔΥΟ ΣΥΣΤΑΤΙΚΩΝ
Για σύστημα 2 συστατικών ο αριθμός των συντεταγμένων υπερβαίνει τον αριθμό των στοιχείων του συστήματος κατά μια μονάδα. Δηλαδή οι συντεταγμένες που περιγράφουν τις ισορροπίες για δύο συστατικά είναι τρεις (τρισδιάστατο)
Οι βαθμοί ελευθερίας είναι F= r+2 -φ. ή F= 2+2 -φ. Για 1 φάση (στερεά ή υγρή ήαέρια) οι βαθμοί ελευθερίας είναι 3 (τρισδιάστατο διάγραμμα) Για διάγραμμα ισορροπίας δύο φάσεων (π.χ. στερεα- υγρά) οι βαθμοί ελευθερίας είναι 2
Όμως μπορούμε να δώσουμε επίπεδο διάγραμμα εάν κρατάμε κάποια σταθερη παραμέτρο. Εάν κρατάμε την μια παράμετρο σταθερή (π.χ. Διάγραμα Πίεσης -Γραμμομοριακό κλάσμα x1 ή x2 κρατάμε σταθερή την Θρμοκρασία) μπορεί να δοθεί δισδιάστατα
ΣΥΣΤΑΣΗ ΦΑΣΕΩΝ
ΓΡΑΜΜΟΜΟΡΙΑΚΟ ΚΛΑΣΜΑ x, XHMIKO ΔYNAMIKO μ
.Η σύσταση της φάσης στα διάφορα συστατικά που περιέχει, περιγράφεται με διάφορους τρόπους
Κατά την ανάλυση των ισορροπιών των φάσεων, ο συνηθέστερος τρόπος είναι με τα γραμμομοριακά κλάσματα xi = ni /Σni .
2 ΣΥΣΤΑΤΙΚΩΝ ΜΕ ΑΠΕΡΙΟΡΙΣΤΗ ΔΙΑΛΥΤΟΤΗΤΑ ΑΜΟΙΒΑΙΑ
- ΙΣΟΡΡΟΠΙΑΣ ΥΓΡΟΥ -ΣΤΕΡΕΟΥ ΔΙΑΛΥΜΑΤΟΣ (ΜΟΝΟΦΑΣΙΚΟΥ)
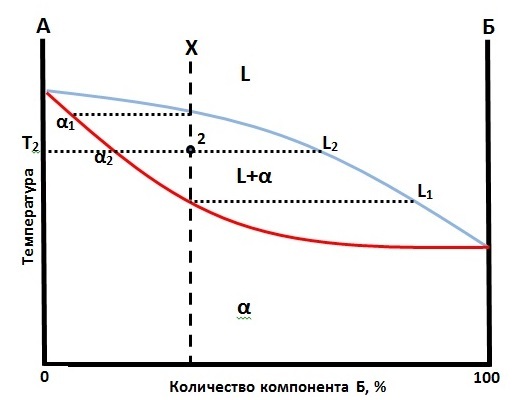
Οι βαθμοί ελευθερίας για την περιοχή του υγρού διαλύματος και για την περιοχή του στερεού διαλύματος σύμφωνα με τον κανόνα των φάσεων είναι F= 2+2 -φ. ή F= 2+2 -1 =3, (θερμοκρασία, Πίεση, σύσταση)
ενώ για την γραμμή ισορροπίας υγρής -στερεάς φάσης είναι F=2. (δύο από τα τρία πάνω)
Το διάλυμα που έχουμε αποτελείται από 2 συστατικά μ ε απεριόριστη διαλυτότητα το ένα στο άλλο καταργούμε τον έναν από τους δύο βαθμούς ελευθερίας
Καταργώντας την ελευθερία στην Πίεση με Πίεση καθορισμένη έχουμε τα εξής::
Σε διάγραμμα Σύστασης % της ουσίας Β( άξονας τετμημένων) -Θερμοκρασίας (άξονας τεταγμένων), υπάρχει περιοχή με Υγρή Α με Β (L) και περιοχή με Στερεό διάλυμα Α και Β φάση (a) και μεταξύ των καμπυλών ο ενδιάμεσος χώρος παριστάνει 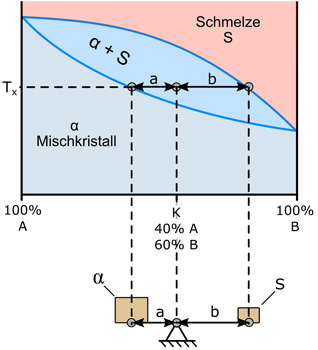 περιοχή που συνυπάρχουν η στερεά (στερεό διάλυμα) και η υγρή φάση των Α και Β.
περιοχή που συνυπάρχουν η στερεά (στερεό διάλυμα) και η υγρή φάση των Α και Β.
Oi γραμμές ισορροπίας φάσεων είναι καμπύλες γιατί η συνάρτηση του σημείου πήξεως με την σύσταση είναι μια μη γραμμική συνάρτηση
Η άνω καμπύλη προσδιορίζει την σύνθεση του τήγματος στο σύστημα ενώ η κάτω είναι η γραμμή του στερεού που δίνει το σημείο ζέσεως σε σχέση με την σύσταση του στερεού διαλύματος για διάφορες περιεκτικότητες σύστασης Α και Β συστατικού. Μεταξύ των καμπυλών ισορροπίας (s-l) βρίσκεται περιοχή στερεού διαλύματος του Α και Β και τήγματος
Μεταξύ των καμπυλών, μπορούμε σε κάθε σημείο καθορισμένης θερμοκρασίας, να βρούμε την σύσταση σε ουσία Α και σε ουσία Β σημείου που βρίσκεται στην περιοχή συνύπαρξης Στερεού -υγρού με τον κανόνα του μοχλού χρησιμοποιόντας τις αποστάσεις του σημείου από τις καμπύλες μετάβασης
- ΚΑΜΠΥΛΕΣ ΨΥΞΕΩΣ : ΚΑΜΠΥΛΗ ΧΡΟΝΟΥ - ΘΕΡΜΟΚΡΑΣΙΑ ΨΥΞΕΩΣ
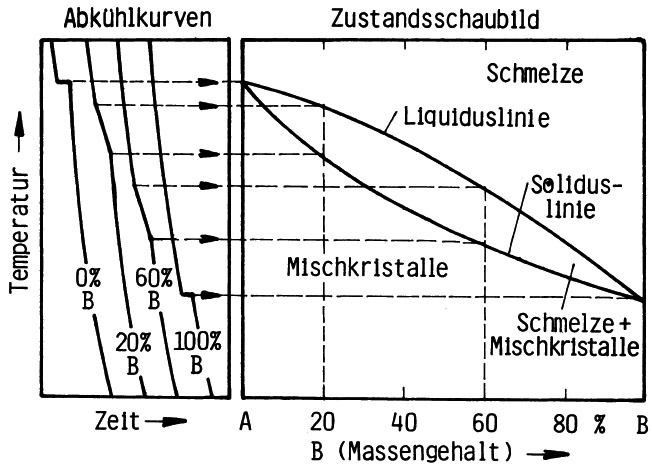 Ακόμα μπορούμε να πάρουμε διαγράμματα ψύξεως του μείγματος ανάλογα με την σύσταση στις 2 ουσίες, στην οποία απελευθερώνεται θερμότητα κατά την μετάβαση από την υγρή στην στερεά φάση. Η πρώτη γραμμή στα αριστερά δίνει την ψύξη ουσίας που αποτελείται μόνο από το Α καθαρό συστατικό μόνο.. Στο σημείο μετάβασης δεν υπάρχει πτώση της θερμοκρασίας γιατί η θερμότητα που απελευθερώνεται χρησιμοποιείτται για στερεοποίηση.
Ακόμα μπορούμε να πάρουμε διαγράμματα ψύξεως του μείγματος ανάλογα με την σύσταση στις 2 ουσίες, στην οποία απελευθερώνεται θερμότητα κατά την μετάβαση από την υγρή στην στερεά φάση. Η πρώτη γραμμή στα αριστερά δίνει την ψύξη ουσίας που αποτελείται μόνο από το Α καθαρό συστατικό μόνο.. Στο σημείο μετάβασης δεν υπάρχει πτώση της θερμοκρασίας γιατί η θερμότητα που απελευθερώνεται χρησιμοποιείτται για στερεοποίηση.
Παρατηρούμε διαορές μεταξύ της πρώτης γεαμμής όπου έχουμε καθαρό συστατικό Α και της τελευταίας που έχουμε καθαρό συστατικό Β, ενώ στο διάγραμμα θερμοκρασία ζέσεως- σύσταση στις περιοχές αυτές οι περιοχή μεταξύ των καμπυλών γίνεται σημειακή και δεν υπάρχει μείγμα στερεού -υγρού. Οι καμπύλες πήξεως επίσης δίνουν μηδενική κλίση (ευθεία) εκεί που το υγρό μετατρέπεται σε στερεό και η θερμότητα .
δεν ελευθερώνεται στο περιβάλλον ούτως ώστε να υπάρχει πτώση θερμοκρασίας αλλά για στερεοποίηση 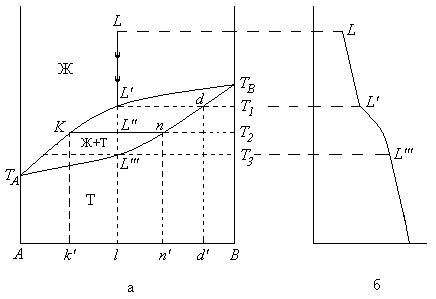
Η δεύτερη και η τρίτη γραμμή δίνουν περιοχές που η κλίση της γραμμής αλλάζει και μάλιστα, η κλίση είναι διαφορετικές. Αντιστοιχούν στις αντίστοιχες περιοχές εντός των καμπυλών διαγράμματος θερμοκρασίας - σύστασης όπου υπάρχει συνύπαρξη υγρής και στερεάς φάσης διαλύματος , γιατί ένα μέρος μόνο από την θερμότητα που ελευθερώνεται χρησιμοποιείται για στερεοποίηση.
Ενώ στο προηγούμενο διάγρααμα η ουσία Α είχε υψηλότερο Σημείο τήξεωα από τη Β εάν δώσουμε αντίστροφα
ΙΣΟΡΡΟΠΙΑΣ ΥΓΡΟΥ -ΣΤΕΡΕΟΥ ΔΙΑΛΥΜΑΤΟΣ 2 ΣΥΣΤΑΤΙΚΩΝ
ΜΕ ΠΕΡΙΣΜΕΝΗ ΔΙΑΛΥΤΟΤΗΤΑ ΤΩΝ ΣΥΣΤΑΤΙΚΩΝ ΣΤΗΝ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ
ΕΥΤΗΚΤΙΚΟ ΜΕΙΓΜΑ
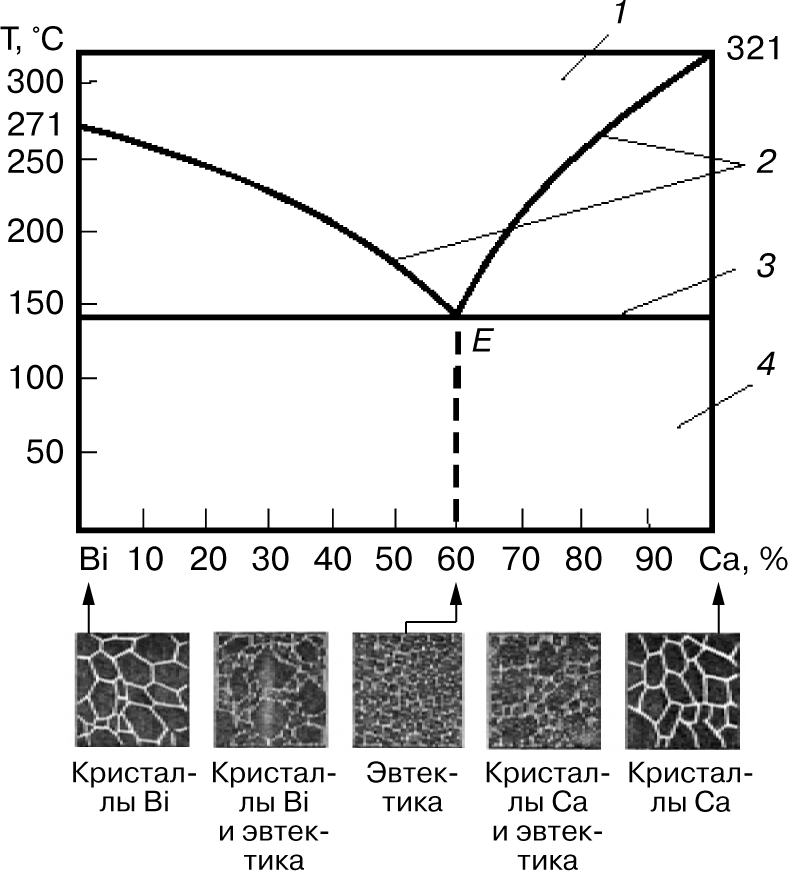
Διαλύματα ισορροπίας φάσεων με περιορισμένη διαλυτότητα των συστατικών το ένα στο άλλο στη στερεά κατάσταση. Τέτοιες ουσίες σχηματίζουν ευτηκτικά μείγματα.
Ένα τέτοιο Καδμίου (ΣΤ 321οC) - Βισμουθίου (ΣT271οC) παρουσιάζεται στο διάγραμμα
φάσεων Σύστασης % της ουσίας Β( άξονας τετμημένων) -Θερμοκρασίας (άξονας τεταγμένων), ξεκινόντας από την αρχή με σύσταση Α 100% και Β 0% αυξάνει σταδιακά η σύσταση του Β και η καμπύλη
Στην κορυφή υπάρχει περιοχή με Υγρό τήγμα Α με Β (L) που οριοθετείται από τη γραμμή που συνδέει τα σημεία τήξεως Βι (271 με το Cd (321) μέσω του σημείου ευτηκτικού μείγματος Ε, για διάφορες περιεκτικότητες του μείγματος σε Βι και Cd Cd
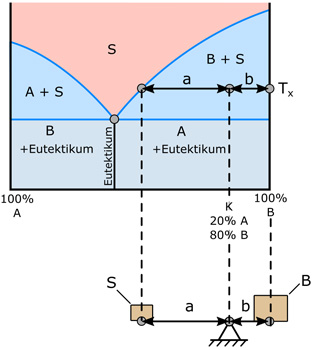 Μπορούμε να βρούμε την σύσταση σε ουσία Α και σε ουσία Β σημείου που βρίσκεται στην περιοχή συνύπαρξης Στερεού -υγρού επίσης με τον κανόνα του μοχλού χρησιμοποιόντας τις αποστάσεις του σημείου από τις καμπύλες μετάβασης
Μπορούμε να βρούμε την σύσταση σε ουσία Α και σε ουσία Β σημείου που βρίσκεται στην περιοχή συνύπαρξης Στερεού -υγρού επίσης με τον κανόνα του μοχλού χρησιμοποιόντας τις αποστάσεις του σημείου από τις καμπύλες μετάβασης
Στο ευτηκτικό σημείο Ε με 60% Βι και 40% η καμπύλη ισορροπίας διέρχεται από κατώτατο σημείο και είναι στο σημείο έχουμε την χαμηλότερο σημείο τήξεως του στερεού διαλύματος.
Η ευθεία γραμμή που περνά από το Ε οριοθετεί την στερεά φάση που είναι κάτω, σε χαμηλότερες θερμοκρασίες με σύσταση ανάλογη των 2 ουσιών. Στο διάγραμμα Bi- Cd αποτελείται από ένα μωσαϊκό από διαφορετικές μορφές κρυστάλλωσης .
Σε άλλες περιπτώσεις η στερεά φάση μπορεί να αποτελείται από διαφορετικές περιοχές που να περιέχουν ευτηκτικό μίγμα μαζύ με καθαρούς κρυστάλλους του ενός ή του άλλου συστατικού
σχηματισμός μικτών κρυστάλλων
Μια άλλη περίπτωση σχηματισμού ευτηκτικού μείγματος ( με περιορισμένη διαλυτότητα στη στερεή κατάσταση), έχουμε όταν στην
στερεά φάση υπάρχουν μικτοί κρύσταλλοι διαφορετικών τύπων μαζί με στερεοποιημένο ευτηκτικό τήγμα και ταυτόχρονα περιοχές με Α και Β συστατικά μεγάλης καθαρότητας.
περιοχές καθαρών συστατικών
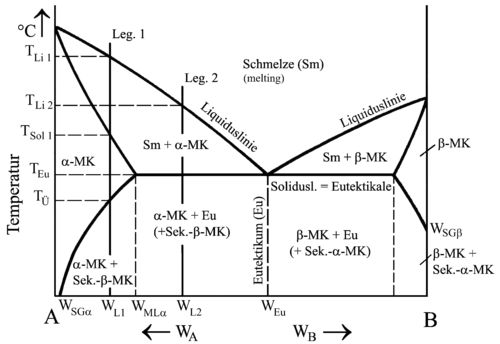
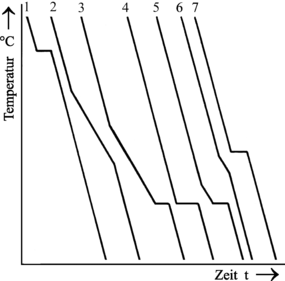
Επεξήγηση: Δεδομένου ότι, η περιορισμένη διαλυτότητα στη στερεή κατάσταση σημαίνει κατ αρχή ότι ένα συστατικό του μείγματος μπορεί να απορροφήσει έως ένα ποσοσστό ατόμων από το άλο συστατικό κατά την κρυστάλλωση και επίσης η διαλυτότητα μειώνεται με την πτώση της θερμοκρασίας γιατί τα κρυσταλλικά πλέγματα συρρικνώνονται και έτσι προσφέρεται λιγότερος χώρος για ξένα άτομα. Η μείωση της διαλυτότητας σε χαμηότερες θερμοκρασίες οδηγεί σε διαχωρισμό μικτών κρυστάλλων και ακόμη μερικό διαχωρισμό των συστατικών στο στερεό μίγμα λόγω μείωσης της διαλυτότητας σε χαμηλότερες θερμοκρασίες (σχήμα αριστερα) και η ανάλυση ψύξεως δίνει διαφορετικά αποτελέσματα για περιοχές διαφορετικής σύστασης. Η πρώτη και η τελευταία γραμμη παριστούν την ψύξη της αριστερής περιοχής (καθαρό συστατικό Α) και δεξιάς (καθαρό Β). Η τέταρτη και πέμπτη γραμμή (παρόμοιες με 1η και τεευταία) δίνουν περιοχές με μεγάλη περιεκτικότητα σε ευτηκτικό μείγμα
Σχηματισμός χημικήε ένωσης
.png) Μια άλη περίπτωση ουσιών σε μείγμα που αναμιγνύονται πλήρως είναι όταν τα συτατικά μπορούν να σχηματίσουν μεταξύ τους σταθερές χημικές ενώσεις Τότε προκύπτει ένας συνδυασμός διαγραμμάτων των συτατικών δεδομένου ότι ο αριθμός τους έχει αυξηθεί κατά το πλήθος των χημικών ενώσεων που έχουν σχηματιστεί.
Μια άλη περίπτωση ουσιών σε μείγμα που αναμιγνύονται πλήρως είναι όταν τα συτατικά μπορούν να σχηματίσουν μεταξύ τους σταθερές χημικές ενώσεις Τότε προκύπτει ένας συνδυασμός διαγραμμάτων των συτατικών δεδομένου ότι ο αριθμός τους έχει αυξηθεί κατά το πλήθος των χημικών ενώσεων που έχουν σχηματιστεί.
 Στο διάγραμμα αριστερά τα αρχικά 2 συστατικά Α και Β σχηματίζουν χημική ένωση S.
Στο διάγραμμα αριστερά τα αρχικά 2 συστατικά Α και Β σχηματίζουν χημική ένωση S.
Ta 2 διαγράμματα που τοποθετούνται δίπλα-δίπλα είναι των συστατικών Α-S και B-S.
Στα σημεία ΤΑ, S, TB το σύστημα είναι μη μεταβλητό
Στα Ε1 και Ε2 έχουμε τα 2 ευτηκτικά σημεία για το πρώτο και το δεύτερο σύστημα. Αν σχηματίζονται 2 χημικές ενώσεις τα διαγράμματα γίνονται πολυπλοκότερα (σχήμα δεξιά)
Διάγραμμα κατάστασης με πολλές φάσεις
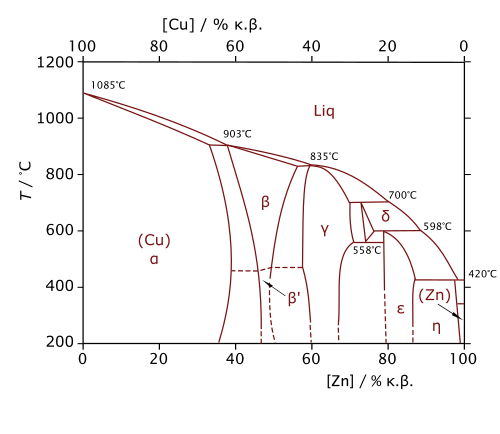
Ορείχαλκoς Cu-Zn)
Εμφανίζονται πολλές φάσεις στο διάγραμμα:
α : στερεό διάλυμα ψευδαργύρου σε χαλκό 'evw 35% ,
β. διατεταγμένο στερεό διάλυμα που περιέχει χημική ένωση CuZn, a+b φάση . Ζn 32-39%
Σε υψηλές θερμοκρασίες πλαστική, σε χαμηλότερες τακτική.
Η φάση γ είναι μια ηλεκτρονική ένωη Cu5Zn8
ΙΣΟΡΡΟΠΙΑΣ ΥΓΡΟΥ -ΣΤΕΡΕΟΥ ΔΙΑΛΥΜΑΤΟΣ 2 ΣΥΣΤΑΤΙΚΩΝ
ΜΕ ΠΛΗΡΗ ΑΔΙΑΛΥΤΟΤΗΤΑ ΤΩΝ ΣΥΣΤΑΤΙΚΩΝ ΣΤΗΝ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ
ΕΥΤΗΚΤΙΚΟ ΜΕΙΓΜΑ 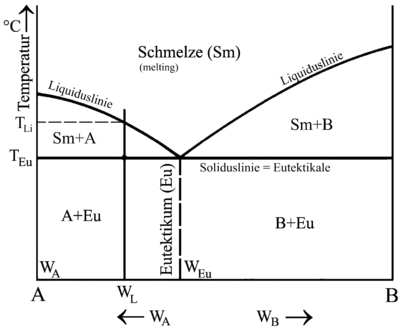
Είναι υλικά που διαόονται μεταξύ τους στην υγρή φάση αλλά διαχωρίζονται εντελώς στην στερεά φάση με κρυστάλλωση. Παρόλο που η στερεοποίηση του μίγματος γίνεται αρχικά σε μια περιοχή, οι κρύσταλλοι του κάθε συστατικού σχηματίζονται χωριστά. Στο ευτηκτικό σημείο οι κρύσταλλοι των δύο συστατικών σχηματίζονται ταυτόχρονα στο σημείο στερεοποίησης (για μεταλλικά μείγματα λέγεται ευτηκτικό κράμα) και διαχωρίζονται μετά λόγω των ιδιαίτερων χαρακτηριστικών τους
.jpg)
Δήμητρα Σπανού
ΠΗΓΕΣ
Παραδείγματα διαγραμμάτων ισορροπίας φάσεων
zweistoffdiagramm-e-02.jpg (500×261)
Βασικές αρχές της θεωρίας κραμάτων
Zustandsdiagramme verstehen und lesen
s://studfile.net/preview/5862380/page:11/
ΑΠΟΧΩΡΙΣΜΟΣ ΟΥΣΙΩΝ ΑΠΟ ΔΙΑΛΥΜΑΤΟΣ 2 ΣΥΣΤΑΤΙΚΩΝ ΣΤΗΝ ΣΤΕΡΕΑ ΦΑΣΗ.
ΔΙΑΓΡΑΜΜΑΤΑ ΠΗΞΕΩΣ - ΣΥΣΤΑΣΕΩΣ
Κατ' αρχήν, στη μελέτη ισορροπίας υγρής και στερεάς φάσης παραβλέπουμε την αέρια φάση λόγω της αμελητέας επίδρασης της πίεσης σε υγρά και στερεά σε σχέση με τα αέρια.
Ο αριθμός των βαθμών ελευθερίας σε μείγμα 2 συστατικών είναι F= 2+2 -φ. Εάν φ=1 για σημεια εκτός καμπυλών f=3
Στην περίπτωση που τα 2 συστατικά του μείγματος Α και Β δεν σχηματίζουν χημική ένωση σε διάγραμμα πήξεως συστάσεως θα διακρίνουμε τις εξής φάσεις :
α. Κορεσμένο διάλυμα του Α σε Β,
. β. κορεσμένο διάλυμα του Β σε Α,
γ. στερεό Α+ κορεσμένο διάλυμα του Α σε Β, δ. στερεό Α+ κορεσμένο διάλυμα του Α σε Β, ε. στερεό Α + ευτηκτικό μείγμα στ.

