Δήμητρα Σπανού, συνταξιούχος καθηγήτρια χημικός Β/θμιας Εκπ/σης-
σε επεξεργασία
ΘΕΡΜΟΔΥΝΑΜΙΚΗ- ΕΙΣΑΓΩΓΙΚΟ
Θερμοδυναμική είναι η μελέτη μετατροπής της ενέργειας από μηχανική ενέργεια- εργο σε θερμότητα και αντίστροφα μέσα από μελέτη θερμοδυναμικών διεργασιών που είναι οι μεταβάσεις από την μια κατάσταση ενός συστήματος σε άλλη.
Η Κλασσική Θερμοδυναμική που διατυπώθηκαν χωρίς την βοήθεια θεωριών περί δομής της ύλης όπως η Μοριακή Θεωρία, βασίζεται σε νόμους και αξιώματα εκ των οποίων τα δύο σημαντικότερα είναι:
Το πρώτο θερμοδυναμικό αξίωμα ή Πρώτος νόμος της θερμοδυναμικής αναφέρει στην διατήρηση της ενέργειας
Το δεύτερο θερμοδυναμικό αξίωμα ή Δεύτερος νόμος της Θερμοδυναμικής αναφέρει την κατεύθυνση μεταφοράς της θερμότητας και την εισαγωγή της έννοιας της εντροπίας.Η εφαρμογή αυτού του 2ου νόμου διευρύνει τους ορίζοντες της θερμοδυναμικής πέραν των θερμικών μηχανών σε άλλα πεδία, όπως η απόδοση των χημικών αντιδράσεων (Χημική Θερμοδυναμική), η μέγιστη τάσης μιας ηλεκτρικής στήλης, η μεταβολή τάσεως ατμών υγρού με την θερμοκρασία κ.α.
Η Θερμοδυναμική όπως και άλλες επιστήμες εξελίσσεταικαι από τις αφηρημένες έννοιες προχωρεί σε ειδικά συμπεράσματα που αποδεικνύονται πειραματικά.
Τα φαινόμενα της θερμοδυναμικής περιγράφονται με τις θερμοδυναμικές μακροσκοπικές παραμέτρους οι οποίες χωρίζονται σε εκτατικές και εντατικές
Τα ποικίλα είδη των μεταβολών (σε όγκο, θερμοκρασία, ύληκ.α.)
Δεδομένου ότι μεγέθη που περιγράφουν μια κατάσταση τα ονομάζουμε καταστατικά, πολλές από τις μεταβολές αυτές εμφανίζονται απλά σαν διαφορικά των καταστατικών συναρτήσεων και στην εξέλιξή της εισάγει ευρέως την χρήση του διαφορικού λογισμού.
Η ανάπτυξη της θεωρίας που είχε ξεκινήσει από τα διάφορα είδη μεταβολών όπως ο θερμοδυναμικός κύκλος του CARNOT προχωρά προς τις καταστατικές συναρτήσεις που τις θεωρεί σαν βασικές έννοιες όπως η ενέργεια, η εντροπία κ.α.
Τέλος να σημειώσουμε ότι η κλασσική Θερμοδυναμική εξετάζει τις ιδιότητες των συστημάτων σε κατάσταση ισορροπίας.
Τελευταία όμως έχει επεκταθεί έξω από τις περιοχές ισορροπίας.
ΜΕ ΤΗΝ ΧΡΗΣΗ ΤΩΝ ΜΑΘΗΜΑΤΙΚΩΝ
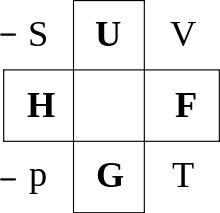
ΑΠΟ ΤΑ ΔΙΑΦΟΡΙΚΑ ΕΝΕΡΓΕΙΑΚΩΝ ΕΚΤΑΤΙΚΩΝ ΠΑΡΑΜΕΤΡΩΝ (U, F, G) ΠΡΟΚΥΠΤΟΥΝ ΣΑΝ ΘΕΡΜΔΥΝΑΜΙΚΑ ΠΑΡΑΓΩΓΑ
ΕΝΤΑΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ (ΘΕΡΜΟΚΡΑΣΙΑ, ΠΙΕΣΗ, ΧΗΜΙΚΟ ΔΥΝΑΜΙΚΟ)
Τα φαινόμενα της θερμοδυναμικής περιγράφονται με τις θερμοδυναμικές μακροσκοπικές παραμέτρους οι οποίες χωρίζονται σε εκτατικές και εντατικές
Για να γίνει αυτό θα πρέπει να χρησιμοποιηθούν καθορισμένες μαθηματικές έννοιες και σχέσεις
Συνάρτηση στα μαθηματικά ορίζεται σαν μια αντιστοίχιση κάθε στοιχείου ενός συνόλου Α (πεδίο ορισμού) σε ένα σύνολο Β (πεδίο τιμών). Αποτελεί θεμελιώδη έννοια στα μαθηματικά σαν εργαλίο επίλυσης προβλημάτων στα μαθηματικά αλλά και στην Φυσική και σήμερα σε πολλές άλλες Επιστήμες
 Διαφορική συνάρτηση: Συνάρτηση που μπορεί να παραχθεί, δηλαδή σε ένα ή περισσότερα σημεία υπάρχει η παράγωγός της δηλαδή περιγράφεται ο ρυθμός μεταβολής της κοντά στο σημείο
Διαφορική συνάρτηση: Συνάρτηση που μπορεί να παραχθεί, δηλαδή σε ένα ή περισσότερα σημεία υπάρχει η παράγωγός της δηλαδή περιγράφεται ο ρυθμός μεταβολής της κοντά στο σημείο
Γεωμετρικά αντιστοιχεί στην κλίση της εφαπτωμένης της γραφικής παράστασης στο σημείο αυτό.
Παραγώγιση ή διαφοροποίηση, ονομάζεται η διαδικασία εύρεσης της παραγώγου μιας συνάρτησης
πιο συγκεκριμένα στην περίπτωσή μας, οι ορισμοί:
Διαφορικές συναρτήσεις: Συναρτήσεις των οποίων υπάρχει παράγωγος που περιγράφει τον ρυθμό μεταβολής τους, σε κάθε σημείο τους . Αποτελούν θεμελιώδη έννοια του διαφορικού λογισμού,
Διαφορική εξίσωση, είναι μια εξίσωση που εκτός από μια συνάστηση συσχετίζει και τις παραγώγους της. Παράγωγοι, συναρτήσεις ανεξάρτητες μεταβλητές και παράμετροι μπορούν να συμπεριληφθούν στην εξίσωση (οπωσδήποτε μια παράγωγος)
Σε αντίθεση με τις αλγεβρικές εξισώσεις που αναζητούν έναν αριθμό, οι διαφορικές εξισώσεις αναζητούν μια συνάρτηση
Υπάρχουν πολλά είδη διαφορικών συναρτήσεων με διαφορετικούς ορισμούς εφαρμογές και χαρακτηριστικά: σταθερή, γραμμικη, τετραγωνική, εκθετική, τριγωνομετρική, λογαριθμική, πολυονυμική κ.λ.π.αποκλείονται οι τιμές των μεταβλητών που μηδενίζουν τον παρονομαστή
Σημειώνουμε τις ρητές και οι ριζικές συναρτήσεις στις οποίες αποκλείονται τιορισμένες τιμές καθώς και τις τμηματικές συναρτήσεις στις οποίες η τιμή και η συμπεριφορά τους διαφοροποιείται σε ορισμένα διαστήματα τιμών στο πεδίο ορισμού τους.
Αν μια διαφορική εξίσωση είναι πολυώνυμο ο βαθμός αυτού του πολυωνύμου ονομάζεται βαθμός της διαφορικής εξίσωσης
(Βαθμός συνάρτησης σε πολυονυμική συνάρτηση: Ο μεγαλύτερος εκθέτης της πολυονυμικής εξίσωσης που καθορίζει τον μέγιστο αριθμό λύσεων)
Διαφορική εξίσωση
Η παραγώγιση του x υψωμένου σε ν δύναμη
| ( xν ) ʹ = νx ν−1 |
Διαφόριση συναρτήεως πολλών μεταβλητών f(x,y,z, ) (με πεδίο ορισμού την τομή των των πεδίων ορισμού κάθε μιας από τις μεταβλητές αυτές): Εδώ για να διαφοροποιήσουμε πρέπει να ορίσουμε και να βρούμε την μερική παράγωγο της συνάρτησης f για κάθε μια από τις μεταβλητές διατηρώντας σταθερές τις άλλες μεταβλητές.
Με την προυπόθηση ότι εδώ έχουμε για συνάρτηση πολλών μεταβλητών, το ολικό διαφορικό που αναπτύσσεται με προσφορές των μερικών διαφορικών, προσδιορίζονται από τις μερικές διαφορικές παραμέτρους που παράγονται ενώ οι υπόλοιπες μεταβλητές παραμένουν σταθερές
Παράδειγμα:
Το τέλειο διαφορικό συνάρτησης πολλών μεταβλητών
Έστω συνάρτηση F= F(x, y, z) και το διαφορικό της (τέλειο) πυ είναι dF= (θf/θx)y,z dx + (θf/θy)x,z dy + (θf/θz)y,x dz
Ta (θf/θx)y,z dx (θf/θy)x,z dy (θf/θz)y,x dz Eίναι οι μερικές παράγωγοι της F ως προς x (y, z σταθερά) ως προς y (x. z σταθερά) και ως προς z x, y σταθερά)
ΠΩΣ ΑΠΟ ΤΙΣ ΕΚΤΑΤΙΚΕΣ ΘΕΡΜΟΔΥΝΑΜΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΠΡΟΚΥΠΤΟΥΝ
ΟΙ ΕΝΤΑΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΘΕΡΜΟΔΥΝΑΜΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ
Οι Εκτατικές ιδιότητες είναι παράμετροι του συστήματος των οποίων η τιμή εξαρτάται από το μέγεθος του συστήματος ( Εσωτερική Ενέργεια, Ενθαλπία ενέργεια Gibbs)
Οι Εντατικές ιδιότητες αντίθετα είναι θεμελιώδη θερμοδυναμικά μεγέθη ποου η ποσότητά τους δεν εξαρτάται από την ποσότητα ύλης ή τον όγκο ή την εσωτερική ενέργεια του συστήματος και δεν αλλάζουν αν αλλάξει η τιμή αυτών
Ο Βαθμός των διαφορικών συναρτήσεων (οι εντατικές)
που προκύπτουν σαν διαφορικά των εκτατικών θερμοδυναμικών συναρτήσεων
Ισχύει ότι: Κάθε εκτατική θερμοδυναμική ιδιότητα παρουσιάζεται σαν ομογενής συνάρτηση 1ου βαθμού
Η παραγώγιση του x υψωμένου σε ν δύναμη είναι το x υψωμένο στην ν-1 δύναμη επί το ν
| ( xν ) ʹ = νx ν−1 |
επομένως,
Οι πρώτες παράγωγοι των εκτατικών ιδιοτήτων είναι ομογενείς συναρτήσεις μηδενικού βαθμού
αν έχω (f(x)= xn -> f(x)΄=x(n-1) +c Για συναρτήσεις f 1ου βαθμού n=1 άρα ο βαθμός της f΄είναι 1-1=0.
Άρα οι τιμές τους δεν εξαρτώνται από το μέγεθος του συστήματος. Αυτό σημαίνει πως :
Οι θερμοδυναμικές ιδιότητες που προκύπτουν από τις πρώτες παραγώγους των συναρτήσεων των εκτατικών ιδιοτήτων (U, G, V, n ..) είναι εντατικές θερμοδυναμικές :
Διαφόριση συναρτήσεων πολλών μεταβλητών:
Για να διαφορίσουμε μια συνάρτηση πολλών μεταβλητών με πεδίο ορισμού την τομή (κοινό σύνολο) των πεδίων ορισμού κάθε μιας από τις μεταβλητές , πρέπει αρχικά να βρούμε τις μερικές παραγώγους της συνάρτησης ως προς κάθε μιας από τις μεταβλητές αυτές που συμβολίζουμε
Οι εντατικές συναρτήσεις που προκύπτουν από τη μερική διαφοροποίηση των εκτατικών θερμοδυναμικών συναρτήσεων πολλών μεταβλητών
Το διαφορικό μιας τέτοιας θερμοδυναμικής εκτατικής συνάρτησης είναι τέλειο ή πλήρες διαφορικό. Με την προυπόθηση ότι εδώ έχουμε για συνάρτηση πολλών μεταβλητών, Το διαφορικό αναπτύσσεται με συνεισφορές που προσδιορίζονται από τις μερικές διαφορικές παραμέτρους εκάστου παράγοντα ενώ οι υπόλοιποι παραμένουν σταθεροί.
Παράδειγμα:
Ένα διαφορικό είναι ένα γραμμικό μέρος της αύξησης μιας συνάρτησης Συνήθως γράφεται df (το διαφορικό είναι ο τελεστής)
Μια παραγωγική συνάρτηση (παράγωγος συνάρτησης) είναι μια ένοια του διαφορικού λογισμού που χαρακτηρίζει τον ρυθμό μεταβολής μιας συνάρτησης σε ένα δεδομένο σημείο
Η διαδικασία υπολογισμού μιας παραγώγου λέγεται παραγοτοποίηση
ΕΝΤΑΤΙΚΕΣ ΠΑΡΑΜΕΤΡΟΙ ΘΕΡΜΟΔΥΝΑΜΙΚΑ ΠΑΡΑΓΩΓΑ,
ΠΟΥ ΠΡΟΚΥΠΤΟΥΝ ΣΑΝ ΘΕΡΜΟΔΥΝΑΜΙΚΑ ΠΑΡΑΓΩΓΑ
ΕΝΕΡΓΕΙΑΚΩΝ ΕΚΤΑΤΙΚΩΝ ΣΥΝΑΡΤΗΣΕΩΝ (U, Η, F ή Α, G)
ΑΠΟ ΤΗΝ ΕΣΩΤΕΡΙΚΗ ΕΝΕΡΓΕΙΑ (U)
ΕΝΤΑΤΙΚΕΣ ΠΑΡΑΜΕΤΡΟΙ ΠΟΥ ΠΡΟΚΥΠΤΟΥΝ ΕΙΝΑΙ;
Η ΘΕΡΜΟΚΡΑΣΙΑ(,V, n σταθ) ΠΙΕΣΗ (Τ,n σταθ), ΧΗΜΙΚΟ ΔΥΝΑΜΙΚΟ (V,T σταθ)
ΣΤΑΘΕΡΕΣ : Cv, π
Έχουμε U= q - w + Σμιni ή dU = TΔS -PΔV + Σμιdni (1)
Aν δεν έχουμε μεταβολή των αριθμών των moles
dU = TΔS -PΔV
Aνεξάρτητες μεταβλητές Εντροπία και Όγκο
Το ολικό διαφορικό της U =U(T, P)
Αν θεωρήσουμε μια απειροελάχιστη μεταβολή της Εσωτερικής Ενέργειας είναι το άθροισμα κάθε μιας από τις μερικές διαφορικές παράμετρες εκτατικών ιδιοτήτων (ενώ οι άλλες εκτατικές ιδιοόήτες παραμένουν σταθερές)
έχουμε dU = (θU/θS)V dS +(θU/θV)SdV (2)
σύγκριση (1) και (2) και θέτοντας
Ανoικτό σύστημα με πανομοιότυπο αριθμο σωματιδίων ( 1 συστατικό)
η συνάρτηση της εσωτερικής ενέργειας δίνεται με τη γενική της μρφή με την γενική της μορφή U= U(S, V ,n)
dU = TΔS -PΔV +Σμidni
dU = (θU/θS)V,n dS +(θU/θV)S,nSdT + Σ(θU/θn1)S,V, dn
Οι μερικές διαφορικές παράγωγοι που είδαμε, μας δίνουν tiw άλλες εντατικές ιδιότητες
(θU/θS) V,n1, n2,.. είναι ταυτόσημη με την θερμοκρασία Τ
και μπορεί να οριστεί ως η μερική παράγωγος της εσωτερικής ενέργειας U ως προς την εντροπία S με σταθερό τον όγκο και τα moles
(θU/θV)S,n1, n2... είναι ταυτόσημη με την Πίεση P
και μπορεί να οριστεί ως η μερική παράγωγος της εσωτερικής Ενέργειας U ως προς τoν όγκο μεαθερά εντροπία και τα moles
(θU/θn1)S,V, n2, n3...ni. είναι ταυτόσημη με το χημικό δυναμικό του συστατικού 1 μ1
(θU/θn2)S,V, n1, n3...ni. είναι ταυτόσημη με το χημικό δυναμικό του συστατικού 2 μ2 κ.λ.π.
, Μέσα από την Εσωτερική Ενέργεια ορίζεται και το χημικό δυναμικό ενός είδους ως η μερική παράγωγός της προς τον αριθμό σωματιδίων
Αποτελεί τον ρυθμός μεταβολής της Εσωτερικής Ενέργειας του συστήματος λόγω της αλλαγής στον αριθμό των ατόμων ή μορίων των ειδών
Έτσι είναι η μερική παράγωγος της Εσωτερικής ενέργειας σε σχέση με την ποσότητα των ειδών ενώ οι συγκεντρώσσεις των άλλων ειδών παραμένουν σταθερές . Όταν η Εντροπία και ο Όγγκος διατηρούνται σταθερά, και ο αριθμός των σωματιδίων εκφράζεται σε mol,
¨οπου Χημικό Δυναμικό μ ορίζεται ως η μερική παράγωγος της εσωτερικής ενέργειας U ως προς τον αριθμό των moles ενός συστατικού με σταθερές τις άλλες εκτατικές ιδιότητες (Π.χ. S, V, T n2, ...)
OI ΘΕΡΜΟΔΥΝΑΜΙΚΕΣ ΣΤΑΘΕΡΕΣ ΠΟΥ ΕΞΑΓΟΝΤΑΙ ΑΠΟ ΤΗΝ ΕΣΩΤΕΡΙΚΗΣ ΕΝΕΡΓΕΙΑ
dU = θU/θV)TdV + (θU/θΤ)PdΤ αν διαιρέσουμε με το θΤ έχουμε και (θU/θΤ)Ρ = θU/θV)TV .(θV/θΤ)Ρ+ [(θU/θΤ)PdT ]/dT
(θU/θΤ)Ρ = πτ.(θV/θΤ)Ρ+ CV
H θερμοχωρητικότητα υπό σταθερό όγκο CV = (θU/θT)V
Η ισόθερμη μεταβολή της Εσωτερικής Ενέργειας όταν αλλάζει ο όγκος π= θU/θV)T
Ο συντελεστής γραμμικής διαστολής α = 1/Τ. (θV/θΤ)Ρ
ΑΠΟ ΤΗΝ ENΘΑΛΠΙΑ (Η)
ΕΝΤΑΤΙΚΕΣ ΠΑΡΑΜΕΤΡΟΙ ΠΟΥ ΠΡΟΚΥΠΤΟΥΝ ΕΙΝΑΙ;
Η ΘΕΡΜΟΚΡΑΣΙΑ( P, n σταθ) ΟΓΚΟΣ (S, n σταθ), ΧΗΜΙΚΟ ΔΥΝΑΜΙΚΟ (S, P σταθ)
( ΘΕΡΜΟΟΧΩΡΗΤΙΚΟΤΗΤΑ ΥΠΟ ΣΤΑΘΕΡΗ ΠΙΕΣΗ, ΑΔΙΑΒΑΤΙΚΗ ΣΥΜΠΙΕΣΤΟΤΗΤΑ )
Προεργασία: Παράγουμε μια πιο κατάλληλη σχέση της Ενθαλπίας ώστε από αυτήν να προχωρήσουμε στην εξαγωγή εντατικών συναρτήσεων
Από τον ορισμό της Ενθαλπίας H= U +PV +Σμini και την διαφορική και dH = dU + dPV +Σμidni
Aν δεν έχουμε μεταβολή των αριθμών των moles
H= U +PV και την διαφορική και dH = dU + dPV
Από την βασική της U που διαφοροποιούμε και αντικαθιστούμε
ανεξάρτητες μεταβλητές Εντροπία, Πίεση
U = TS -PV και dU = TdS -PdV κΙ dH =dU + PdV +VdP και έχοντας dU =TdS (εάν η ανταλλαγή θερμότητας γίνεται υπό στααθερά V, n1, n2,...n)
με αντικατάσταση έχουμε
dH = TdS +VdP (1)
και παίρνοντας το διαφορικό της Ενθαλπίας
Το ολικό διαφορικό της Η =Η(S, P)
Αν θεωρήσουμε μια απειροελάχιστη εταβολή της Εσωτερικής Ενέργειας είναι το άθροισμα κάθε μιας από τις μερικές διαφορικές παράμετρες εκτατικών ιδιοτήτων (ενώ οι άλλες εκτατικές ιδιοόήτες παραμένουν σταθερές) έχουμε
dΗ = (θΗ/θS)P dS +(θΗ/θP)SdP (2)
ανoικτό σύστημα με πανομοιότυπο αριθμο σωματιδίων 1 συστατικό
ενώ η συνάρτηση της εσωτερικής ενέργειας με την γενική της μορφή U= U(S, V ,n)
dH = TΔS + VdP +Σμdn
dΗ = (θΗ/θS) PndS,n dS +(θΗ/θP)S,ndP + Σ(θΗ/θV)S,V dn
Και τώρα μπορούμε να πάρουμε τα θερμοδυναμικά παράγωγα - Εντατικές παραμέτρους
Από την ενθαλπία σε αδιαβατική μεταβολή
dH = TdS +VdP και την dΗ = (θΗ/θS) PndS,n dS +(θΗ/θP)S,ndP
προκύπτει η καταστατική εξίσωση της Θερμοκρασίας για ανοικτό σύστημα με 1 συστατικό
(θΗ/θS)p είναι ταυτόσημη με την θερμοκρασία Τ(S,P) και
Από την ενθαλπία σε αδιαβατική μεταβολή : dH = TdS +VdP προκύπτει η καταστατική εξίσωση του όγκου ενώ ΔS= Q/T
(θΗ/θΡ)S είναι ταυτόσημη με τον Όγκο V (S,P)
Έτσι, για συστατικά n1, n2, ...
Οι μερικές διαφορικές παράγωγοι που είδαμε, μας δίνουν τις άλλες εντατικές ιδιότητες
(θΗ/θS) P,n1, n2,.. είναι ταυτόσημη με την θερμοκρασία Τ και μπορεί να οριστεί ως η μερική παράγωγος της Ενθαλπίας ως προς την εντροπία S με σταθερό τον όγκο και τα moles
(θΗ/θP)S,n1, n2... είναι ταυτόσημη με την Πίεση P και μπορεί να οριστεί ως η μερική παράγωγος της ενθαλπίας ως προς τoν όγκο με σταθερά εντροπία και τα moles
OI ΘΕΡΜΟΔΥΝΑΜΙΚΕΣ ΣΤΑΘΕΡΕΣ ΠΟΥ ΕΞΑΓΟΝΤΑΙ ΑΠΟ ΤΗΝ ΕΝΘΑΛΠΙΑ
dH = TdS +VdP +Σμdn Σε Ισοβαρή διαδικασία και για ένα συσταρικό, έχουμε dH = TdS και για μια μεταβολή της θερμοκρασίας dT φτάνουμε στην θερμοχωρητικότητα υπό σταθερή πίεση : είναι το πηλικο του ποσού της θερμότητας που πρέπει να προσφέρουμε σε ένα σώμα για να προκαλέσουμε μεταβολή της θερμοκρασίας του κατά dΤ προς την μεταβολή dT
Θερμοχωρητικότητα υπό σταθερή πίεση Cp = T(θS/θΤ)p,n = (θΗ/θΤ)p,n
dH = TdS +VdP +Σμdn Σε αδιαβατική διαδικασία (ΔS= Q/T) έχυμε dH = VdP και
για μια μεταβoλή τoυ όγκου dV φτάνυμε στην
Αδιαβατική συμπιεστότητα : θΗ/θP)S = V(θΡ/θV)T
(είναι μια ιδιότητα της ουσίας να αλλάζει τν όγκο της υπό την επίδραση μιας συνολικής ομοιόμορφης πίεσης)
π = V(θΡ/θV)T,n =(θΗ/θP)S,n
ΑΠΟ ΤΗΝ ΕΝΕΡΓΕΙΑ GIBBS (G)
ΕΝΤΑΤΙΚΕΣ ΠΑΡΑΜΕΤΡΟΙ ΠΟΥ ΠΡΟΚΥΠΤΟΥΝ ΕΙΝΑΙ;
Η ΘΕΡΜΟΚΡΑΣΙΑ( P, n σταθ) ΠΙΕΣΗ (S, n σταθ), ΧΗΜΙΚΟ ΔΥΝΑΜΙΚΟ (S, P σταθ)
dU = TΔS -PΔV + ΣμιNi μπορούμε να πάρουμε την ΣμιNi = U - TS +PV
Όμως μέσω μετασχηματισμών Legrendre έχπυμε G= U -TS +PV Καταλήγουμε σε G = ΣμιNi
H Ενέργεια Gibbs είναι γνωστή και σαν Χημικό δυναμικό
εκτατική ιδιότητα και εξαρτάται από το μέγεθος του συστήματος ή αλλιώς την ποσότητα της ουσίας . Μετράτια σε Joules ή cal Aνεξάρτητες μεταβλητές πίεση και θερμοκρασία
Από την
εκφράζεται ως : G(p,T) = H - TS που είναι ίδιο με G(p,T, n)= U +pV -TS + ΣμιNi
Για μια απειροστή αντιστρεπτή μεταβολή της G
dG = dU + pdV +Vdp -d(ST) = dU +pdV + Vdp -SdT -TdS + ΣμιdNi επειδή ισόθερμη , ισοβαρής και αντιστρεπτή) dU=0, dT=0, dP=0
έχουμε ΄την μορφή της Θεμελιώδους εξίσωσης gibbs
dG = + Vdp -SdT + ΣμιdNi (1)
dG = (θG/θT)V,n dT +(θG/θP),T,ndP + Σ(θG/θn)S,V dn (2)
από την (1) και (2) έχουμε
(θG/θT)V,n dT =-S
(θG/θT)V,n dT = V
(θG/θn1)S,V,n2, n3...ni. = μ1 χημικό δυναμικό συστατικού 1 που είναι η ενέργεια που μπορεί να απορροφηθεί ή να απελευθερωθεί λόγω αλλαγής του αριθμού των σωματιδίων με σταθερά τα υπόλοιπα . Το ίδιο για n2, n3 ,,,
Το χημικό δυναμικό ενός είδους εκφράζεται ως η μερική παράγωγος της ενέργειας Gibbs προς τον αριθμό σωματιδίων
και ορίζεται ως ο ρυθμός μεταβολής της ελεύθερης ενέργειας G του συστήματος λόγω της αλλαγής στον αριθμό των ατόμων ή μορίων των ειδών
Έτσι είναι η μερική παράγωγος της ελεύθερης ενέργειας σε σχέση με την ποσότητα των ειδών ενώ οι συγκεντρώσσεις των άλλων ειδών παραμένουν σταθερές και όταν η θερμοκρασία και η Πίεση διατηρούνται σταθερές, και ο αριθμός των σωματιδίων εκφράζεται σε mol, το χημικό δυναμικό είναι η Ελεύθερη ενέργεια Gibbs
ΑΠΟ ΤΗΝ ΕΝΕΡΓΕΙΑ HELMHOlTZ (F ή Α)
ΕΝΤΑΤΙΚΕΣ ΠΑΡΑΜΕΤΡΟΙ ΠΟΥ ΠΡΟΚΥΠΤΟΥΝ ΣΑΝ ΘΕΡΜΟΔΥΝΑΜΙΚΑ ΠΑΡΑΓΩΓΑ
Στα άλλα θερμχωρητικά Δυναμικά Ενέργεια Gibbs και Αλεύθερη Ενέργεια Helmholtz
F (ή Α)= U-TS ώστε F= F(T, V, n1, n2...)
dF =d(U -TS ) = dU- d(TS) = TdS - PdV - SdT -Tds
dF =- PdV - SdT (1)
dF = (θF/θV),TndV + (θF/θT)V,n dT + Σ(θF/θn),T,V dn (2)
(θF/θV),Tn = -P
(θF/θT)V,n =-S
(θF/θn),T,V = μ
ΕΝΤΡΟΠΙΚΕΣ ΕΝΤΑΤΙΚΕΣ ΠΑΡΑΜΕΤΡΟΙ,
ΠΟΥ ΠΡΟΚΥΠΤΟΥΝ ΣΑΝ ΘΕΡΜΟΔΥΝΑΜΙΚΑ ΠΑΡΑΓΩΓΑ
ΕΝΤΡΟΠΙΚΩΝ ΕΚΤΑΤΙΚΩΝ ΣΥΝΑΡΤΗΣΕΩΝ
ΑΠΟ ΤΗΝ ΕΝΤΡΟΠΙΑ (S)
ΕΝΤΡΟΠΙΚΑ ΘΕΡΜΟΥΝΑΜΙΚΑ ΕΙΝΑΙ 1/T(V, n..), P/T( U, n..), μ/T(P, V, n1...nν-1)
OI ΘΕΡΜΟΔΥΝΑΜΙΚΕΣ ΣΤΑΘΕΡΕΣ ΠΟΥ ΕΞΑΓΟΝΤΑΙ ΑΠΟ ΤΗΝ ΕΝΤΡΟΠΙΑ
Στηην θεμελιώδη σχέση για την εσωτερική ενέργεια : ΔU = δq - δw
Επίσης Η μεταβολή της Εντροπία ορίζεται από την σχέση ΔS = δq/T και επομένως δq = ΔS.T και αντικαθιστώντας έχουμε
dU = TΔS -PΔV + Σμιdni
λύνοντας ως προς ΔS έχουμε
ΔS = dU/Τ +-(P/Τ)ΔV - Σ (μι/Τ) dni
και ενώ η S είναι συνάρτηση εκτατικών ιδιοτήτων κάθε απλού συστήματος ως μια συνεχής, παραγωγίσιμος και μονοτόνως αύξουσα συνάρτηση της ενέργειας
S= S(U, V, n1,...ni)
ισχύει : dS = (θS/θU)V,n1...nidU + (θS/θV)U,n1...ni dV - Σ(θS/θn),U,V dn
(θS/θU)V,n1...ni =1/T
(θS/θV)U,n1...ni = P/T
(θS/θn1),U,V,n2,...ni = - μ1/T
(θS/θn2),U,V,n1,...ni = - μ2/T
....
Tο Θεώρημα τυ EULER για ομγενείς συναρτήσεις
Εάν σε μια συνάρτηση ν μεταβλητών και n βαθμού πάρουμε το ολικό διαφορικό σαν άθροισμα των μερικών διαφορικών της, Οι θερμοδυναμικές συναρτήσεις που προκύπτουν Π.χ. U = TdS -PdV είναι 1ου βαθμού ως προς τις μεταβλητές ποσότητες. Με την διαφοροποίηση δίνουν τις παράγωγες μερικές θερμοδυναμικές συναρτήσεις που είναι μηδεσνικού βαθμού
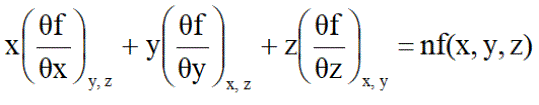
-
 Πλατεία Guggenheim
Πλατεία Guggenheim
PHGES
https://www.scribd.com/document/480341082/10-%CE%94%CE%B9%CE%B1%CF%86%CE%BF%CF%81%CE%B9%CF%83%CE%B7-%CF%83%CF%85%CE%BD%CE%B1%CF%81%CF%84%CE%B7%CF%83%CE%B5%CF%89%CE%BD-%CF%80%CE%BF%CE%BB%CE%BB%CF%89%CE%BD-%CE%BC%CE%B5%CF%84%CE%B1%CE%B2%CE%BB%CE%B7%CF%84%CF%89%CE%BD
https://el.wikipedia.org/wiki/%CE%94%CE%B9%CE%B1%CF%86%CE%BF%CF%81%CE%B9%CE%BA%CF%8C%CF%82_%CE%BB%CE%BF%CE%B3%CE%B9%CF%83%CE%BC%CF%8C%CF%82
ΦΥΣΙΚΟΧΗΜΕΙΑ Βασική θεώρηση Ν.Α, Κατσάνου
2.3. Η θερμότητα ως μορφή μεταφοράς ενέργειας σε μια θερμοδυναμική διαδικασία
Συνάρτηση κατάστασης εσωτερική ενέργεια U
Ελεύθερη ενέργεια Γκιμπς - Βικιπαίδεια
Ελεύθερη ενέργεια Χέλμχολτς - Βικιπαίδεια
Θερμοδυναμικά δυναμικά - Βικιπαίδεια
Ένα απλό στυλιζαρισμένο διάγραμμα του ψυκτικού κύκλου συμπίεσης ατμών μιας αντλίας θερμότητας: 1) συμπυκνωτής, 2) βαλβίδα διαστολής, 3) εξατμιστής, 4) συμπιεστής.

