Δήμητρα Σπανού, συνταξιούχος καθηγήτρια χημικός Β/θμιας Εκπ/σης-
υπό κατασκευή
ΘΕΡΜΟΔΥΝΑΜΙΚΗ- ΕΙΣΑΓΩΓΙΚΟ
Θερμοδυναμική είναι η μελέτη μετατροπής της ενέργειας από μηχανική ενέργεια- εργο σε θερμότητα και αντίστροφα μέσα από μελέτη θερμοδυναμικών διεργασιών που είναι οι μεταβάσεις από την μια κατάσταση ενός συστήματος σε άλλη.
Η Κλασσική Θερμοδυναμική που διατυπώθηκαν χωρίς την βοήθεια θεωριών περί δομής της ύλης όπως η Μοριακή Θεωρία, βασίζεται σε νόμους και αξιώματα εκ των οποίων τα δύο σημαντικότερα είναι:
Το πρώτο θερμοδυναμικό αξίωμα ή Πρώτος νόμος της θερμοδυναμικής αναφέρει στην διατήρηση της ενέργειας
Το δεύτερο θερμοδυναμικό αξίωμα ή Δεύτερος νόμος της Θερμοδυναμικής αναφέρει την κατεύθυνση μεταφοράς της θερμότητας και την εισαγωγή της έννοιας της εντροπίας.Η εφαρμογή αυτού του 2ου νόμου διευρύνει τους ορίζοντες της θερμοδυναμικής πέραν των θερμικών μηχανών σε άλλα πεδία, όπως η απόδοση των χημικών αντιδράσεων (Χημική Θερμοδυναμική), η μέγιστη τάσης μιας ηλεκτρικής στήλης, η μεταβολή τάσεως ατμών υγρού με την θερμοκρασία κ.α.
Η Θερμοδυναμική όπως και άλλες επιστήμες εξελίσσεταικαι από τις αφηρημένες έννοιες προχωρεί σε ειδικά συμπεράσματα που αποδεικνύονται πειραματικά.
Τα φαινόμενα της θερμοδυναμικής περιγράφονται με τις θερμοδυναμικές μακροσκοπικές παραμέτρους οι οποίες χωρίζονται σε εκτατικές και εντατικές
Τα ποικίλα είδη των μεταβολών (σε όγκο, θερμοκρασία, ύληκ.α.)
Δεδομένου ότι μεγέθη που περιγράφουν μια κατάσταση τα ονομάζουμε καταστατικά, πολλές από τις μεταβολές αυτές εμφανίζονται απλά σαν διαφορικά των καταστατικών συναρτήσεων και στην εξέλιξή της εισάγει ευρέως την χρήση του διαφορικού λογισμού.
Η ανάπτυξη της θεωρίας που είχε ξεκινήσει από τα διάφορα είδη μεταβολών όπως ο θερμοδυναμικός κύκλος του CARNOT προχωρά προς τις καταστατικές συναρτήσεις που τις θεωρεί σαν βασικές έννοιες όπως η ενέργεια, η εντροπία κ.α.
Τέλος να σημειώσουμε ότι η κλασσική Θερμοδυναμική εξετάζει τις ιδιότητες των συστημάτων σε κατάσταση ισορροπίας.
Τελευταία όμως έχει επεκταθεί έξω από τις περιοχές ισορροπίας.
- ΜΕ ΤΗΝ ΧΡΗΣΗ ΤΩΝ ΜΑΘΗΜΑΤΙΚΩΝ
-
ΑΠΟ ΔΙΑΓΡΑΜΜΑΤΑ ΘΕΡΜΟΔΥΝΑΜΙΚΩΝ ΣΥΝΑΡΤΗΣΕΩΝ
ΜΕΤΑΒΟΛΕΣ ΠΟΣΟΤΗΤΩΝ ΠΟΥ ΔΕΝ ΕΙΝΑΙ ΔΙΑΦΟΡΙΚΑ ΣΥΝΑΡΤΗΣΕΩΝ
-
ΜΕ ΤΗΝ ΟΛΟΚΛΗΡΩΣΗ ΥΠΟΛΟΓΙΖΟΝΤΑΙ
- ΓΕΝΙΚΑ
Το αντίθετο δηλαδή η εύρεση της αρχικής συνάρτησης από την παράγωγό της λέγεται ολοκλήρωση
Το ολοκλήρωμα είναι μια από τις σημαντικές έννοιες της μαθηματικής ανάλυσης και με απλουστευμένο τρόπο μπορεί να αναπαρασταθεί ως ανάλογο του αθροίσματος για έναν άπειρο αριθμό απειροελάχιστων όρων
Πριν προχωρήσουμε θυμόμαστε ακριβώς τι είναι:
Το Διαφορικό είναι ένα γραμμικό μέρος της αύξησης μιας συνάρτησης Συνήθως γράφεται df (το διαφορικό είναι ο τελεστής)
Το διαφορικό μπορεί να είναι τέλειο διαφορικό ή μη τέλειο διαφορικό
Το τέλειο διαφορικό παριστάνεται με το δ και ο υπολογισμός του εξαρτάται από τον τρόπο (πορεία ) από την αρχική (πριν την μεταβολή) στην τελική (μετά την μεταβολή) κατάσταση
Το mh τέλειο διαφορικό παριστάνεται με το δ και ο υπολογισμό του γίνεται, εάν καθοριστεί λεπτομερώς η πορεία από την αρχική στην τελική κατάσταση
Το Ολικό Διαφορικό ή τέλειο διαφορικό ή ολική παράγωγο ή απλά διαφορικό μιας συνάρτησης πολλών μεταβλητών
είναι μια μικρή αύξηση (μεταβολή) της συνάρτησης f το οποίο προκύπτει όταν οι μεταβλητών είναι απειροστά μικρές ,δηλαδή τείνουν στο μηδέν
Προκύπτει ως άθροισμα συνεισφορών από τις μερικές διαφορικές παραμέτρους εκάστου παράγοντα, ενώ οι υπόλοιποι παραμένουν σταθεροί
Δηλαδή η μερική παράγωγος είναι μια γενίκευση της έννοιας της παραγώγου και προκύπτει σαν ο λόγος της αύξησης (μεταβολής) μιας συνάρτησης για μια επιλεγμένη μεταβλητή προς την αύξηση της μεταβλητής αυτής Συμβολίζεται με στην περίπτωση που αναφερόμαστε στην μεταβλητή x
Μια διαφορική εξίσωση είναι μια ειδική περίπτωση συναρτησης και μπορεί να περιλαμβάνει παραγώγους, συναρτήσεις και ανεξάρτητες μεταβλητές (οπωσδήποτε μια τουλάχιστον παράγωγο)
Τα τέλεια διαφορικα που δίνει την διαφορά μεταξύ δύο καταστάσεων θερμοδυναμικής συνάρτησης δηλαδή, της τελικής και αρχικής είναι ανεξάρτητο από τον τρόπο που έγινε η μεταβολή αυτή και υπολογίζεται μόνο από την μεταβολή στην αρχική και τελική κατάσταση
Το σύμβολο Δ δίνει την διαφορά μεταξύ δύο καταστάσεων θερμοδυναμικής συνάρτησης δηλαδή, της τελικής και αρχικής ιπ.χ. ΔU είναι η μεταβολή στην εσωτερική ενέργεια
Τα μη τέλεια διαφορικα που δίνει την διαφορά μεταξύ δύο καταστάσεων θερμοδυναμικής συνάρτησης δηλαδή, της τελικής και αρχικής δεν είναι ανεξάρτητο από τον τρόπο που έγινε η μεταβολή αυτή Μπορούν να υπολογιστούν μόνο αν καθοριστεί ο τρόπος μεταβολής
Το σύμβολο δ δίνει την απειροστή ποσότητα μεταβολής χωρίς να είναι διαφορικά συναρτήσεων. π.χ. δw, δq
Ολοκλήρωση είναι μια διαδικασία επίλυσης μιας διαφορικής εξίσωσης
διαφορά με το σύμβολο Δ που δίνει την διαφορά μεταξύ δύο καταστάεων τελικής και αρχικής και είναι ανεξάρτητο από τον τρόπο που έγινε η μεταβολή αυτή παρά μόνο από την αρχική και τελική κατάσταση π.χ. ΔU είναι η μεταβολή στην εσωτερική ενέργεια
ΥΠΟΛΟΓΙΣΜΟΣ ΘΕΡΜΟΤΗΤΑΣ ΚΑΙ ΕΡΓΟΥ ΣΕ ΕΣΩΤΕΡΙΚΑ ΣΥΣΤΗΜΑΤΑ ΜΕ ΟΛΟΚΛΗΡΩΣΗ
Για τον υπολογισμό του έργου και της εσωτερικής ενέργειας σε συστήματα χρησιμοποιούνται τα αλγεβρικά αθροίσματα της μεταβολής της θερμότητας και του έργου . Αυτά εμφανίζονται και υπολογίζονται μόνο κατά την διάρκεια της μεταβολής τους δηλαδή δεν αποτελούν μόνιμες ιδιότητες των συστημάτων.
Και τα δύο είναι μη τέλεια διαφορικά και η τιμή τους εξαρτάται από την πορεία της θερμοδυναμικής διαδικασίας . Ως εκ τούτου δεν μπορούν να είναι καταστατικά μεγέθη τα οποία όπως αναφέρθηκε μπορούν να περιγράφουν μια κατάσταση.
Και τα δύο μεγέθη είναι τα κύρια στοιχεία για να διατυπωθεί ο πρώτος νόμος της θερμοδυναμικής που λέει:
Εάν πρόκειται για ένα κλειστό σύστημα που τα moles n1, n2, ni παραμένουν σταθερά.
Το ποσό της θερμότητας που απορροφά ένα θερμοδυναμικό σύστημα είναι ίσο με το αλγεβρικό άθροισμα της μεταβολής της εσωτερικής του ενέργειας (ΔU) και του έργου. q= ΔU +w ή
Η μεταβολή στην εσωτερική ενέργεια του συστήματος οφείλεται στην ενέργεια που προσφέρεται (ή αφαιρείται) από το περιβάλλον τόσο υπό μορφή θερμότητας όσο και υπό μορφή έργου ΔU = q -w
Για μια μικρ΄μεταβολή στην ενέργεια χρησιμοποιούμε το dU (τέλειο διαφορικο) ενώ για το έργο και την θερμότητα (μη τέλεια διαφορικά) για απειροστές μεταβολές τα δw και δq dU = δq -δw
ΔU = δq - δw
H Θερμότητα και η εσωτερική ενέργεια είναι δυνατόν να υπολογιστούν από καταστατικές εξισώσεις
ΥΠΟΛΟΓΙΣΜΟΣ ΤΟΥ ΕΡΓΟΥ ΑΕΡΙΟΥ ΣΕ ΙΣΟΘΕΡΜΗ ΑΝΤΙΣΤΡΕΠΤΗ ΔΙΕΡΓΑΣΙΑ
Αν θεωρήσουμε ότι η θερμοκρασία κατά την μεταβολή παραμένει σταθερή η προσφερόμενη από το περοβάλολο θερμότητα μετατρέπεται σε έργο
δq ΄= δw
 Το έργο αυτό εάν πρόκειται για αέριο το παραγώμενο έργο συνδέεται με την αλλαγή στον όγκο . Εάν η πίεση παραμένει σταθερή
Το έργο αυτό εάν πρόκειται για αέριο το παραγώμενο έργο συνδέεται με την αλλαγή στον όγκο . Εάν η πίεση παραμένει σταθερή
δw=p ΔV
Tότε το έργο αυτό υπολογίζεται από το μβαδόν του διαγράμματοςστο οποίο η Πίεση παραμένει σταθρή.
Τι συμβαίνει όμως άν η πίεση μεταβάλλεται ;

Σχ. 4.6 Σε μια τυχαία αντιστρεπτή μεταβολή το έργο κατά την εκτόνωση του αερίου από όγκο V1 σε όγκο V1+ΔV είναι ίσο με το εμβαδόν της επιφάνειας με το κίτρινο χρώμα.

Σχ. 4.7 Σε μια τυχαία αντιστρεπτή μεταβολή το έργο του αερίου κατά τη μεταβολή του από το Α στο Β είναι ίσο με το εμβαδόν κάτω από την γραμμή του διαγράμματος.(Φυσική (Β΄ Λυκείου - Θετικών Σπουδών) - Βιβλίο Μαθητή (Εμπλουτισμένο))
Αν θεωρήσουμε ότι η μεταβολή αυτή περνά από διαδοχικές καταστάσεις ισορροπίας και η μεταβολή της πίεσης είναι ελάχιιστη ( όπως στο σχήμα) μπορούμε να την θεωρήσουμε σταθερή και να υπολογίσουμε όπως στο προηγούμενο. Το έργο είναι ίσο με το γραμμοσκιασμένο εμβαδόν
Εάν μια τέτοια μταβολή θεωρήσουμε ότι περνά από πολλές διαδοχικές καταστάσεις ισορροπόας μπορούμε να την διαιρέσουμε νοητά σε πολλές μικρές μεταβολές και να θεωρήσουμε σαν το συνολικό έργο το γραμμοσκιασμέενο εμβαδόν που περιέχεται στην καμπύλη και στις ευθείες αρχικού και τελικούνόγκου και στον άξονα χτιμές
Για να πάρουμε όμως τιμή για το έργο θα πρέπει η καμπύλη να είναι καμπύλη συνάρτησης και τότε να υπολογίσουμε το ολοκλήρωμα αυτής για τιμές μεταξύ V1 και V2
Αυτό γίνεται αν θεωρήσουμε το σύστημά μας ιδανικό αέριο για το οποίο ισχύει η καταστατική εξίσωση PV= nRT και εδώ η πίεση είναι συνάρτηση του όγκου P=F(V) P=nRT/V
Το έργο που αντιστοιχεί στο γραμμοσκιασμένο εμβαδόν του διαγράμματος
που δίνεται με ολοκλήρωμα
η
Ρ είναι συνάρτηση του όγκου και αντικαθιστούμε

Με ολοκλήρωμα όμως θα μπορούσαμε να υπολογίσουμε και την αρχική περίπτωση όταν η πίεση είναι σταθερή, θωρώντας την P= F(V) = σταθρή ενώ,
Τότε το έργο δίνεται από την επίλυσή της που είναι W=p [V]1.2 =P (V2-V1)
ΥΠΟΛΟΓΙΣΜΟΣ ΤΗΣ ΘΕΡΜΟΤΗΤΑΣ ΑΠΟ ΤΗΝ ΕΝΤΡΟΠΙΑ ΜΕ ΟΛΟΚΛΗΡΩΣΗ
ΗΕντροπία είναι μια θερμοδυναμική ιδιότητα που δεν μπορεί να μετρηθεί άμεσα γιατί δεν έχει επιδράσεις στα όργανα μέτρησης, αλλά μόνο από άλλες θερμοδυναμικές παραμέτρους όπως η πίεση η θερμοκρασία ο όγκος. Η γνωστή βασική σχέση που δίνει την ποσότητα της θερμότητας και την μεταβολή της Εντροπίας είναι dS = δq/Τ
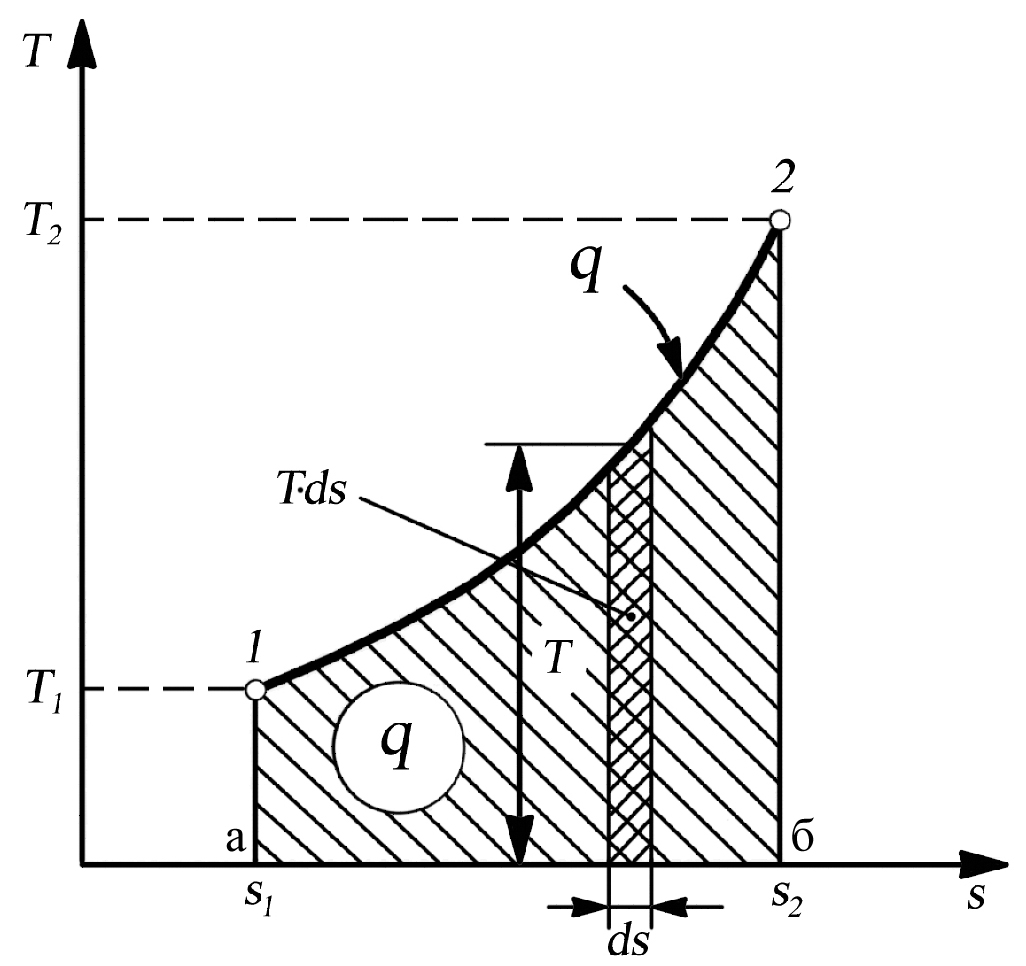 Απεικονίζοντας την σχέση αυτή σε διάγραμμα Τ-S μπορούμε να υπολογίσουμε την θερμότητα που απορροφάται αν επιλύσουμε ως προε δq (στοιχειώδης αλλαγή στην q και όχι τέλειο διαφορικό.
Απεικονίζοντας την σχέση αυτή σε διάγραμμα Τ-S μπορούμε να υπολογίσουμε την θερμότητα που απορροφάται αν επιλύσουμε ως προε δq (στοιχειώδης αλλαγή στην q και όχι τέλειο διαφορικό.
δq = dS.T
Για στοιχειώδεις μεταβολές μπορούμε να θεωρήσουμε το Τ σταθερό ώστε το γινόμενο ΤdS να δίνει την στοιχειώδη μεταβολή της θερμότητας δq1. Στο διάγραμμα αυτό απεικονίζεται με μικρό γραμμοσιασμένα παραλληλόγραμμα που παίρνουμε κάθε φορά που αλλάζουμε το Τ. Εάν αθροίσουμε όλα τα στοιχειώδη παραλληλόγραμμα θα πάρουμε το συνολικό ποσό θερμότητας που απορροφήθηκε. Αυτό μπορεί να γίνει μόνο με την ολοκλήρωση της σχέσης μεταξύ της αρχικής και της τελικής κατάστασης
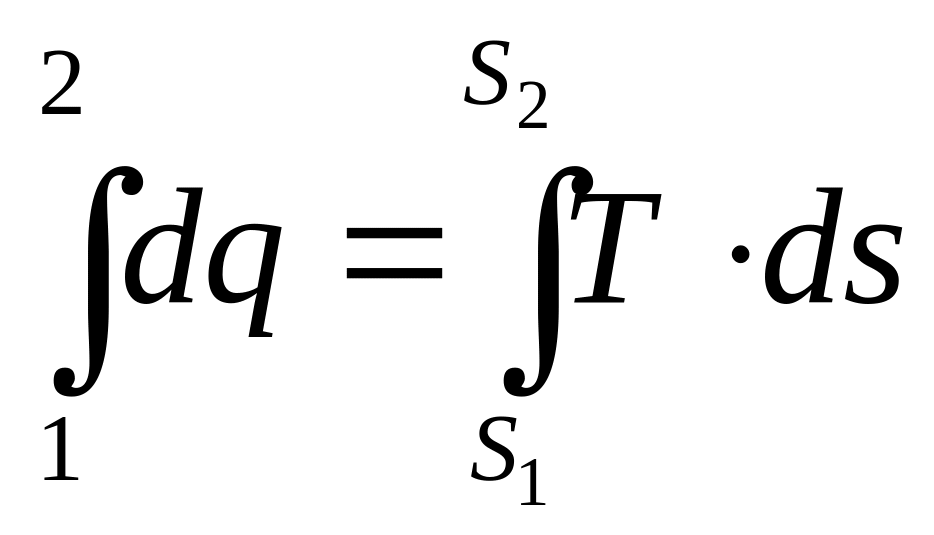 Για να προχωρήσουμε στον υπολογισμό πρέπει να γνωρίζουμε την σχέση που συνδέει τις τιμές της θερμοκρασίας με την εντροπία T=f(S)
Για να προχωρήσουμε στον υπολογισμό πρέπει να γνωρίζουμε την σχέση που συνδέει τις τιμές της θερμοκρασίας με την εντροπία T=f(S)
PHGES
https://www.scribd.com/document/480341082/10-%CE%94%CE%B9%CE%B1%CF%86%CE%BF%CF%81%CE%B9%CF%83%CE%B7-%CF%83%CF%85%CE%BD%CE%B1%CF%81%CF%84%CE%B7%CF%83%CE%B5%CF%89%CE%BD-%CF%80%CE%BF%CE%BB%CE%BB%CF%89%CE%BD-%CE%BC%CE%B5%CF%84%CE%B1%CE%B2%CE%BB%CE%B7%CF%84%CF%89%CE%BD
https://el.wikipedia.org/wiki/%CE%94%CE%B9%CE%B1%CF%86%CE%BF%CF%81%CE%B9%CE%BA%CF%8C%CF%82_%CE%BB%CE%BF%CE%B3%CE%B9%CF%83%CE%BC%CF%8C%CF%82
ΦΥΣΙΚΟΧΗΜΕΙΑ Βασική θεώρηση Ν.Α, Κατσάνου
2.3. Η θερμότητα ως μορφή μεταφοράς ενέργειας σε μια θερμοδυναμική διαδικασία
Ισόθερμη μεταβολή - Βικιπαίδεια

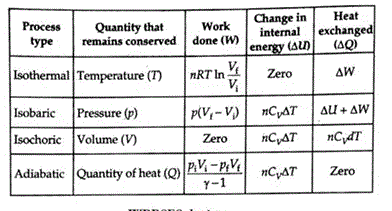
 στην περίπτωση που αναφερόμαστε στην μεταβλητή x
στην περίπτωση που αναφερόμαστε στην μεταβλητή x
